Clear Sky Science · zh
通过原位与动态交换策略进行多组分协同固载以构建分级生物药物
为什么构建更“智能”的药物很重要
当今最强效的许多药物是大型且脆弱的生物分子,例如蛋白质和酶。它们可以对抗癌症、杀灭有害细菌并加速愈合,但易受损且难以被准确递送到体内合适位置。本文描述了一种新方法,将多种这些脆弱成分一起“打包”到一种具有海绵状保护结构的材料内,使它们能够按顺序协同发挥更强的作用并减小副作用。
把晶体变成分子公寓楼
研究者从一种由金属离子和小有机构件构成的特殊多孔材料出发。它有点像微小而灵活的公寓楼,内部布满房间和走廊。研究显示,这种被称为沸石状嘧啶骨架的框架可以在蛋白质周围生长,使蛋白质最终被保护在晶体内部。该“原位”捕获不会压坏或失活蛋白质,精细成像证实它们均匀分布在内部,就像住在楼中每层的住户一样。
可变形的宿主用于表面修饰
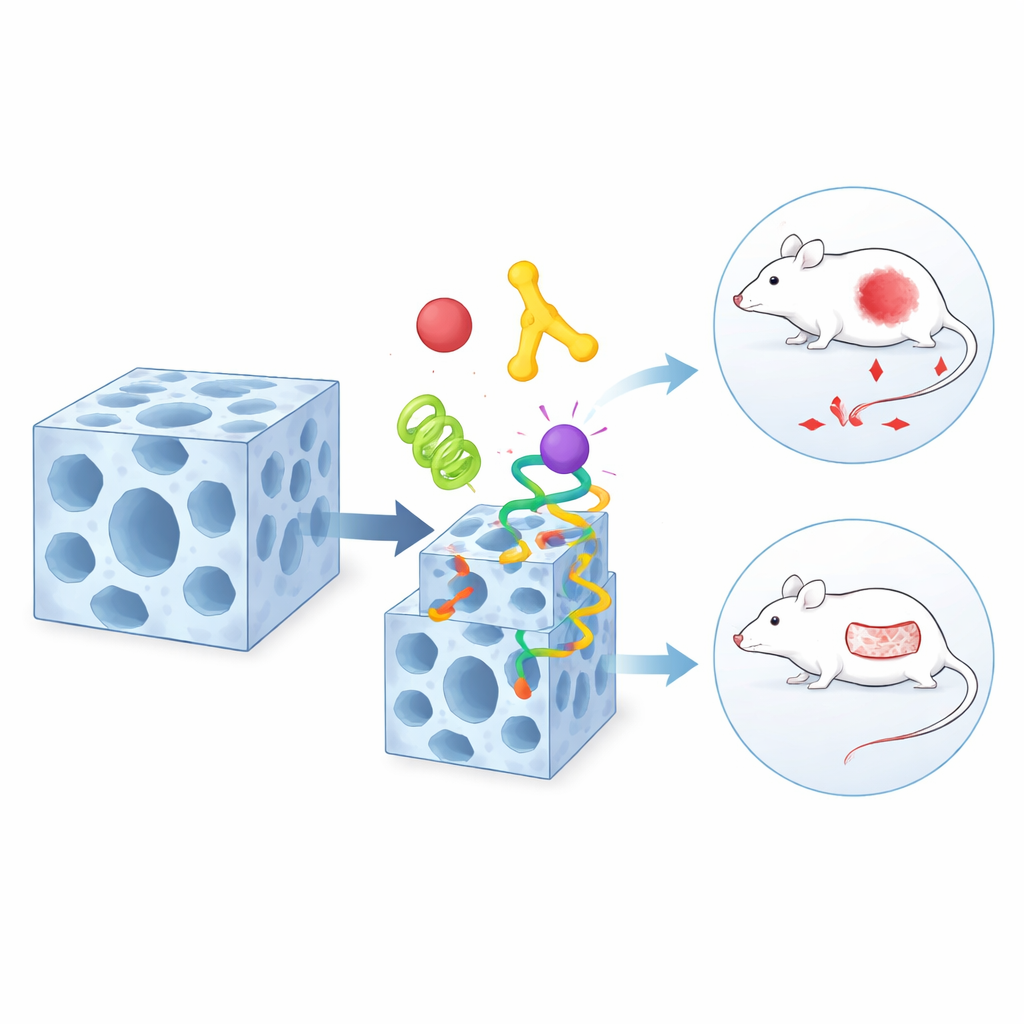
同一材料还具有一个令人惊讶的第二特性:在接触某些溶剂或水时,它的内部结构可以可逆地改变。在这一温和的形变过程中,框架中的一些化学键会松动然后重新形成。团队发现,蛋白质表面上的特定化学基团——例如某些氨基酸中的基团——能够利用这一短暂的薄弱时刻。它们暂时与框架原有的构件竞争,滑入表面附近新形成的“缺陷”中。因此,一层蛋白质主要锚定在晶体外部,而内部的蛋白质仍然保持原位。这种动态交换过程让科学家能够决定哪些成分位于深处、哪些装饰外壳。
设计酶的装配线
在内外空间都可控的情况下,作者构建了微小的酶学“装配线”。例如,在一个实例中,一种将糖转化为有害中间产物的酶被封锁在框架内部,而第二种能够安全分解该中间产物的酶则固定在表面附近。这种内外分布使反应比传统的核壳设计或酶的随机混合更快、更高效。由于外层酶更易被分子接近且有害中间体被迅速清除,系统在多次循环中保持活性,并更耐热、耐恶劣条件与重复使用。
智能抗癌与抗菌载体
当将该方法应用于医学时,其真正威力显现出来。团队在单个分层颗粒中组合了一个肿瘤靶向蛋白、一个消耗葡萄糖的酶和一种常规化疗药物。表面上的靶向成分引导颗粒到达癌细胞,酶通过消耗局部糖分削弱其能量供应,而小分子药物再给予致命一击。在带有人类肿瘤移植的小鼠中,这种三合一组合比任何单一成分或更简单排列的混合物更有效地缩小肿瘤。在另一种设计中,作者将抗菌肽和重塑组织的酶放在同一载体的不同区域,用于感染性皮肤伤口。在大鼠模型中,这些颗粒较传统治疗显著降低感染并加速难愈合伤口的闭合。

这项工作如何推动医学进步
对非专业读者而言,关键信息是这项研究将单一多孔晶体转变为可编程的多种疗法分子的“家”。通过决定谁住在内部、谁驻留在表面以及各自的比例,研究者可以在一个微小颗粒内协调分步治疗——先靶向、再攻击、然后修复。这一策略不仅保护了脆弱的生物药物,还使它们相互协助,从而带来更强、更精确的抗癌和抗菌疗法。相同的设计原则可被改造用于许多未来需要多组件在适当时间地点协同工作的“智能药物”。
引用: Yang, M., Meng, X., Shi, R. et al. Multicomponent synergistic immobilization via in-situ and dynamic exchange strategies for constructing hierarchical biopharmaceuticals. Nat Commun 17, 2208 (2026). https://doi.org/10.1038/s41467-026-69009-8
关键词: 金属有机框架, 酶固定化, 癌症纳米医学, 伤口愈合, 生物制剂递送