Clear Sky Science · zh
大肠埃希菌通过释放中性粒细胞胞外网维持增强子–启动子环路,促进结直肠癌转移
肠道菌与癌症的秘密通道
结直肠癌致死常常并非由肠内的原发肿瘤直接造成,而是因为癌细胞迁移至肝脏并在那里定植。本研究揭示了这一旅程中一位出乎意料的帮凶:一种常见的肠道细菌——大肠埃希菌。通过追踪从肠道细菌到肝脏具有攻击性的肿瘤的一连串事件,研究人员展示了微生物、免疫细胞与癌细胞内DNA构象如何协同助推转移,并提出了可中断这条链条的新思路。
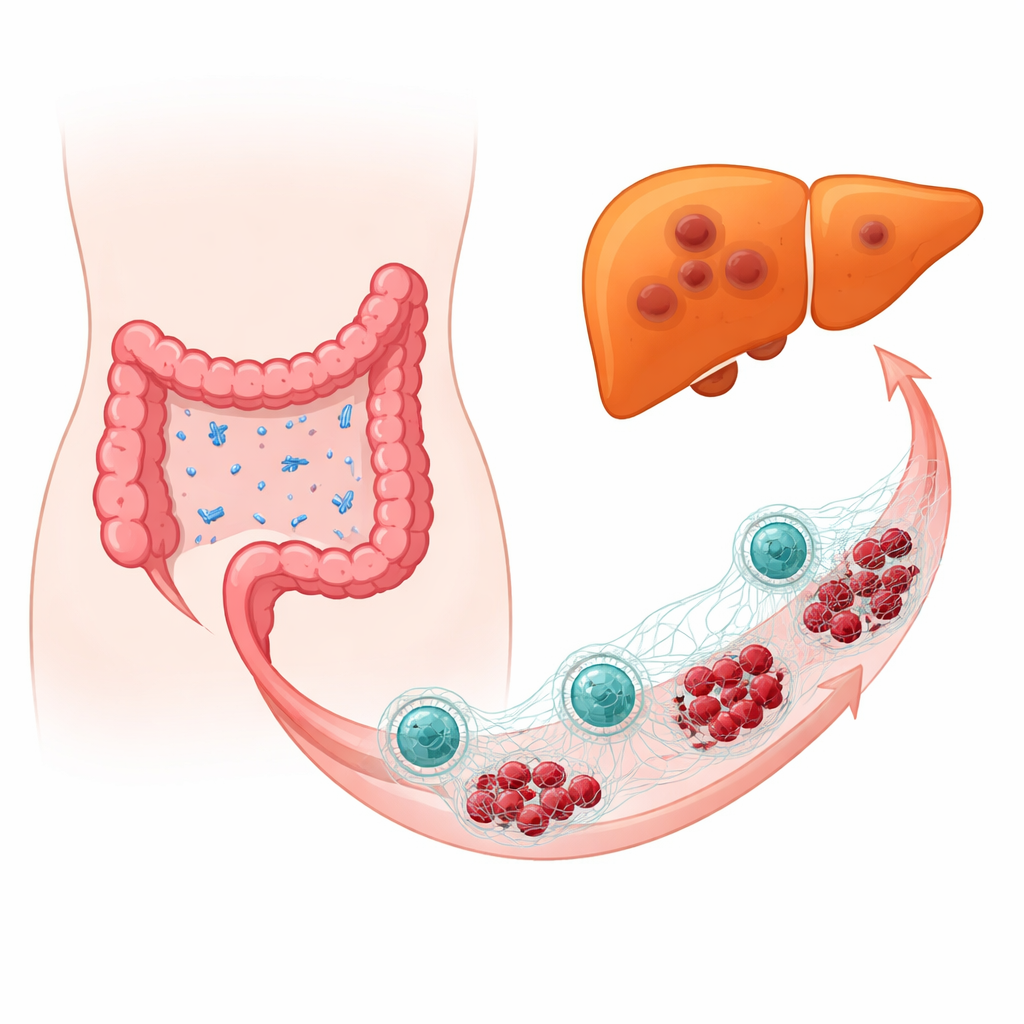
从“友好”细菌到敌对力量
研究团队分析了结直肠癌患者的肿瘤样本,将已发生肝转移者与未发生者比较。通过高分辨率的基于DNA的微生物谱分析,他们发现大肠埃希菌在已播散至肝脏的癌症中明显更为丰富。在小鼠模型和具有“人源化”免疫系统的老鼠中,将大肠埃希菌有意置于结直肠肿瘤附近,会使肝转移更大且更频繁,并推动肿瘤细胞向更具有运动性和侵袭性的表型转变。即便多数正常肠道菌群被抗生素清除,仅重新引入大肠埃希菌,细菌仍然促进肿瘤生长与扩散,表明并非一般性微生物组破坏,而是大肠埃希菌本身在发挥作用。
帮助癌细胞逃逸的免疫网
中性粒细胞——作为前线免疫细胞,通常用于捕捉并杀灭微生物——成为了关键的中介。作为对大肠埃希菌的反应,中性粒细胞释放出由DNA和毒性蛋白组成的网状结构,称为胞外网(extracellular traps)。这些网本意在捕获细菌,但在此情境下却无意中保护并助长了癌细胞。研究者用酶分解这些网或阻断其形成所需的关键酶时,肝转移缩小且肿瘤侵袭性下降。耗竭中性粒细胞也产生了类似的保护效果,这指向一个悖论:原本用于对抗感染的免疫反应被劫持,反而帮助癌症扩散。
从电信号到基因开关
细胞外黏稠的DNA网如何改变肿瘤细胞细胞核深处发生的事情?答案在于钙离子——一种在细胞内作为电信号的重要离子。研究显示,中性粒细胞胞外网提高了结直肠癌细胞表面的一种通道蛋白TRPC1的水平。TRPC1使更多钙离子涌入细胞,进而激活对钙敏感的调控因子NFATC3,并形成一个自我强化的循环以维持高水平的TRPC1。这股钙激增促使两个小蛋白S100A8与S100A9结合并随后与一个主要的生长控制蛋白STAT3结合。这一复合体进入细胞核后做了一件尤其显著的事:帮助弯曲并环绕DNA,使远端的调控区域与基因起始位点接触,物理上稳定了能提高特定基因表达的“增强子—启动子环路”。
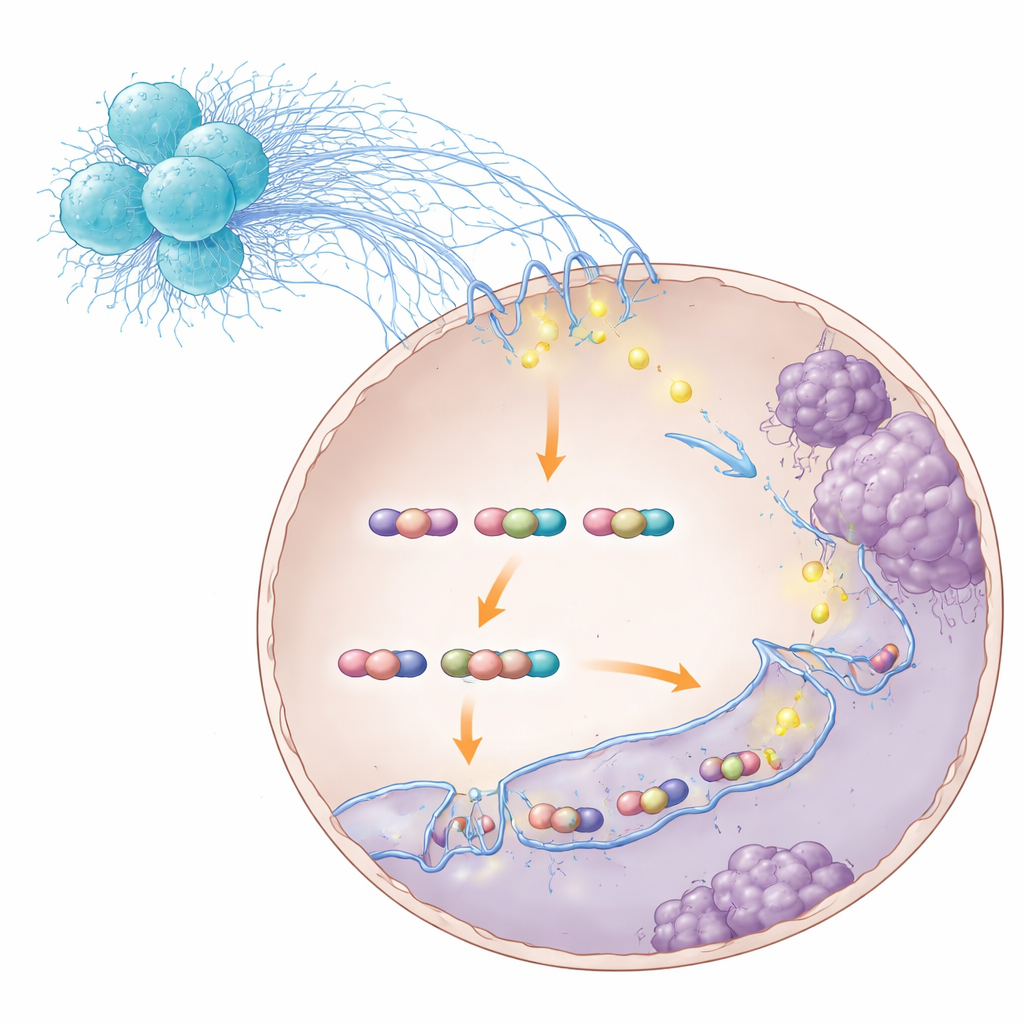
将癌细胞改接为转移模式
通过绘制基因组三维接触图谱,研究者发现STAT3–S100A8/9复合体促进了有利于细胞运动与侵袭的环路。其中一个显著基因是TNS1,它促使细胞放松附着并更容易迁移。破坏STAT3–S100A8/9复合体后,许多此类环路减弱或消失,TNS1表达下降,癌细胞的侵袭与在肝脏播种的能力受损。重要的是,这种干预并未完全阻止STAT3与DNA的相互作用——它特异性地破坏了那些使转移程序被超增幅的环路构象。在动物模型中,从中性粒细胞中的细菌感应分子RIPK2,到S100A8/9,再到STAT3本身,阻断链条中不同步骤均减少了肝转移并改善了生存。
切断菌与肿瘤之间的链条
给非专业读者的关键信息是:一种常见的肠道细菌能够通过先诱发免疫细胞释放DNA网,然后利用这些网触发一条以钙为动力的信号接力,从而重接癌细胞的基因开关,帮助结直肠癌扩散。与其依赖会损害有益微生物并削弱癌症免疫疗法的广谱抗生素,这项工作指出了更精确的药物靶点:如细菌感知器RIPK2、TRPC1–钙–S100A8/9级联以及将转移相关基因锁定在高表达状态的STAT3驱动DNA环路。在这些或多个环节上中断链条,或可为阻止结直肠癌从局部肠道问题变为致命肝脏疾病提供新的策略。
引用: Pan, B., Yao, Y., Zhang, Z. et al. Escherichia coli promotes colorectal cancer metastasis by maintaining enhancer-promoter loops through releasing neutrophil extracellular traps. Nat Commun 17, 2290 (2026). https://doi.org/10.1038/s41467-026-69005-y
关键词: 结直肠癌转移, 肠道微生物组, 中性粒细胞胞外网, STAT3 信号通路, 表观遗传基因调控