Clear Sky Science · zh
共价抑制剂设计赋予对KRAS G12C GDP 结合态和 GTP 结合态均有活性的能力
这对未来癌症治疗为何重要
由名为 KRAS 的基因突变驱动的癌症长期以来被视为最难治疗的类型之一。最近,能够抑制一种常见突变形式 KRAS G12C 的新药已进入临床并开始改变这一局面。本文探讨了一个更具雄心的设想:我们能否设计出同时阻断细胞内 KRAS G12C 两种主要工作模式的药物,这会不会使癌症治疗更快、更强或更持久?
在两个位置将分子开关关闭
KRAS 像一个微小的细胞生长信号开–关开关。它在“关”态(结合 GDP)和“开”态(结合 GTP)之间切换。KRAS G12C 突变使得该开关部分处于开启状态,从而推动肿瘤生长。现有获 FDA 批准的药物附着于“关”态并将其锁定;随着更多 KRAS 在该状态之间循环,突变蛋白的总体活性被耗尽。许多科学家认为,能够同时抓住 KRAS 两种状态的药物应当更有效,尤其是针对那些通过维持更多 KRAS 处于“开”态来产生适应的肿瘤。
设计一种新型的分子钩
作者着手构建这种双用途药物。他们聚焦于位于 KRAS 一处称为 Switch II 的灵活区域附近的小凹槽,这是现有药物结合的位置。研究者并非改变分子在凹槽中的结合紧密度,而是对与位于 12 位点的突变半胱氨酸形成永久化学键的“战斗头”部分进行重新设计。通过计算机建模并合成数十种变体,他们发现了一种由三部分组成的特殊战斗头,从略微不同的角度接近半胱氨酸。这一细微的改变为体积更大的 GTP 分子留出了足够空间,使得新化合物能够在 KRAS 携带 GDP 或 GTP 时都能发生结合。生化测试证实,先导化合物可在两种状态下破坏 KRAS 与关键信号伙伴 RAF 的相互作用。
观察蛋白如何重塑自己
为理解这些分子为何有效,团队解析了药物结合 KRAS 的高分辨率晶体结构。这些快照显示,新型战斗头在化学骨架的一个不同寻常位置发生反应,断裂了一个氟原子并在不同于典型针对半胱氨酸的抗癌药物的碳位上形成了共价键。这种改变的化学特性有助于药物即使在 GTP 存在时也能嵌入 Switch II 口袋。结构还显示,当抑制剂结合时,它推挤了一个微小的水分子并微妙地重排了另一个通常与下游信号蛋白接触的环状结构 Switch I。这种“变构”重塑将两个氨基酸拉近,形成紧密的盐桥,扭曲了表面,使得 RAF 无法再停靠并传递生长信号。
快速关闭,但长期效果并不更强
凭借这些结构学见解,研究者优化出了两种先导分子,它们高效且选择性地共价结合 KRAS G12C,同时在很大程度上避免与其他含半胱氨酸的蛋白发生反应。在癌细胞系中,这些双态抑制剂迅速阻断了被称为 MAPK 的关键信号转导通路,表现为 ERK 蛋白上的化学标记丧失和细胞生长的强烈抑制。它们比只针对失活状态的参照药更快使细胞内的 KRAS 失活。在小鼠肿瘤模型中,一种先导化合物表现出良好的口服利用度,能快速形成共价键并缩小或延缓肿瘤生长。然而,当团队在更长时间尺度上比较双态与失活态药物时,两类药物最终在 KRAS 关闭、通路抑制和肿瘤控制方面都达到了相似的水平。
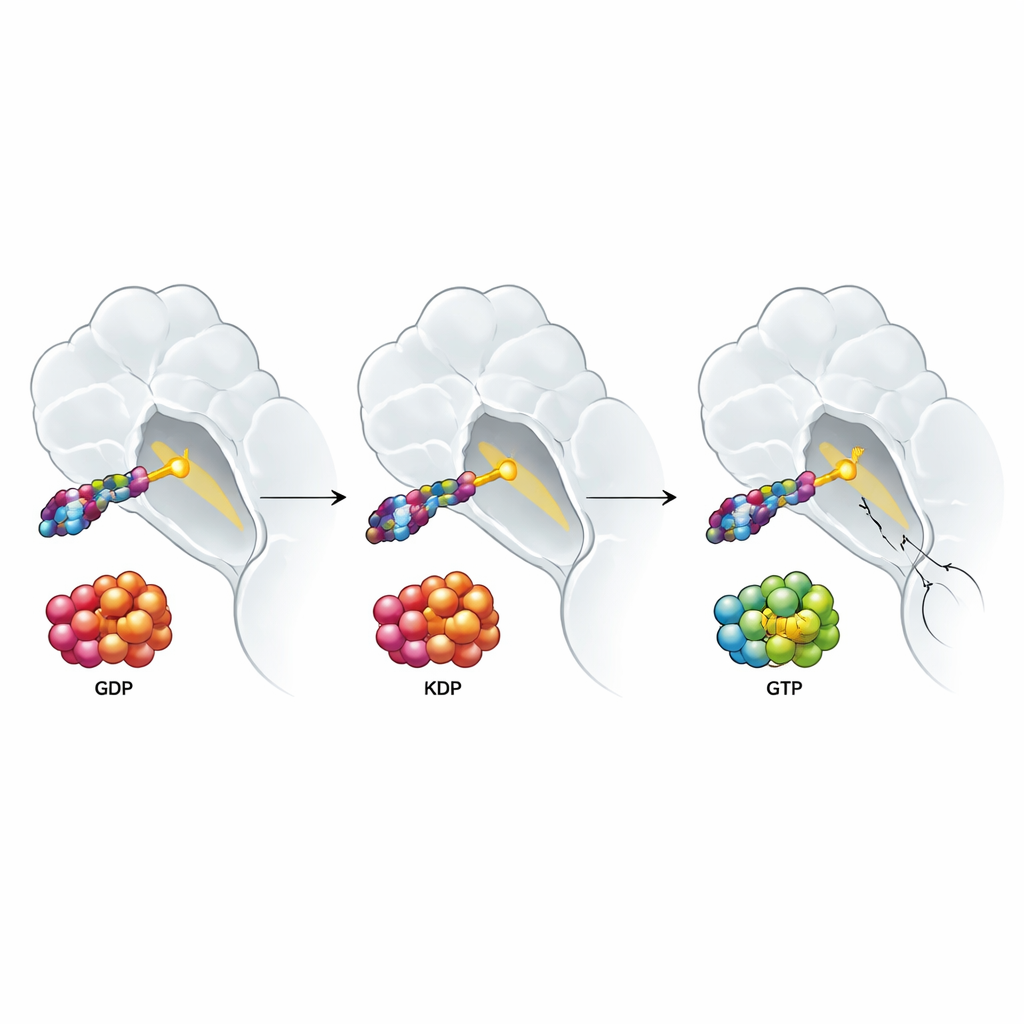
为何来自肿瘤周围的生长信号仍占上风
研究还探究了肿瘤微环境中的信号如何影响这些药物。像 EGF 和 HGF 这样的生长因子在许多肿瘤周围十分丰富,会推动 RAS 蛋白进入含 GTP 的活性状态,并已知会削弱靶向治疗的反应。人们可能期望能结合活性 KRAS G12C 的药物能够规避这一问题。但作者发现,在这些生长因子存在时,双态和失活态抑制剂的效力均下降。细致的实验指向了一个意想不到的元凶:正常的、未突变的 RAS 形式(H‑RAS 和 N‑RAS)的激活,它们可以旁路 KRAS G12C 并维持生长信号的传递。当研究者在一株肺癌细胞系中删除了 H‑RAS 和 N‑RAS 后,由生长因子驱动的耐药在各类 KRAS G12C 靶向药物中基本消失,而阻断通路下游某一步的药物本来受影响更小。
这对患者和药物开发意味着什么
总体而言,这项工作表明,从化学和结构上可以构建出在 KRAS 的开启态和关闭态都能抓住该蛋白的共价 KRAS G12C 药物,并且这些双态抑制剂能够比现有药物更快地关闭信号通路。然而,这种快速结合并未在前临床模型中转化为显著更好的肿瘤控制或解决由生长因子驱动的耐药问题。对患者而言,这提示仅仅增加对活性 KRAS 形式的抑制可能不足以带来实质改进;可能需要同时针对其他 RAS 家族成员或通路下游节点的组合策略。尽管如此,这里提出的新型战斗头和结构学蓝图扩展了靶向 KRAS 的工具箱,并将为未来几代精准癌症疗法提供参考。
引用: Condakes, M.L., Zhang, Z., Danahy, D.B. et al. Covalent inhibitor design confers activity against both GDP- and GTP-bound forms of KRAS G12C. Nat Commun 17, 2233 (2026). https://doi.org/10.1038/s41467-026-69003-0
关键词: KRAS G12C, 共价抑制剂, 双态抑制, MAPK 信号传导, 药物耐受性