Clear Sky Science · zh
微生物组诱导的 EI24 通过代谢调控改善稳态但削弱肺泡巨噬细胞功能
为什么这些微小的肺部守护者很重要
你每一次呼吸带入肺里的不仅有氧气,还有灰尘、微生物和其他入侵物。在这道前沿防线巡逻的是肺泡巨噬细胞——一种专门的免疫细胞,它们吞噬碎屑并帮助抵御感染和肿瘤。该研究揭示了日常微生物如何出人意料地“训练”这些细胞:由微生物组激活的一种分子 EI24,使肺部警卫更加稳定和低反应,但代价是削弱了它们对抗病毒和肿瘤的能力。理解这种权衡可为更安全、更有效的免疫疗法打开新思路。
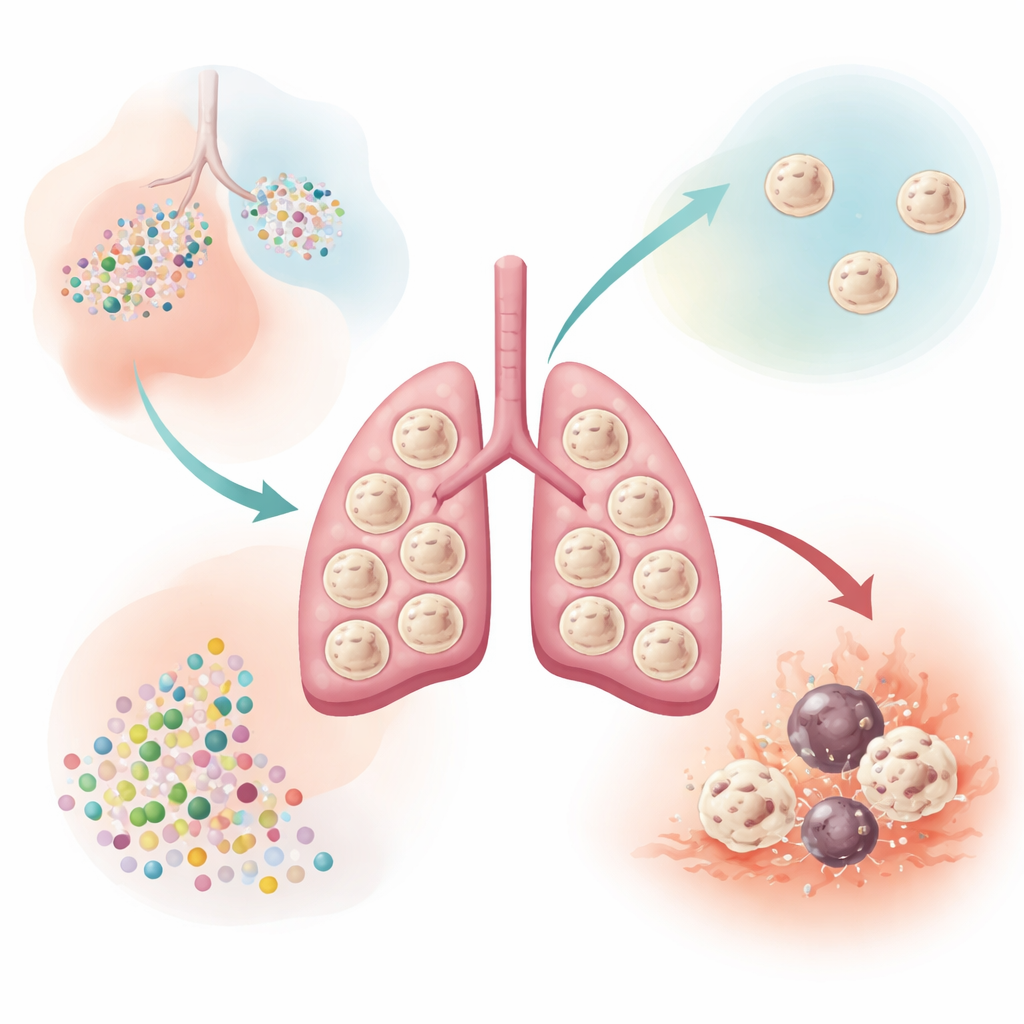
认识肺里的长期清洁工
肺泡巨噬细胞驻留在肺部进行气体交换的微小气囊中。它们在此处存活多年,自我更新,默默清除肺表面活性物质、死亡细胞和杂质,同时避免不必要的炎症以免损害脆弱组织。作者将注意力集中在一种名为 EI24 的蛋白上,之前它与细胞应激反应和细胞自噬/回收有关,但在肺部免疫中的作用尚不清楚。他们发现,在体内多种组织巨噬细胞中,肺泡巨噬细胞的 EI24 表达特别高,这暗示该蛋白可能对暴露在外的肺表面细胞生存至关重要。
肺部防御者的稳定性与战斗力之争
为了弄清 EI24 的实际作用,研究者培育了在巨噬细胞中特异性缺失该蛋白的老鼠。这些动物发育正常,肺中早期巨噬细胞前体数量也正常,但随着成熟,约一半的肺泡巨噬细胞消失。存活下来的细胞显示出明显的细胞死亡迹象,这种死亡由典型的凋亡酶 caspase-3 驱动。然而,剩下的这些细胞并不脆弱:在体外测试中它们表现出更“在岗”的特征,吞噬细菌能力更强,刺激时炎性分子产生更多。基因和染色质分析显示,数百个参与抗原呈递、细胞杀伤和炎症反应的基因被上调,而通常抑制活化的调控通路则被放松。
代谢升压带来的隐性代价
进一步挖掘发现,缺乏 EI24 的巨噬细胞其代谢被重编程。它们不再主要依赖平稳、节能的状态,而是同时提高了糖酵解(燃糖)和线粒体能量产生的水平。这些增强的能量通路为更强的炎性反应和更积极的吞噬微生物与肿瘤细胞提供燃料。但这种代谢过度驱动也增加了线粒体内的活性氧副产物,进而激活 caspase-3,促使细胞走向程序性死亡。阻断这些代谢通路或清除活性分子可减少过度炎症和细胞死亡的倾向,将细胞能量利用、杀伤能力与寿命联系在一起。
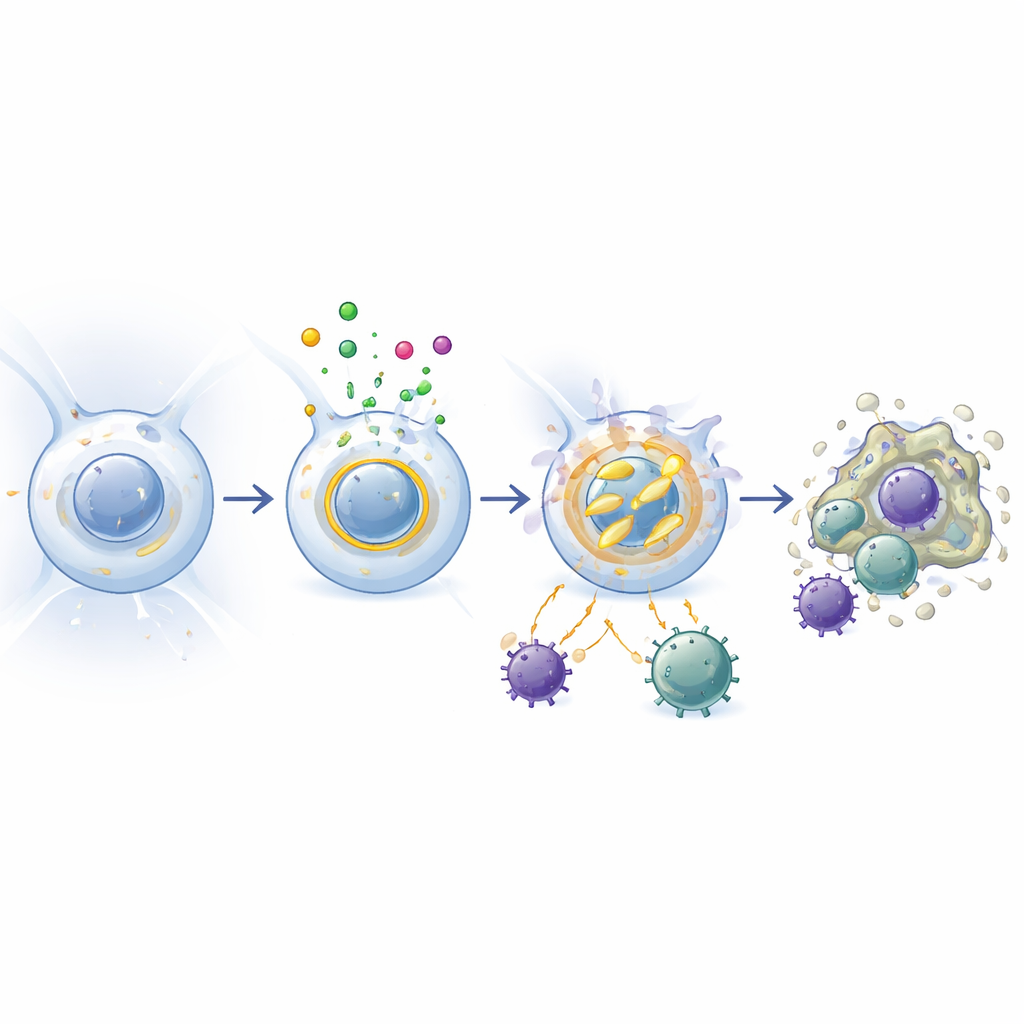
友好微生物如何设定这个刻度
肺不是一个密封室;它不断接触来自空气和肠道的无害或有益微生物。研究者将常规饲养的老鼠与无菌(无微生物)条件下长大的动物进行了比较。在无菌老鼠中,肺泡巨噬细胞产生的 EI24 远低于常规老鼠,而且在这些动物中移除 EI24 对细胞数量或行为影响不大。当这些无菌老鼠随后暴露于常规微生物时,其肺巨噬细胞的 EI24 水平上升。使用微生物感知通路的实验证明,通过 Toll 样受体 2 和 4(识别细菌成分的分子“门铃”)检测到的信号促成了这种增加。实际上,微生物组通过提高 EI24 水平,把肺泡巨噬细胞推向更稳定、更不反应的状态,帮助在本来可能持续触发免疫报警的环境中维持平静。
降低 EI24 以增强治疗效果
尽管这些小鼠的巨噬细胞数量减少,但在没有 EI24 的情况下它们对严重流感感染和实验性黑色素瘤肺转移的防护更好。它们更有效地清除病毒,在气道中产生更多抗病毒的干扰素,且其巨噬细胞更容易吞噬肿瘤细胞。重要的是,这些动物没有出现慢性肺损伤或肺功能丧失,表明在短期到中期内,有选择地去除 EI24 可在不明显损害肺健康的情况下增强防御。研究团队还展示了经工程改造、缺失 EI24 的骨髓来源巨噬细胞在移入其他小鼠时表现更佳,在限制肺部病毒感染和肿瘤扩散方面优于正常巨噬细胞。
这对未来治疗意味着什么
对普通读者而言,核心信息是:我们的定居微生物通过开启 EI24,帮助维持肺部免疫细胞的存活与平静——但这一安全机制也会削弱这些细胞对抗感染和癌症的能力。通过谨慎降低 EI24 水平,科学家可以将巨噬细胞推向更有活力、更具攻击性的状态,从而更有效地清除病毒和肿瘤细胞,同时在实验动物中仍能保持整体肺健康。这项工作表明,靶向 EI24 或其控制的代谢回路,未来有望使基于巨噬细胞的疗法成为对抗呼吸道感染和转移性癌症的更有力盟友。
引用: Huang, Y., Su, M., Zhang, Y. et al. Microbiota-induced EI24 improves homeostasis but impedes function of alveolar macrophages via metabolic regulation. Nat Commun 17, 2227 (2026). https://doi.org/10.1038/s41467-026-69000-3
关键词: 肺泡巨噬细胞, 肺部免疫, 微生物组, 巨噬细胞代谢, 癌症与抗病毒防御