Clear Sky Science · zh
受 HaloTag 技术启发的谷氨酸共价修饰
将蛋白“锚点”变为药物靶点
许多现代抗癌药通过结合细胞内的蛋白发挥作用。但一些关键蛋白缺乏容易被药物抓住的“把手”。这项研究借鉴了实验室常用工具 HaloTag 的巧妙化学思路,能够结合蛋白上通常难以触及的一个位点,这个位点参与控制与癌症相关的生长信号。该工作可能为更持久关闭驱动肿瘤通路的新药开辟路径。
为什么大多数共价药物都瞄准同一个位点
近年来,所谓的靶向共价药物已成为令人兴奋的一类药物。它们携带一个温和反应性的化学基团,可以与蛋白上的特定氨基酸形成永久键,将药物锁定。几乎所有这类药物都瞄准半胱氨酸,这是一种虽少见但高度反应性的氨基酸。相比之下,天冬氨酸和谷氨酸更常见,且常对蛋白的构象和功能至关重要,但它们的酸性“羧酸盐”基团在细胞的水溶环境中反应性要低得多。这使得选择性修饰它们非常困难,在本研究之前,仅有少数成功靶向谷氨酸或天冬氨酸的共价药物实例。
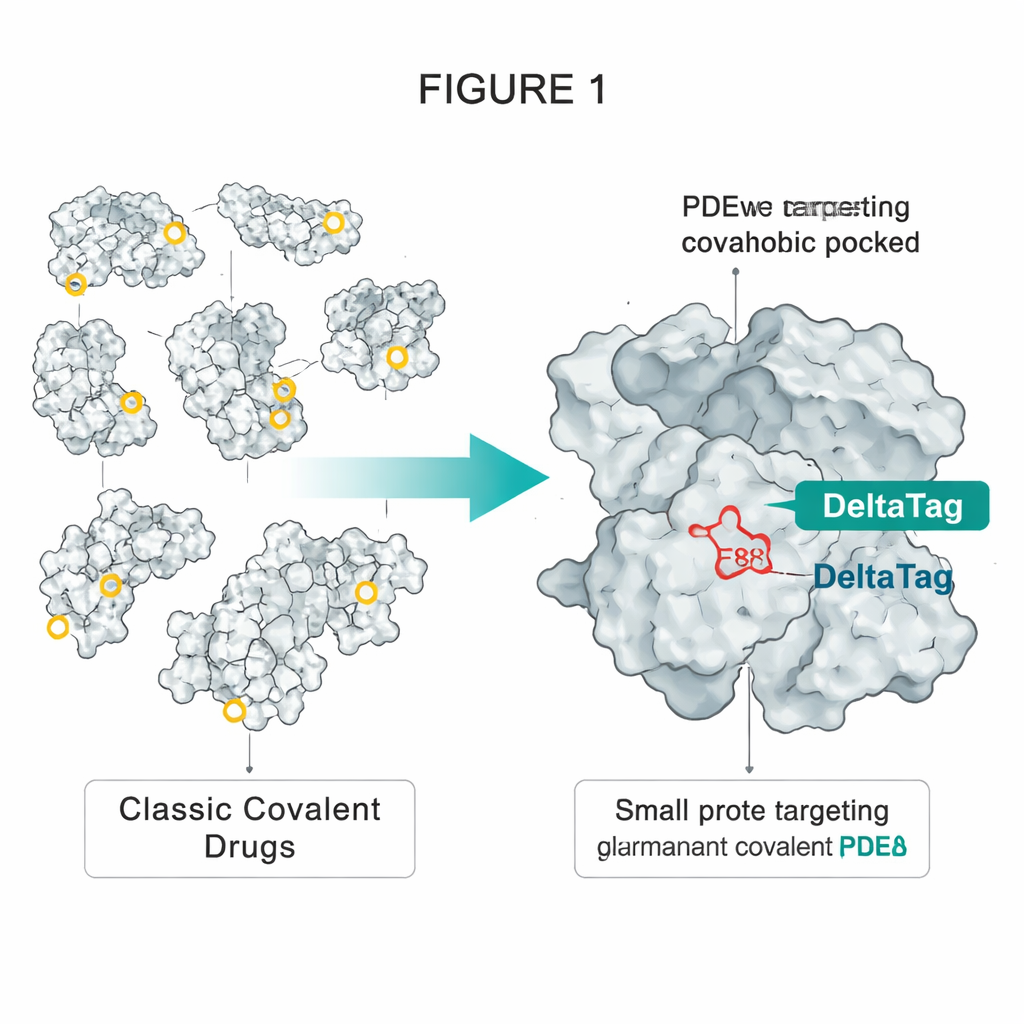
借用 HaloTag 技术中的一个把戏
作者们从 HaloTag 获得灵感:HaloTag 是一种广泛使用的工程化蛋白,可被永久标记荧光染料。在 HaloTag 中,一个特殊位置的天冬氨酸位于疏水口袋深处,会与染料上的简单氯代烷链发生反应,形成稳定的酯键。研究团队注意到另一个蛋白 PDEδ 具有类似的疏水口袋,口袋内含有一个可接近的谷氨酸,称为 E88。PDEδ 搬运带有脂质修饰的信号蛋白(如小 GTP 酶 Rheb),帮助它们到达细胞膜,在那里像 mTORC1 这样的促生长复合体被激活。先前对 PDEδ 的非共价抑制剂能阻断这种搬运,但其效应有限,因为另一个蛋白 Arl2 随时间会把抑制剂从口袋中挤出。
设计 DeltaTag 以锁定谷氨酸
为了解决这种“被踢出”的问题,研究者从已知的高亲和力 PDEδ 阻断剂出发,重新设计其一个侧链,使之携带类似 HaloTag 配体的卤代烷“武器”基团。通过多轮基于蛋白晶体结构的结构性调整,他们得到了一种名为 DeltaTag 的化合物。其关键特点是一个苯乙基溴基团被定位到位——当分子嵌入 PDEδ 的脂质口袋时,溴原子恰好对准并能与 E88 发生反应。生物物理测定和高分辨率 X 射线结构证实 DeltaTag 与该谷氨酸形成了特异性的共价酯键,而 PDEδ 上其他潜在更具反应性的氨基酸则保持未被触及。该化合物反应性足以有效标记蛋白,同时在水溶液和细胞主要含硫抗氧化剂谷胱甘肽存在下仍足够稳定,以避免广泛且不分青红皂白的损伤。
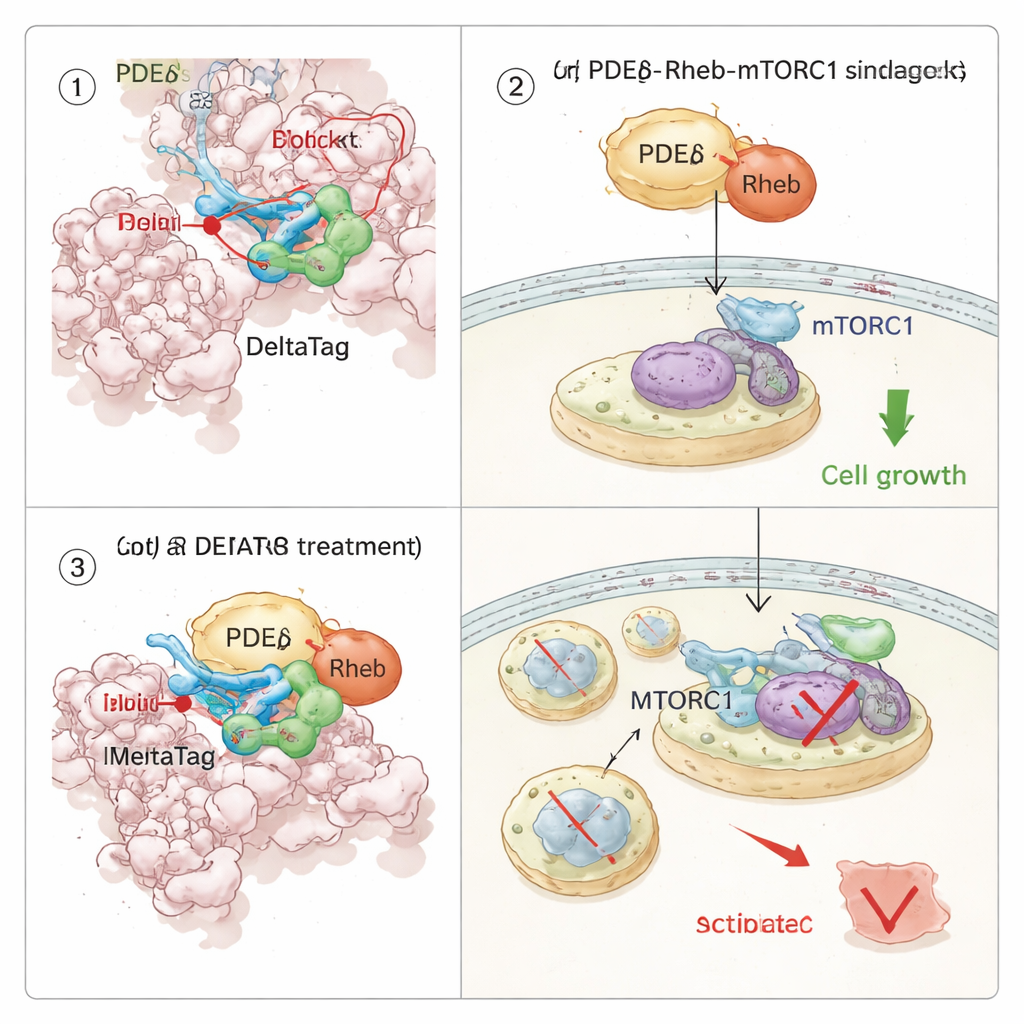
在癌细胞内重连生长通路
由于 PDEδ 搭载 Rheb,而 Rheb 又开启 mTORC1 生长通路,团队研究了对 PDEδ 的共价抑制如何在细胞信号中引发连锁反应。通过对数千种蛋白进行热稳定性谱分析,他们表明 DeltaTag 在细胞提取物中选择性结合 PDEδ,并扰动与 Rheb–mTOR 轴相关的蛋白。在活细胞成像实验中,DeltaTag 使 Rheb 从细胞内部弥散的分布重新定位到更聚集的内膜上,这与其正常搬运被破坏一致。整体磷蛋白组学和针对性的 Western 印迹显示,mTORC1 活性(通过核糖体蛋白 S6 的磷酸化来追踪)随时间下降,而相关通路中的补偿性信号上升。重要的是,在多株由突变 KRAS 驱动且依赖强 mTOR 信号的人类癌细胞系中,DeltaTag 比密切相关的可逆抑制剂更有效减缓细胞增殖,并且在缺乏 PDEδ 的细胞中其影响较弱,支持其主要作用为靶向作用。
为新型药物靶点打开一扇门
该工作表明,可以利用从 HaloTag 借用的相对简单的卤代烷化学,构建能够与蛋白疏水口袋内埋藏的单个谷氨酸形成永久且高度特异性键的小分子。在模型系统 PDEδ 中,这一共价连接比早期的可逆药物产生了对癌症相关生长通路的更持久阻断。更广泛地说,只要存在策略性位置的谷氨酸或天冬氨酸,同样的设计逻辑可应用于其他具有疏水空腔但缺乏通常“反应性”氨基酸的蛋白。经过进一步优化,像 DeltaTag 这样的靶向谷氨酸的共价抑制剂可能成为化学生物学的有用工具,并最终成为针对目前难以成药蛋白的新疗法的先导化合物。
引用: Zhang, R., Liu, J., Gasper, R. et al. Covalent modification of a glutamic acid inspired by HaloTag technology. Nat Commun 17, 1257 (2026). https://doi.org/10.1038/s41467-026-68999-9
关键词: 共价抑制剂, 靶向谷氨酸, PDEδ, mTOR 信号, 癌症药物设计