Clear Sky Science · zh
构建具有不同双层不对称性的膜内结构的合成细胞工程
为什么微小的合成囊泡重要
每个活细胞都被一层像智能柔性皮肤一样的膜包裹着。这层“皮”并不均匀:内外两侧,甚至表面不同区域的成分和形态可能大相径庭。这些差异有助于细胞传递信号、吸附蛋白质,甚至完成分裂。然而,要构建既简单又可控、同时能捕捉这种复杂性的模型膜一直非常困难。本研究提出了一种实用方法,可以制备细胞大小的“合成细胞”,其膜在两侧具有不对称性并在平面上被划分为不同区域——为更逼真的细胞模拟以及研究膜图案如何驱动芽生和分裂开辟了新途径。 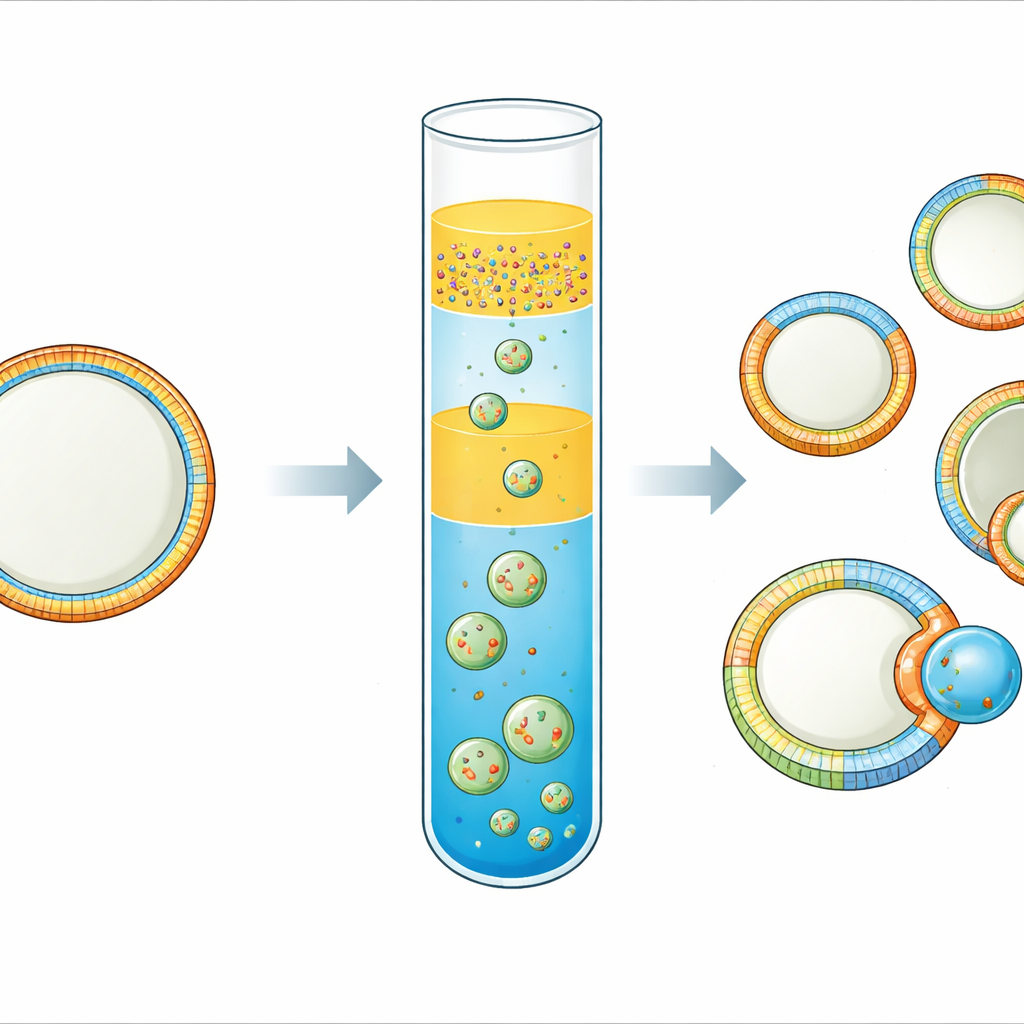
构建更好的细胞模拟器
真实细胞膜具有不对称性:内侧富含带负电荷的脂质以招募信号蛋白,而外侧则带有介导细胞间识别的不同脂质。许多实验室方法能制备巨囊泡——由类脂分子形成的空心球体——但它们的两层通常相同,且囊泡内部难以访问。其他能产生不对称性的策略往往需要复杂设备、特殊脂质,或使囊泡粘附在表面。作者着手创建悬浮、细胞尺寸的囊泡,既能高效包封生物分子,又能实现稳健、可调的类细胞不对称性。
三层配方用于不对称膜
团队改良了一种“倒置乳剂”技术:在该技术中,被脂质包覆的微小水滴穿过油—水界面形成囊泡。他们的关键创新是采用三层油体系。底层是含有将成为外叶层脂质的油。其上是没有脂质的薄隔离油层,顶部则是携带内叶层脂质的第二种油中的水滴乳剂。在短暂离心步骤中,水滴穿过隔离层和底层,带上第二层脂质包并闭合成囊泡。通过选择两种不同密度的油并加入隔离层,显著限制了脂质库之间的混合,使内外叶层保持各自不同的组成。
验证两侧保持不同
为验证两叶层是否真正不同,研究者使用了化学和蛋白质两类读出方法。在一组测试中,他们仅在其中一侧加入荧光标记脂质,然后将囊泡置于外部溶液中加入一种能淬灭荧光但不能穿膜的化学物质。当荧光脂质位于外侧时,信号几乎完全消失;而当其位于内侧时,信号几乎不变,说明大部分标记脂质保持在预期位置。在第二组实验中,他们在仅一侧放置能结合特定蛋白的脂质——例如用于链霉亲和素的生物素标记脂质或用于His标签绿色荧光蛋白的特殊头基。加入到相对隔间(内或外)的蛋白仅在其匹配的脂质位于相同一侧时结合,证实了强不对称性并保留了蛋白功能。
创建“筏”并观察膜的芽生
真实细胞膜还包含“筏”:富含胆固醇和鞘磷脂等特定脂质的小斑块,它们能聚集蛋白并影响形状。用倒置乳剂方法实现这种相分离一直具有挑战,因为胆固醇往往倾向于溶解在油相而不是加入膜中。通过在底层油中使用角鲨烯(squalene),该油对胆固醇的溶解力低于常用矿物油,作者能够可重复地形成膜在液有序相和液无序相共存的囊泡,类似于“筏”。随后他们将这种平面内图案与叶层不对称结合:一个区域在内叶携带能在内部结合链霉亲和素的配体,而另一个区域在外侧携带能结合霍乱毒素的糖脂。 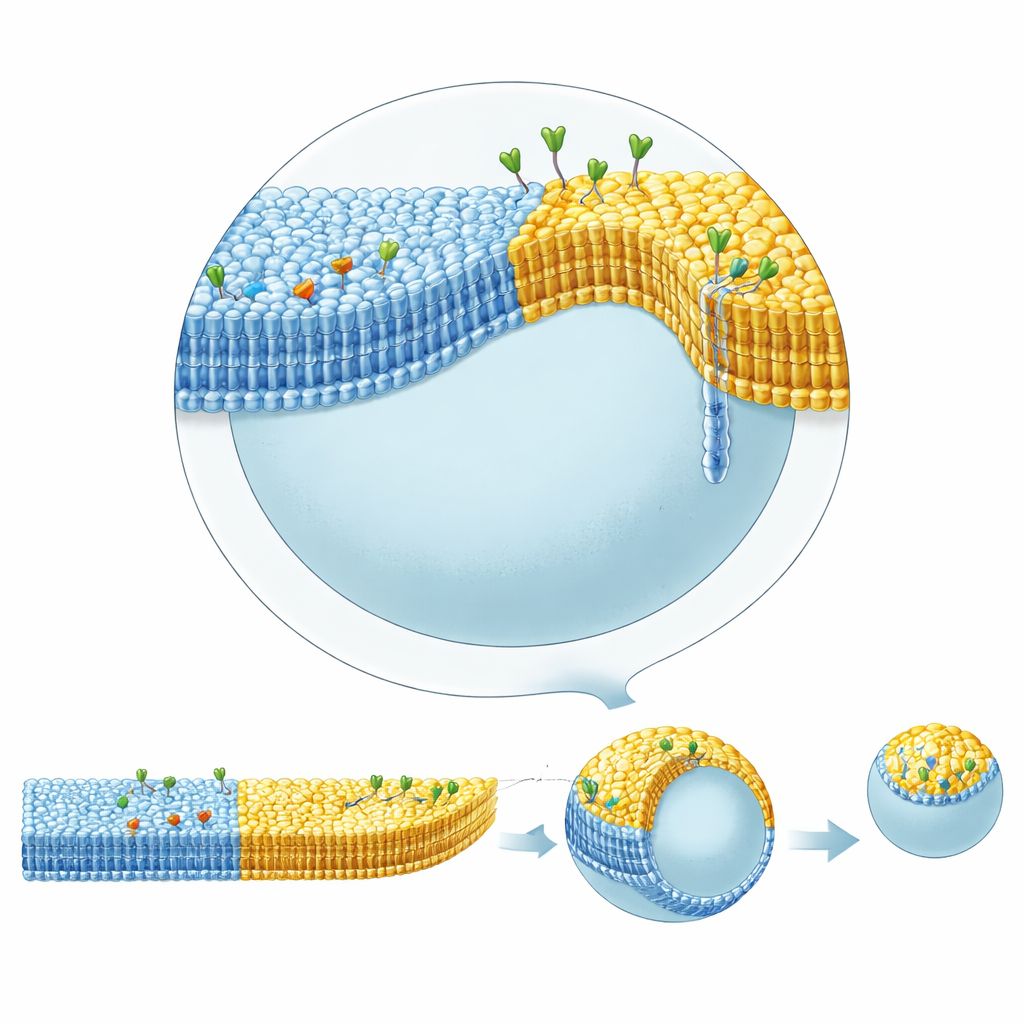
蛋白与图案如何驱动形状变化
这些复杂的囊泡表现出引人注目的形态动力学。当霍乱毒素在外侧结合到有序区的糖脂时,该区向外隆起形成一个由细颈相连的弯曲芽,在轻微渗透胁迫下可完全别离为子囊泡。此类芽生不需要像ATP这样的能量分子或专门的分裂机械;它纯粹源自脂质成分、区域边界和不对称蛋白结合的相互作用。通过增加内侧无序区上结合的链霉亲和素数量,团队可以抵消有序区的外向弯曲并逐步恢复更球形的形态。对囊泡轮廓的详细几何分析显示,膜的曲率在不同区域边界处发生突变,而芽生时闭合的细颈必须承受至少几十皮牛顿的力——量化了区域结构与蛋白拥挤如何在力学上塑造膜。
这对未来合成细胞意味着什么
通俗地说,作者开发出一种配方,能够制作柔软、细胞大小的囊泡,其“皮肤”在平面上有图案且具有双面不对称性,很大程度上模拟了真实细胞膜。由于该方法相对简单、兼容多种脂质,并允许蛋白和其它大分子被包封在内部,它为从底层构建更具生命特征的人工细胞铺平了道路。这类合成细胞可帮助科学家解析膜图案如何控制信号传导、物质运输和分裂,并可能最终作为智能药物载体,在体内按需改变形状或分裂释放负载。
引用: Yandrapalli, N., Seemann, T., Lipowsky, R. et al. Engineering synthetic cells with intramembrane domains possessing distinct bilayer asymmetries. Nat Commun 17, 2620 (2026). https://doi.org/10.1038/s41467-026-68997-x
关键词: 合成细胞, 脂质膜, 膜不对称性, 相分离, 膜芽生