Clear Sky Science · zh
用于疫苗分析的病毒糖蛋白纳米盘平台
将病毒蛋白变为可测量的靶点
现代疫苗越来越依赖精确设计的病毒表面蛋白变体。这些蛋白是防御性抗体的主要靶点,但在其天然的膜结合状态下极难研究。本文描述了一种新的实验室平台,将全长病毒表面蛋白置入称为纳米盘的微小扁平脂质颗粒中。该装置使科学家能够测量疫苗候选物与真实病毒的相似度、抗体如何与之结合,以及如何重新设计这些疫苗以提高防护效果。
为什么重现病毒表面很重要
许多最关键的病毒蛋白都锚定在脂质膜中,就像在真实病毒上一样。传统的实验方法通常去除膜段以便在溶液中更容易表达和纯化这些蛋白。但这种捷径会移除靠近膜的区域,而这些区域往往包含特别有价值的抗体靶位,包括 HIV 的膜近端外部区(MPER)。这些近膜区域在没有嵌入真实脂质环境时,其构象和行为可能发生变化,这意味着可溶性蛋白片段可能无法完整或准确地反映疫苗在体内的表现。
构建多功能纳米盘平台
研究者们创建了一个简化的五日工作流程,从人类细胞中获取全长病毒表面蛋白,保持其天然的跨膜片段完整,并将其重新插入受控的脂质盘中。他们先在细胞表面表达经工程化的 HIV 和埃博拉糖蛋白,然后用温和的去污剂提取并在纯化基质上捕获。蛋白仍附着时,研究者混入定义好的脂质和一种环带状的支架蛋白,该支架蛋白自组装成小型盘状膜。随着去污剂被去除,病毒蛋白沉入这些纳米盘中。所得制备物高度纯净,在冰箱中可稳定数月,且其糖基(糖链)涂层与天然病毒刺突上的糖基模式高度相似。 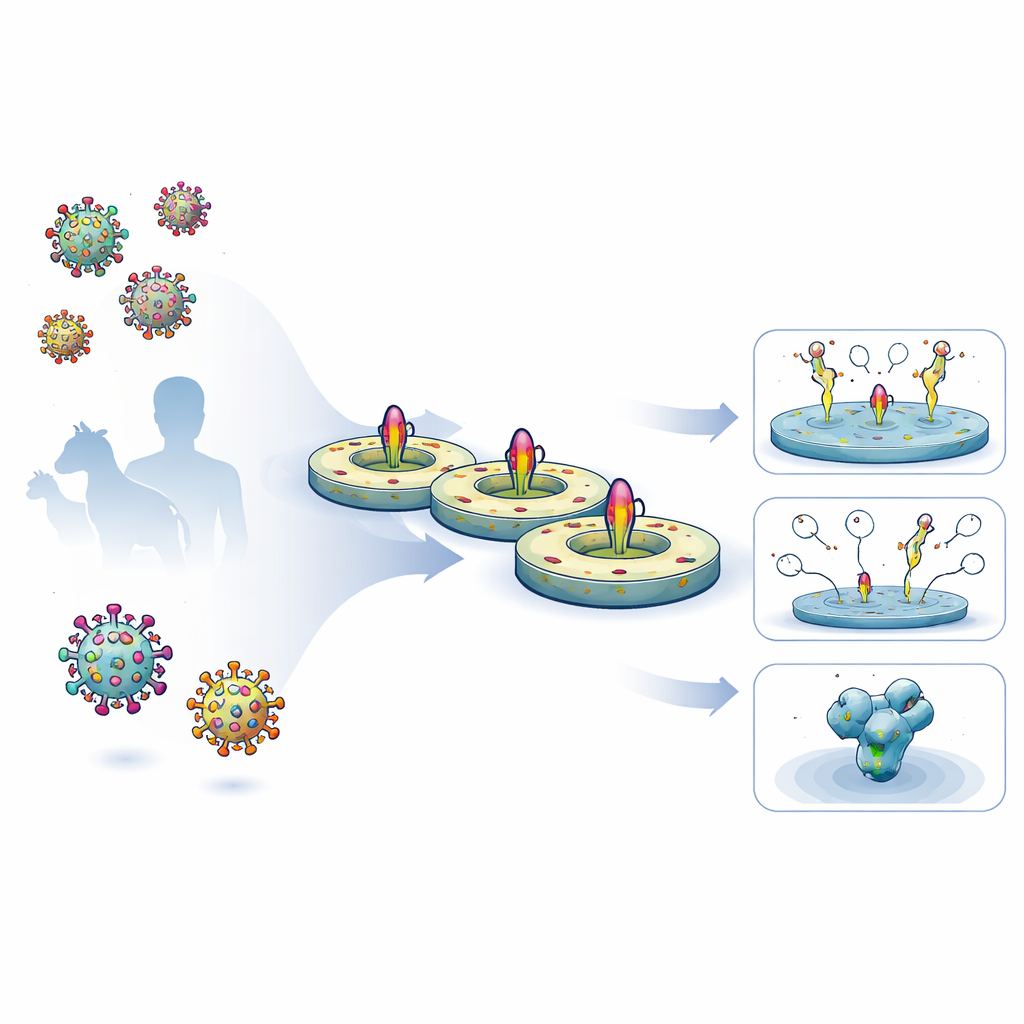
读取抗体结合与免疫反应
利用纳米盘嵌入的蛋白,团队在几种表面等离子体共振(SPR)配置下测试不同抗体的结合能力,这是一种实时追踪结合过程的技术。使用设计为暴露 MPER 区域的 HIV 纳米盘,他们显示一种强效的广谱中和抗体 10E8 与该工程构建体的结合亲和力约比早期设计高 70 倍,这主要因为解离速度显著变慢。破坏 MPER 区的对照突变完全消除了 10E8 的结合,证明该平台可以敏感地报告设计更改如何影响关键表位。这些纳米盘还可作为流式细胞术中的探针,帮助从免疫小鼠和猴子的样本中筛选识别全跨膜形式 HIV 蛋白的 B 细胞,包括标准可溶性探针所缺失的部分。 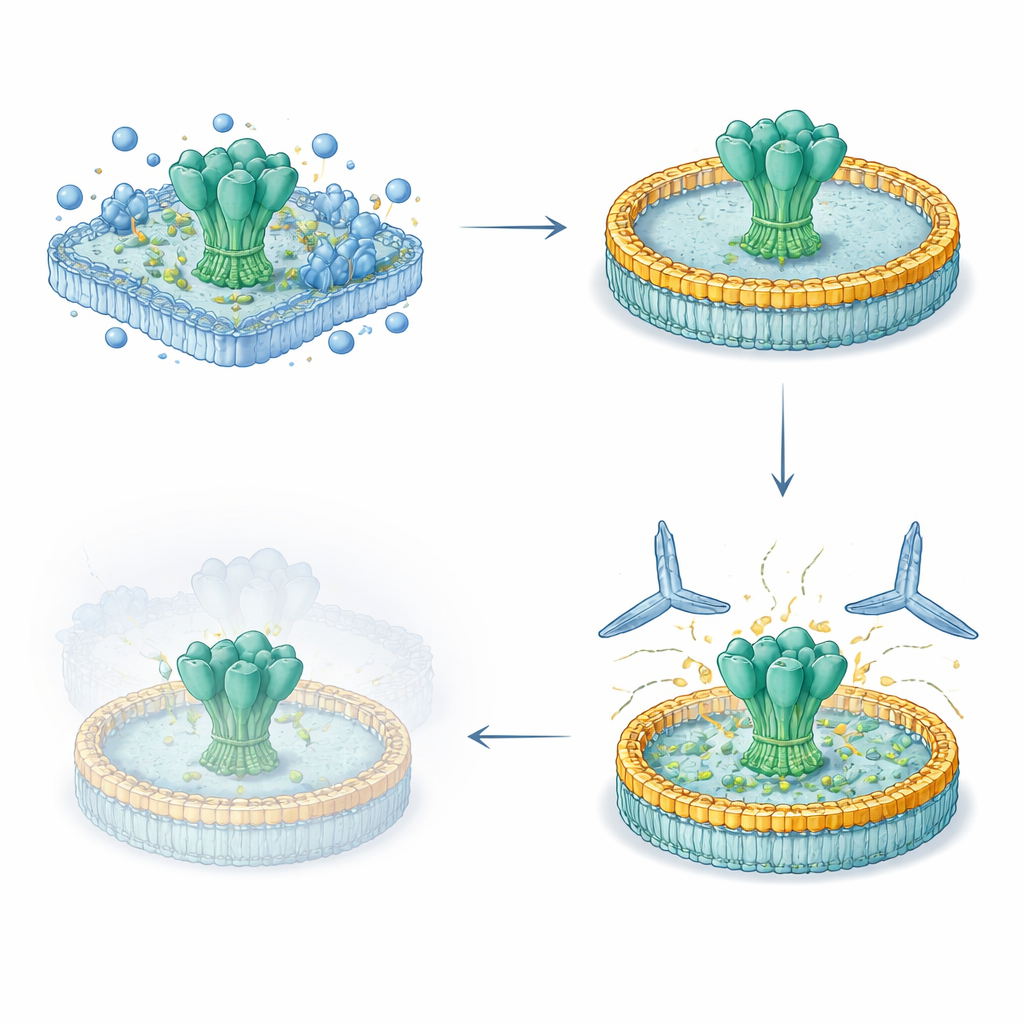
以原子级细节观察完整靶点
为了解抗体如何在其本生环境中识别 MPER,作者使用冷冻电子显微镜成像了与三种不同广谱中和抗体结合的工程化 HIV 纳米盘。他们获得了一个 3.5 埃分辨率的结构,显示抗体 10E8 与 MPER 片段互作,同时 HIV 刺突的其余部分仍锚定在脂质盘中。该结构揭示了 10E8 与 MPER 及邻近外部蛋白部分之间的连续接触网络,包括位于两个亚基连接处的一个深孔袋。将此结构与以前仅与短肽结合的 10E8 图像对比,团队表明膜环境和全长刺突允许额外接触和动态运动,这些在更简单的模型中不可见,并且病毒中的特定氨基酸强烈影响 10E8 的中和能力。
更聪明疫苗的广泛用途
从实用角度看,该纳米盘平台为疫苗设计者提供了一种用长期仅限于可溶性蛋白片段的强大分析工具评估跨膜疫苗候选物的方法。它适用于不同病毒,支持精细的结合测量,能够对疫苗诱导的 B 细胞进行精确分选和测序,并产出捕捉真实膜近表位的高分辨率结构。对普通读者来说,结论是科学家现在拥有一个更为逼真的病毒表面蛋白测试床,它能显示哪些疫苗设计在形态和功能上真正类似真实病毒,以及如何调整它们以诱导更强且更广的抗体反应。这将加速下一代疫苗的开发,不仅针对 HIV,也适用于许多其他包膜病毒。
引用: Rantalainen, K., Liguori, A., Ozorowski, G. et al. Virus glycoprotein nanodisc platform for vaccine analytics. Nat Commun 17, 2561 (2026). https://doi.org/10.1038/s41467-026-68985-1
关键词: 纳米盘, HIV 疫苗, 病毒糖蛋白, 广谱中和抗体, 冷冻电镜