Clear Sky Science · zh
哺乳动物全血中的自由基表位标记法
在真实血液中“看见”蛋白的工作状态
我们血液中的蛋白质在执行抗感染、运输铁、响应疾病等关键任务时不断改变构象。直到现在,大多数用于观察这些微小构象变化的工具仅能在简化的实验样品或分离细胞中使用。本研究首次表明,科学家可以直接在完整的哺乳动物血液中读取蛋白构象,从而开辟了一条在体内真实发生的疾病过程中实时观察蛋白变化的路径。
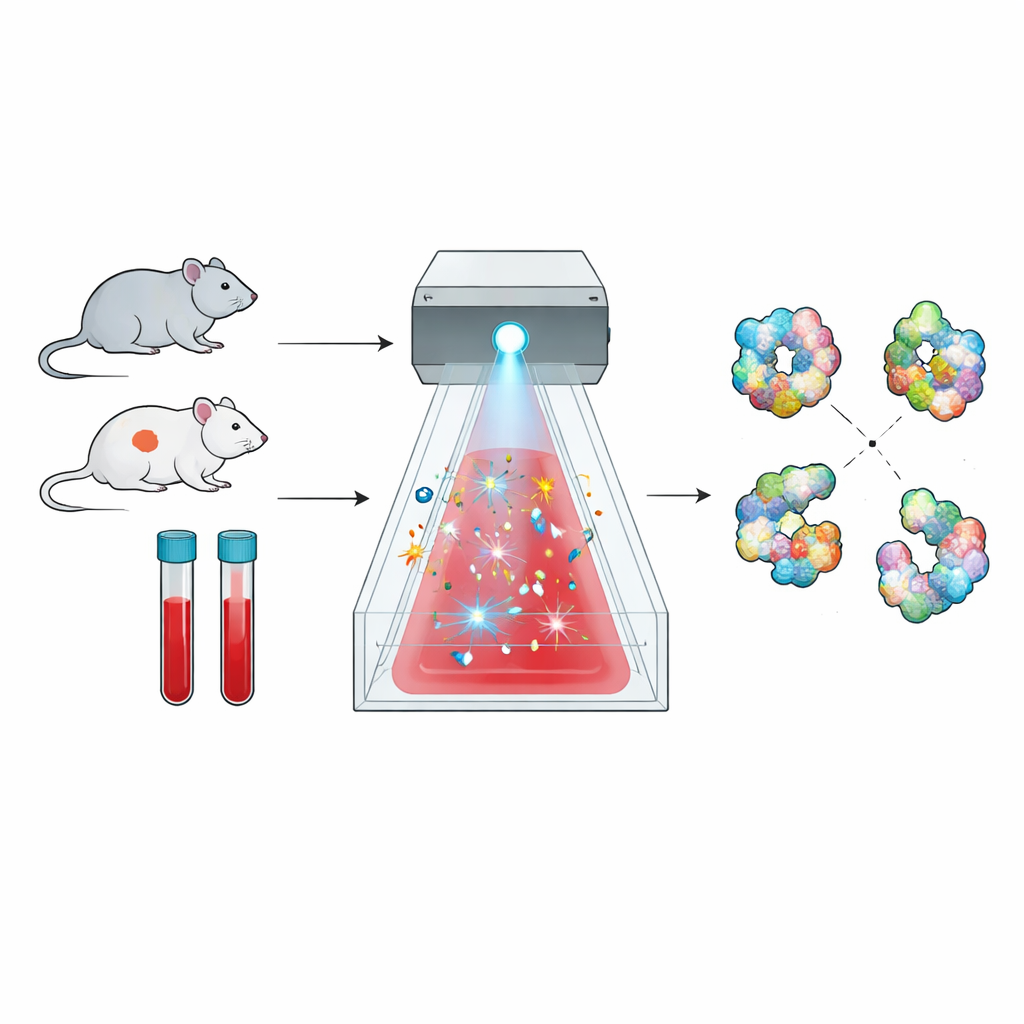
映射蛋白形状的一种新方法
蛋白质不是僵硬的珠子;它们折叠成复杂的三维形态,而这些形态决定了它们的功能。这里探讨的方法称为自由基蛋白表位标记(radical protein footprinting),利用了这一事实。短暂的高反应性分子爆发像化学“闪光灯”,只打击蛋白质暴露于溶液的部分。随后用质谱来计数这些化学打击发生的位置,从而产生每种蛋白表面的某种地图或“足迹”。健康与疾病状态之间足迹的差异可以揭示蛋白折叠或与伙伴分子相互作用的细微变化。
让该技术在全血中可行
将该方法直接应用于血液长期以来面临挑战。血液强烈吸收紫外光,且含有大量酶,如过氧化氢酶,能迅速破坏通常用于产生自由基的化学试剂,使其无法标记蛋白。研究人员通过改用过硫酸钠解决了这一问题,过硫酸盐在强宽光谱闪光下可裂解成高活性的硫酸根自由基。他们使用一种商业系统(称为 FOX)证明了过硫酸盐可以可靠地被激活,并且内置的剂量测定读数能够追踪产生了多少自由基,从而可以精确控制每个样品接受的“暴露”量。
在捕捉细节的同时保护细胞
因为该方法旨在研究接近自然状态的蛋白,所以必须保证血细胞本身不被破坏。对小鼠血液的测试表明,加入高浓度过硫酸盐仅引起红细胞形态的轻微且可逆变化,破裂率低于百分之二,与简单盐溶液相当。研究团队还开发了一种改进的“猝灭”混合物,能迅速清除剩余的活性物质,防止闪光后较慢的副反应造成伪伤害。这些改进使他们得以在保留细胞结构且保持背景噪音极低的条件下,对完整小鼠血液中的蛋白进行标记。
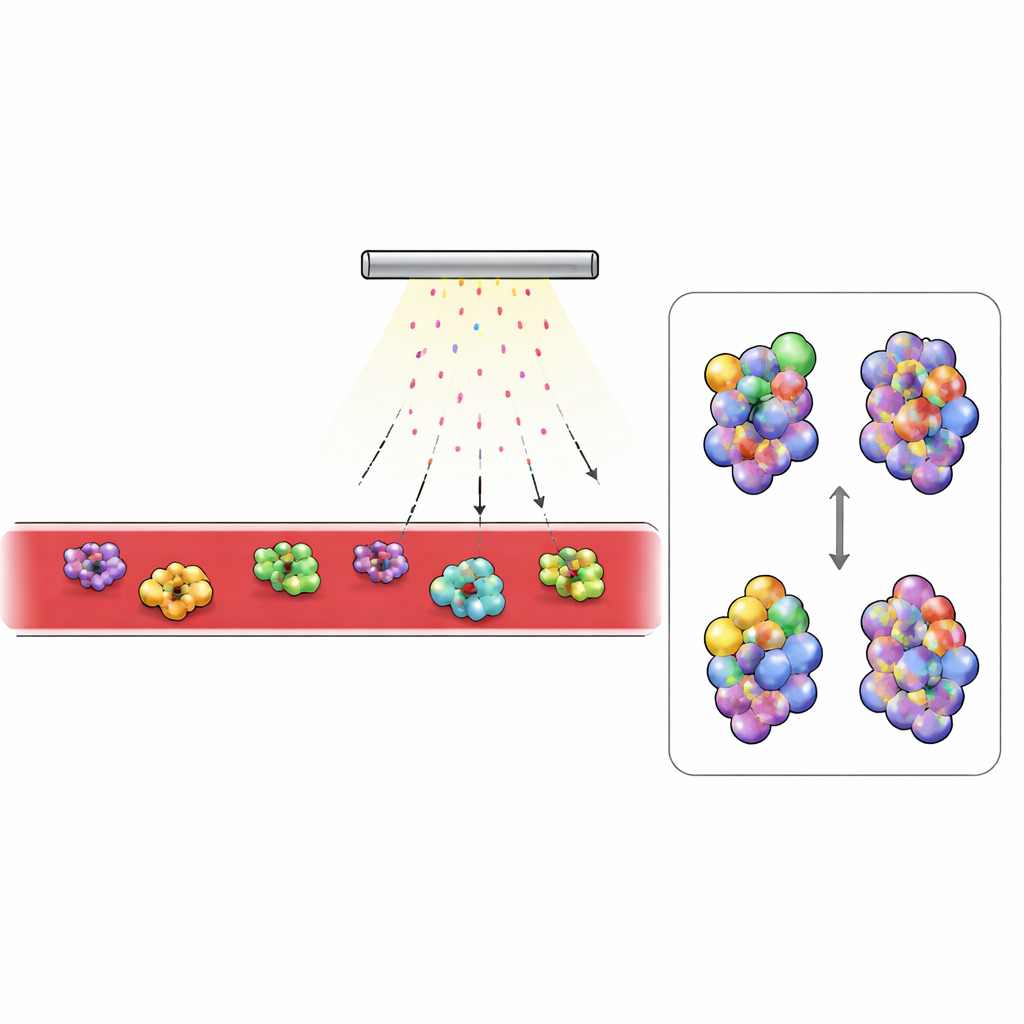
糖尿病血液中发生了什么变化
有了这个平台,研究人员比较了健康小鼠血液与一种常见 2 型糖尿病模型小鼠的血液。他们关注检测到的最丰富的蛋白,尤其是那些循环在细胞外的蛋白。细胞外蛋白的标记明显更强,这反映了过硫酸盐难以渗透入细胞内部。两种血液蛋白尤为突出:补体 C3(免疫系统的关键成分)和转铁蛋白(负责运输铁)。在糖尿病小鼠中,C3 在转换为活性形式时会被掩埋的区域标记较少,而通常被遮蔽的区域则更为暴露。这一模式与 C3 转化为其活性片段 C3b 时已知的结构变化相吻合,血液检测也证实糖尿病动物体内活化的 C3 显著增加。对于转铁蛋白,靠近结合铁位点的区域在糖尿病血液中更受保护,符合该蛋白携带更多铁的情况。独立测量显示糖尿病小鼠血清铁含量较高且转铁蛋白饱和度更大。
这对健康与医疗有什么意义
对非专业读者而言,核心信息是作者开发出了一种方法,能够在真实血液中同时“感知”许多蛋白的形状,并利用这些形状模式推断疾病如何改变体内化学状态。在这种 2 型糖尿病小鼠模型中,该方法揭示了补体信号过度活跃和转铁蛋白铁负荷增加——这是经典检测方法可能遗漏或只能间接观察到的变化。由于该方法适用于少量血样并使用标准化光源,未来它可能有助于识别疾病的早期结构性预警信号、追踪生物药在血液中的行为,并指导更有效治疗策略的设计。
引用: Zhao, M., Tobin, L., Misra, S.K. et al. Radical footprinting in mammalian whole blood. Nat Commun 17, 2470 (2026). https://doi.org/10.1038/s41467-026-68982-4
关键词: 结构蛋白质组学, 血液蛋白, 2 型糖尿病, 补体系统, 铁代谢