Clear Sky Science · zh
蛋白质C端变异影响蛋白稳态
蛋白尾端如何塑造健康
我们细胞中的每种蛋白质都以仅有几个构件组成的微小“尾巴”结尾。这些尾巴看似无足轻重,但本研究表明它们悄然决定了哪些蛋白会持续存在、哪些会被迅速清除。由于蛋白水平与癌症、遗传疾病以及细胞应对压力的能力密切相关,理解这些尾巴提供了评估疾病风险和设计未来疗法的新途径。
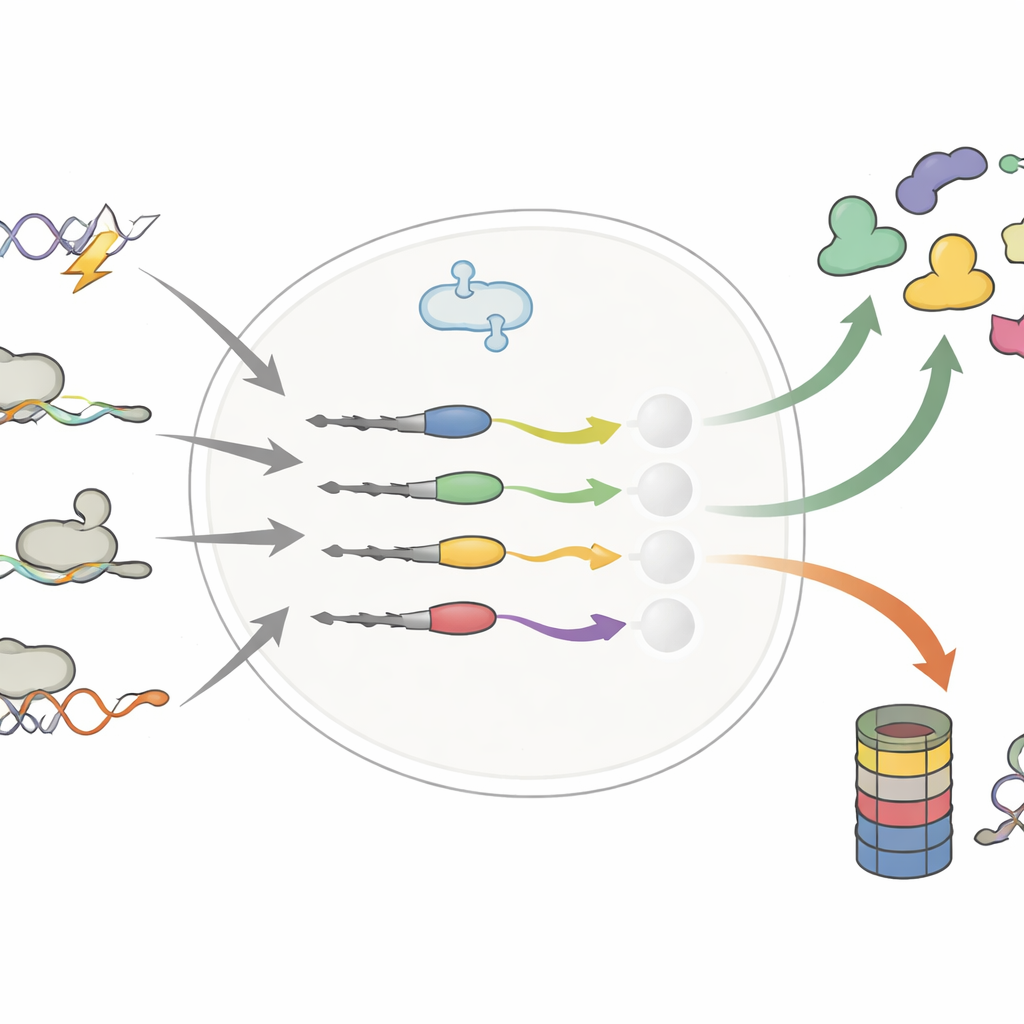
尾端的小变化,寿命的大转变
作者将注意力集中在蛋白质的末端——C末端——即便只有几处额外或替换的构件,也可能由于DNA突变、可变RNA剪接或核糖体越过常见的终止信号而出现。早期研究认为这些“错误”尾巴主要作为处置标签,把有缺陷的蛋白送去细胞的降解机器。通过系统性比较数千种正常与改变的尾巴,本研究推翻了这种简单看法。团队展示了改变的尾巴既能缩短也能延长蛋白的寿命,有时稳定致癌驱动蛋白,有时使抑癌蛋白更易失稳。
基因错误何时助益或有害于蛋白
尾巴改变的一个主要来源是无终止突变(nonstop mutation),即正常的终止信号被抹去,使核糖体继续翻译一段通常静默的RNA。研究者用一种双色报道系统测试了3000多种与疾病相关的nonstop变体,测量每种尾巴对模型蛋白的保护或削弱程度。总体而言,突变尾巴仍使蛋白比正常形式更不稳定,但有相当一部分情况相反:大约每十个nonstop突变中就有一个使蛋白稳定,而近三分之一使其不稳定。这些变化影响了知名的致癌蛋白和肿瘤抑制蛋白,意味着看似细微的突变实际上可以倾斜细胞生长与死亡的平衡。
来自剪接和读穿的内在多样性
并非所有尾端差异都是意外。我们的基因通过可变剪接和程序性终止密码子读穿常规地产生多种蛋白版本。通过挖掘人类基因目录,作者发现近三分之二的基因产生具有不止一种尾端设计的蛋白,且许多仅在最后几处构件上有所不同。对选定实例的测试表明,这些几乎相同的版本常常具有显著不同的半衰期。有些由读穿生成的尾巴使蛋白更稳定,另一些则使其更易降解。这表明细胞有意将尾端变异作为微调旋钮,在不同组织或条件下调整特定蛋白形式的存在时间。
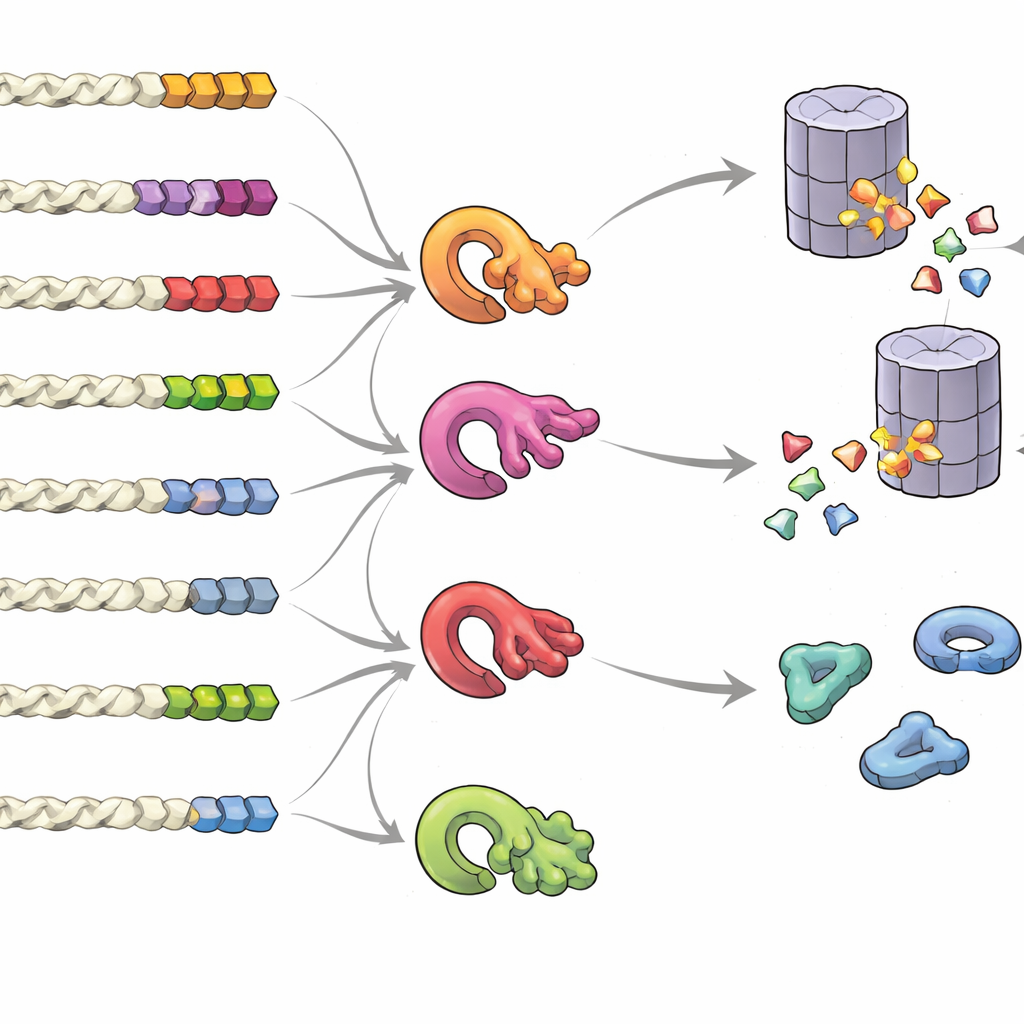
是什么让尾巴成为“留下我”或“丢掉我”的信号
为了解尾巴的哪些特征左右蛋白命运,团队构建了随机尾巴库并进行了批量测量。他们发现并非单一固定的“基序”起作用,而是整体组成、位置以及某些残基的聚集方式才重要。富含小型或疏水成分的尾巴,或含较少见的半胱氨酸和色氨酸的尾巴,倾向于引发降解,尤其当这些残基成簇出现时。相反,富含酸性残基的尾巴偏向稳定。跨物种比较显示,正常蛋白尾端明显受到进化压力以避免高风险的模式,而易出错的读穿或移码尾端则偏向不稳定的组成。研究组还发现,多种质量控制酶——不同的泛素连接酶——专门识别各类疏水尾端模式,形成一个复杂的网络来决定哪些蛋白被销毁。
这对医学与生物技术为何重要
这项工作将蛋白尾端从被动的终点重新定义为蛋白丰度的主动调节因子。对普通读者而言,这意味着许多疾病可能不仅源于蛋白本身的损坏,还可能来自蛋白停留时间的细微变化,这些变化由其末端的小差别驱动。研究也提醒人们,旨在促进终止信号读穿的疗法(用于治疗某些遗传病)可能无意中改变许多正常蛋白的寿命。与此同时,研究结果提出了强有力的新策略:通过设计尾端序列或促使细胞偏好特定剪接形式或读穿事件,科学家或许可以在未来以相当精确的方式调节蛋白水平。
引用: Chu, CY., Hsu, SY., Yeh, CW. et al. Protein C-terminal variations impact proteostasis. Nat Commun 17, 2288 (2026). https://doi.org/10.1038/s41467-026-68979-z
关键词: 蛋白质稳定性, C端尾巴, 蛋白降解, 基因突变, 蛋白稳态