Clear Sky Science · zh
VSIG10L 是食管稳态与遗传性巴雷特食管易感性的主要决定因子
这对有胸口灼热感的人为何重要
慢性胸口灼热(烧心)很常见,但只有少数人会发展为巴雷特食管——一种可能导致食管癌的病变。本研究提出了一个简单但重要的问题:为什么有些家族比其他家族更容易患巴雷特食管?通过追踪单个基因并观察其如何在人体和小鼠中塑造食管上皮,研究人员揭示了一个连接遗传风险、反流损伤与机体维持食管健康能力之间的缺失环节。
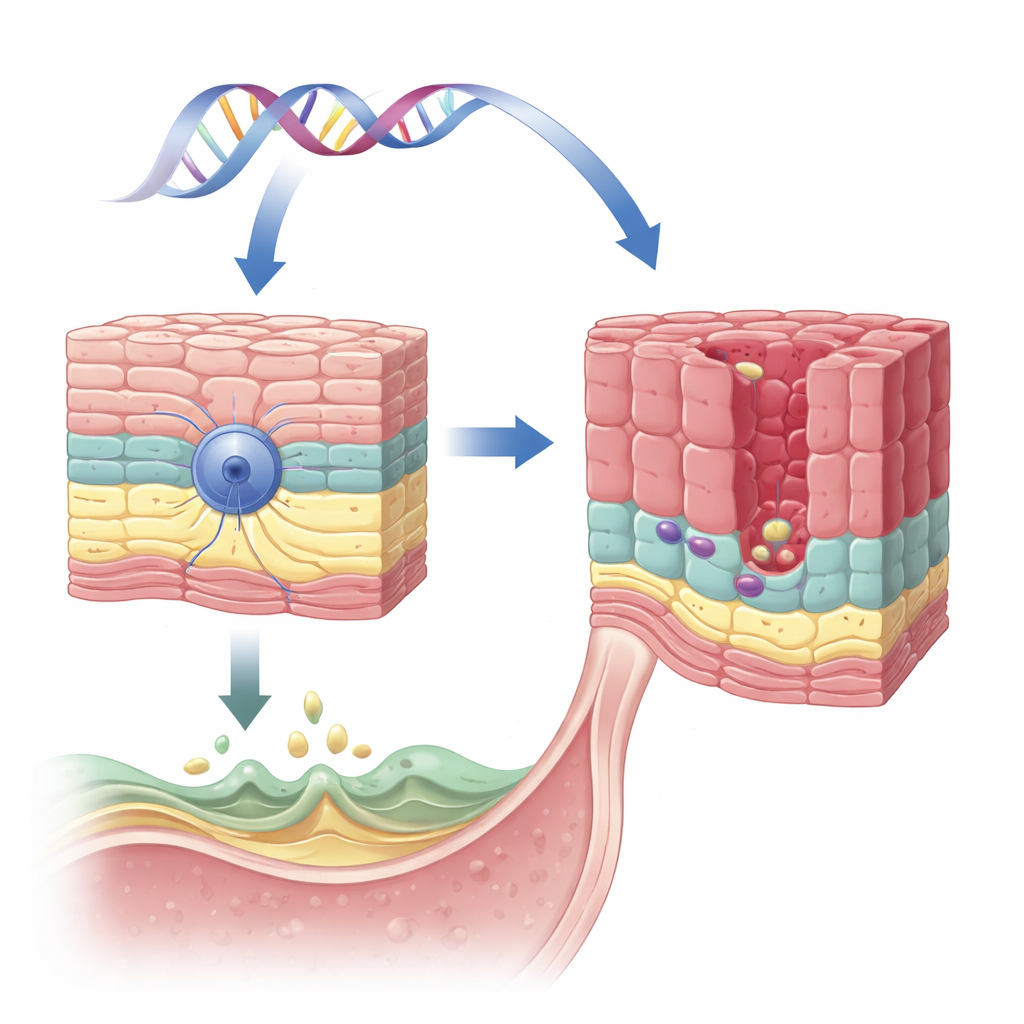
食管上皮中的保护性基因
研究小组将注意力集中在名为 VSIG10L 的基因上,该基因此前在一个多发巴雷特食管及相关癌症的大型家族中被标识。VSIG10L 在食管扁平(鳞状)上皮的上层细胞中有活性,但在更深、更具干细胞样特征的基底层细胞中不表达。研究者在人体、猪和小鼠组织以及人体食管细胞的三维培养物中使用灵敏的 RNA 检测方法,显示 VSIG10L 始终仅在基底层之上的“成熟化”细胞中开启。这种表达模式表明 VSIG10L 有助于鳞状细胞完成最终的成熟步骤并形成稳定的屏障。
削弱屏障的遗传改变
通过对来自 302 个巴雷特及食管癌家系的 684 名个体进行 VSIG10L 基因测序,研究者发现了若干罕见且具有破坏性的变异。为测试这些变异的功能,他们从携带其中一种突变的患者处构建了人类干细胞衍生的食管类器官。与来自健康供者的类器官相比,携带突变的类器官无法构建正常的层状鳞状结构。相反,它们常常形成异常的、腺样的细胞团,停留在基底、未成熟状态,表现为 p63 蛋白的高表达。这种正常分层和成熟的扭曲,与被认为在患者中先于巴雷特食管发生的早期步骤相呼应。
重现人类疾病的小鼠模型
为超越细胞培养体系,研究团队创建了携带人类家族性 VSIG10L 突变精确拷贝或完全缺失该基因的小鼠。在健康小鼠中,对应的 Vsig10l 基因同样仅在上位鳞状细胞中表达。通过电子显微镜观察,突变小鼠在这些层次中显示出明显的桥粒(将相邻细胞固定在一起的微小“铆钉”)丧失。在来自类似下食管结构的小鼠鳞状贲门(forestomach)的基因表达图谱中,显示出结构与分化程序的广泛紊乱。当这些小鼠饲以含有脱氧胆酸的饮食以模拟慢性反流时,70–100% 的 Vsig10l 突变小鼠在鳞柱交界处出现大量富含黏液的巴雷特样病变,而野生型小鼠仅出现小而有限的病灶。
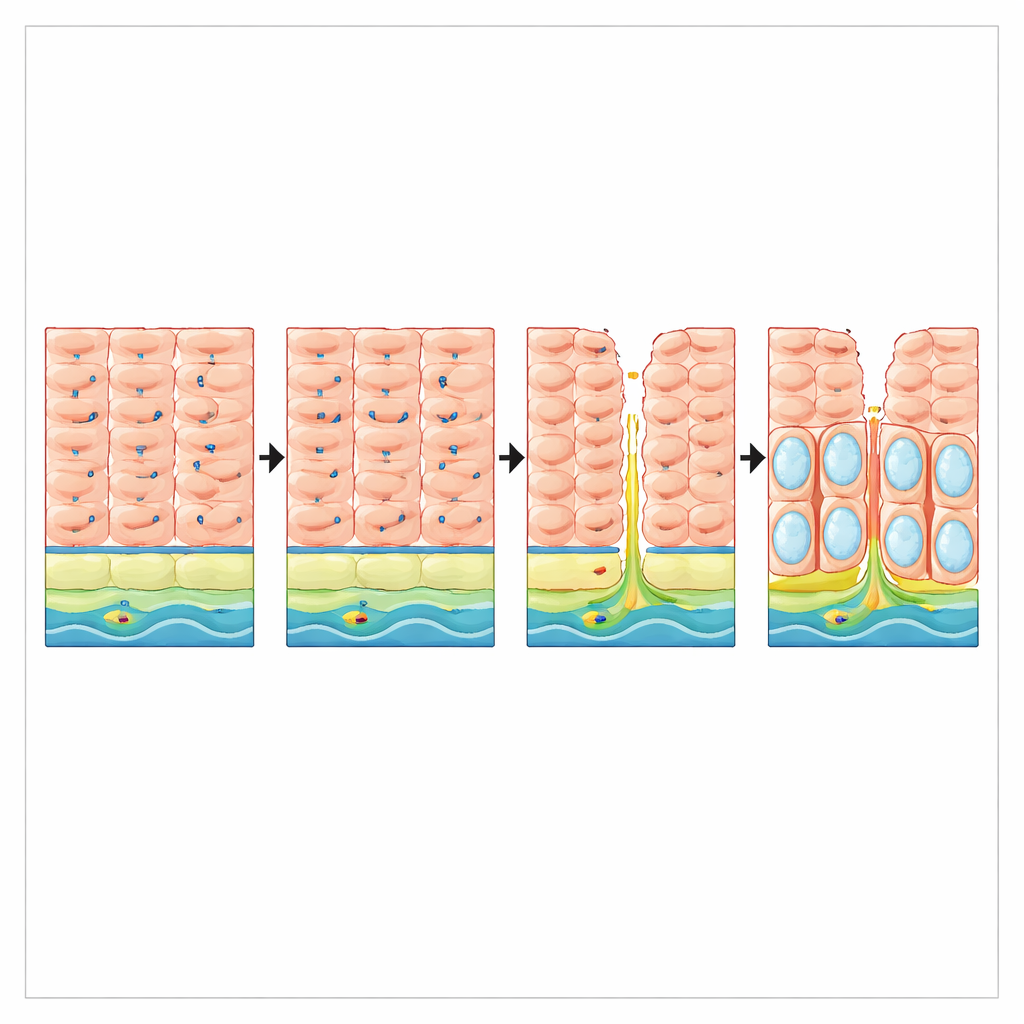
患者中的反流损伤与保护丧失
研究人员随后探究反流本身是否会扰乱人类的 VSIG10L 表达。在来自长期胃食管反流病但尚未出现巴雷特食管患者的活检样本中,VSIG10L 的 RNA 水平比无反流者约低三倍,即使基本的鳞状细胞标志物 TP63 未见变化。在组织切片中,健康食管黏膜显示出一条清晰的 VSIG10L 阳性细胞带,位于基底层之上。相反,受反流损伤的黏膜表现为基底样、p63 丰富细胞的扩展以及 VSIG10L 阳性分化梯度的几近完全丧失。这些发现表明,慢性反流不仅侵蚀了黏膜的物理完整性,也破坏了维持其有序更新的基因程序。
将各环节拼接起来
综上所述,这项工作支持一个简单模型:VSIG10L 是食管鳞状屏障的重要守护因子。该基因的遗传缺陷或因慢性反流而获得性抑制,会导致上皮成熟不良、细胞间连接减少以及表面屏障变得更易渗漏。在这种易损状态下,反复暴露于酸和胆汁促使异常的腺样愈合代替原有鳞状上皮的修复,从而为巴雷特食管的发生铺路。对于患者和家族而言,这项研究指向未来可筛查高风险个体的基因检测,以及旨在维持或恢复 VSIG10L 功能的新疗法,最终目标是预防巴雷特食管及其向癌变的进展。
引用: Ravillah, D., Singh, S., Katabathula, R.M. et al. VSIG10L is a major determinant of esophageal homeostasis and inherited predisposition to Barrett’s esophagus. Nat Commun 17, 2167 (2026). https://doi.org/10.1038/s41467-026-68975-3
关键词: 巴雷特食管, 胃食管逆流, 遗传易感性, 上皮稳态, 食管癌风险