Clear Sky Science · zh
光诱导的极性失配将异喹啉转化为萘的反应
为药物开辟新的光明道路
许多现代药物由扁平的碳环骨架构成。将一种环核替换为另一种可以显著改变药物在体内的行为,但通常需要冗长且昂贵的合成步骤。本研究提出了一种由光驱动的捷径:直接将一种常见的含氮环——异喹啉,转化为一种密切相关的纯碳环——萘。该方法在温和条件下进行,能够容忍多种官能团,并可在药物分子合成的后期应用,为更快获得改良药物开辟了途径。
为何替换环核至关重要
在药物发现中,化学家合成并测试大量相关分子以调节效力、选择性与稳定性等性质。即便仅在中心环中替换一个原子,也可能显著改变化合物与生物靶标的匹配方式或体内的代谢寿命。异喹啉和萘是此类可互换“相似核”的经典例子:它们在尺寸和形状上相近,但前者含有氮原子,后者则仅由碳构成。传统上,要把一种核改为另一种通常需要从头重建分子,通过繁琐的多个步骤。若能实现二者之间的直接一步转化,化学家就能在不重头开始的情况下将现有分子回收为新的变体。
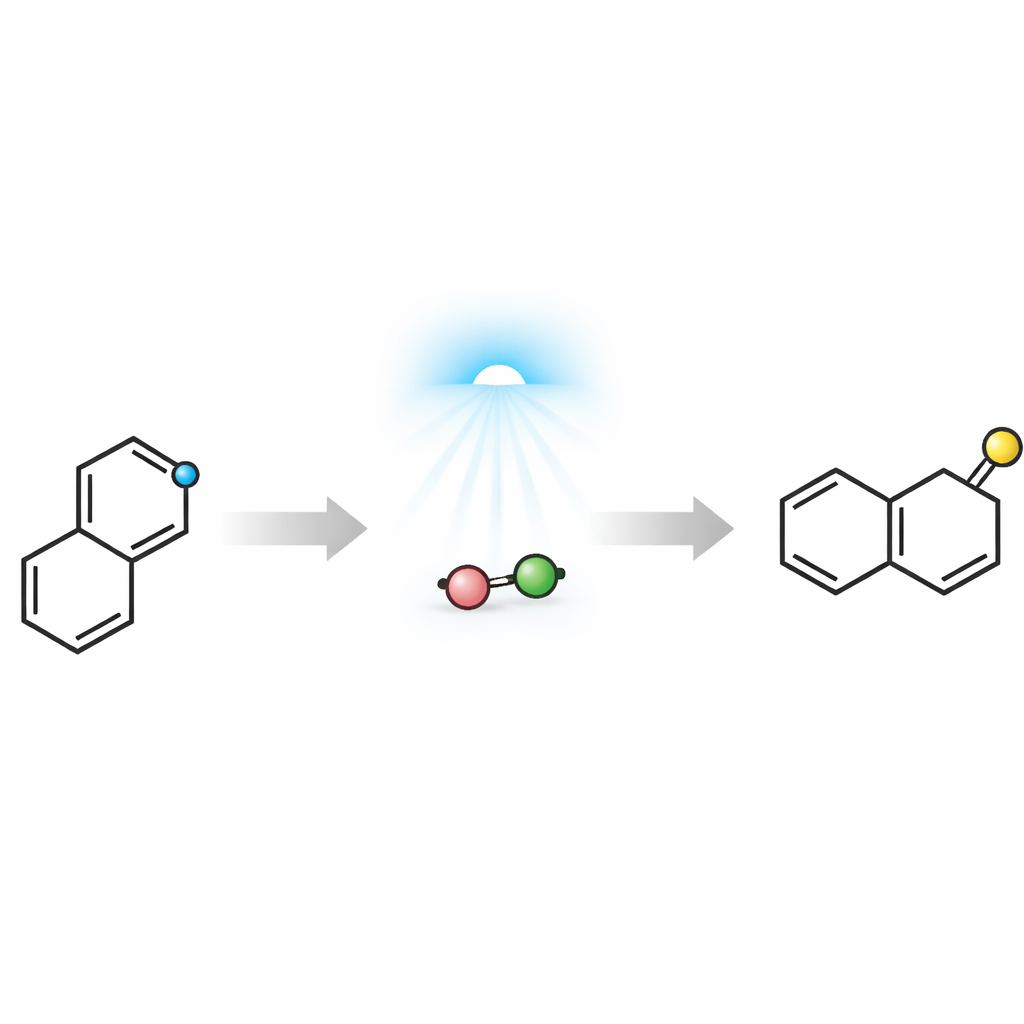
将电子失配变为优势
挑战在于,异喹啉和用于构建萘的炔烃都相对缺电子,因此在关键的成键步骤(即一种六元环构建反应)中通常会相互排斥。作者通过利用可见光和一种简单的无机碱克服了这种“极性失配”。当异喹啉被制成阳离子盐并与碳酸根配对时,两者形成可吸收蓝光的弱配合物。计算研究指导了设计,显示光激发将电子从碳酸根传递到异喹啉阳离子环,暂时将其转变为富电子自由基。在这一活化态下,异喹啉能够逐步加成到缺电子的炔烃上,形成新的环系,最终重排为萘并甩出含氮片段。
在实验室中探究该反应
在实验上,该转化操作简单:将异喹啉阳离子盐、炔烃和碳酸钠在乙醇中搅拌,并在蓝色LED照射下进行,无需额外的光催化剂。团队优化了反应条件,表明碳酸根不仅作为碱是关键,还是电子供体;溴化物离子则有助于促进反应。自由基陷阱剂会中止反应并捕获中间加成物,支持计算提出的自由基途径。光谱学实验确认,异喹啉阳离子–碳酸根对是真正的光吸收复合物,而更换对离子或碱会以其参与电子转移能力一致的方式改变产率。
从模型体系到类药物分子
在优化条件后,作者展示了该方法的广泛适用性。许多不同取代的炔烃都能参与反应,包括携带敏感基团(如碘、额外双键)或来源于天然产物及现有药物的片段。多种异喹啉阳离子盐也能成功反应,即便是拥挤或含杂环的底物,也能生成多取代的萘,这类产物通过传统路线难以获得。该方法甚至能在单步后期操作中将复杂的生物活性分子(如PRMT3抑制剂SGC707和血管痉挛药物法舒地尔)改造成相应的萘类似物。新生成的产物带有酯基,既可作为潜在的蛋白结合位点,也为后续合成提供了多功能入口。
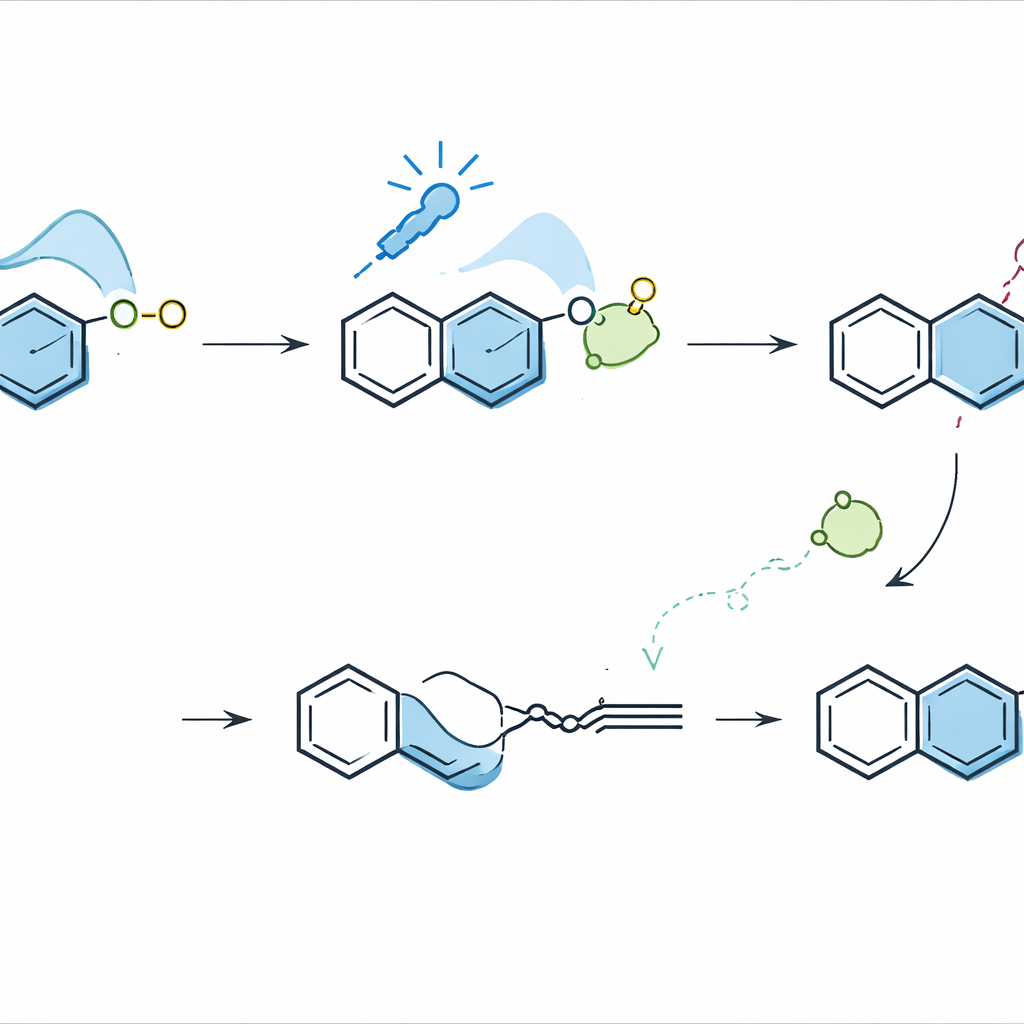
用新环构建更大结构
新合成的萘酯不仅是终点产物;它们可作为构建更复杂结构的积木。团队展示了一系列后续反应,将这些酯转化为高价值的多环芳香烃和手性配体,如苯并芴酮、咔唑、BINOL和QUINOL——这些骨架广泛用于材料科学和不对称催化。在另一例示范中,他们将该方法作为关键步骤,用于从易于拼装的异喹啉前体出发制备类阿达帕林(adapalene)的类似物。
这一工作对未来的意义
通过利用可见光翻转含氮环的电子特性,这项工作把原本不利的反应转变为强有力的骨架编辑工具。化学家现在可以直接将丰富的异喹啉转化为功能化程度很高的萘,绕开冗长的合成路线并保留易碎的侧链。对非专业读者来说,关键结论是——将现有分子“回收”成新核越来越可行,这可能加速更好药物和先进材料的发现,同时降低成本和浪费。
引用: Zhang, C., Zhang, J., Lan, Y. et al. Photoinduced polarity-mismatched transformations of isoquinolines into naphthalenes. Nat Commun 17, 2547 (2026). https://doi.org/10.1038/s41467-026-68969-1
关键词: 骨架编辑, 光化学, 异喹啉, 萘, 药物发现