Clear Sky Science · zh
结合诱导折叠调控替代轻链与前B细胞受体核组装
我们的身体如何试驾新抗体
在骨髓中的幼年B细胞被允许加入免疫系统之前,它必须通过一项严格的测试:能否构建一个可工作的抗体核心?本文探讨了一种特殊的“练习”版本的抗体部分,称为替代轻链,如何帮助执行该测试。通过观察这些蛋白如何折叠并相互配合,作者揭示了一个隐蔽的质量控制系统,它决定哪些未来的抗体足够好可以保留——以及哪些会被丢弃。
幼年免疫细胞的安全检查点
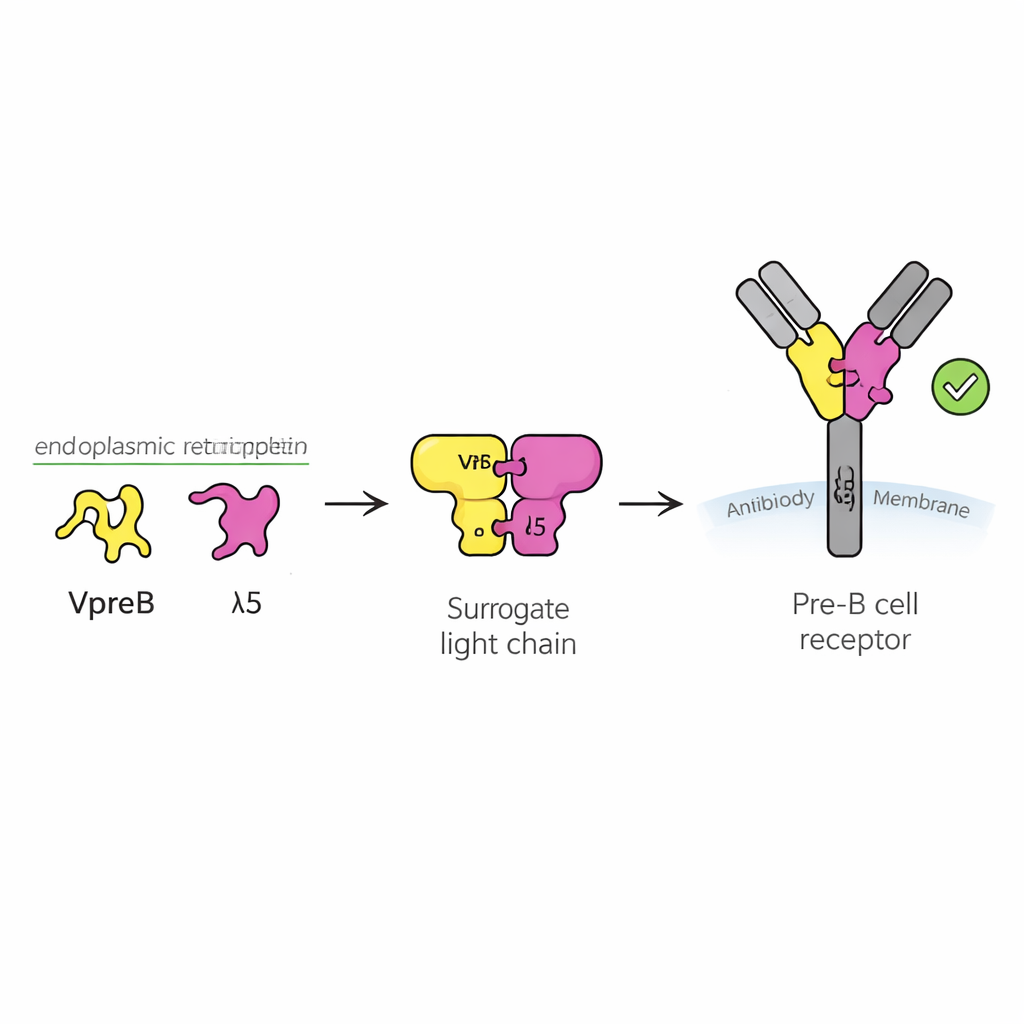
抗体是识别入侵病原体的Y形蛋白。它们由两个主要部分构成:重链和轻链。在B细胞发育过程中,重链先被制造,细胞必须判断这个新重链是否有用,才能继续投入能量去合成匹配的轻链。为此,细胞使用一种临时替代物,称为替代轻链,由名为VpreB和λ5的两种蛋白组成。与重链一起,它们形成前B细胞受体,这是细胞表面的一个传感器,发出“继续”或“停止”的信号。大约一半新重排的重链在这项测试中未通过,因此理解替代轻链的工作原理对于理解健康抗体库的建立至关重要。
通过结合进行折叠:帮助不稳定的搭档
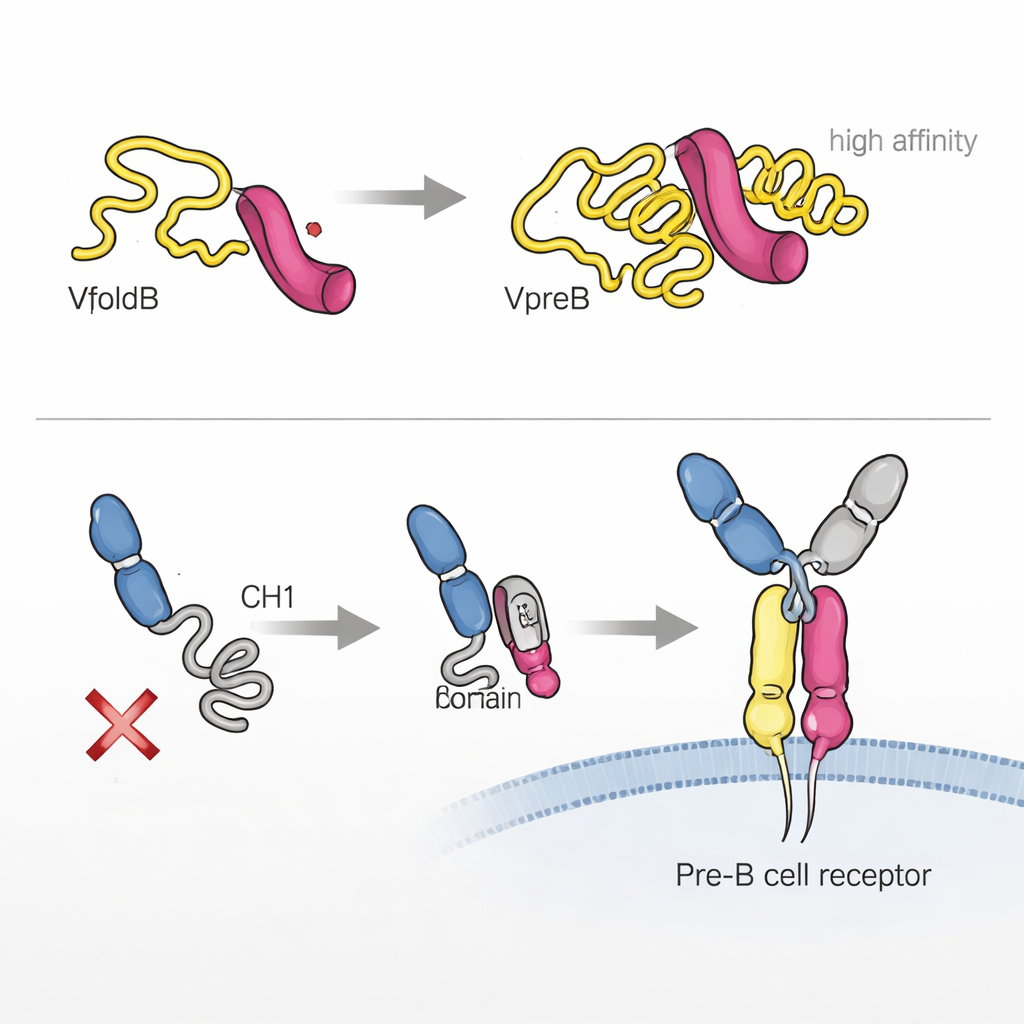
作者发现,其中一个组分VpreB在独自存在时大部分处于未折叠、不稳定的状态。通过生物物理学技术,他们显示出它只有在与λ5结合时才会迅速成形为正确的三维构象。λ5的一小段呈β链状,插入VpreB并完成其结构,类似把缺失的齿嵌入齿轮。这种“结合诱导折叠”不仅稳定了VpreB,也在两种蛋白间建立了非常紧密的相互作用,亲和力达到低纳摩尔水平。在细胞内,只有当VpreB和λ5组装成替代轻链时,它们才能逃脱内质网内的滞留并被分泌或转运到下一步,凸显了折叠与质量控制之间的紧密耦合。
完成重链并通过检查
故事并不止于VpreB和λ5。重链的一个关键区域,称为CH1,最初是无结构的并被保留在细胞内。研究人员表明,λ5在某种程度上像分子伴侣一样,当与CH1结合时能够诱导其折叠。这一第二步的结合诱导折叠对于构建完整的前B细胞受体并使其离开内质网到达细胞表面是必需的。有趣的是,替代轻链的两部分——VpreB和λ5——都能接触重链,但只有λ5能够将CH1推动到其最终的、具备折叠能力的状态。当这一过程未发生时,部分受体会被滞留,细胞因此有效地拒绝该重链。
微调结合与信号传导的柔性尾部
VpreB和λ5都带有松弛的、无结构的片段,称为独特区,这些序列与已知蛋白序列并不相似。尽管这些尾部在体外并非组装所必需,团队发现它们强烈影响替代轻链形成的速度、稳定性以及与重链片段的结合能力。在细胞中,去除这些区域会降低组装复合物的分泌效率。尤其是λ5的尾部表现出多重功能:它帮助加速组装、对与重链可变区的某些接触至关重要,并对前B细胞受体如何与抗原及其他配体相互作用作出重要贡献。在某些情况下,替代轻链—重链组合的抗原结合强度接近常规抗体片段的水平。
这对抗体多样性为何重要
通过描绘这些逐步发生的折叠和组装事件,作者提出替代轻链不仅仅是将重链固定在原位。它充当一个动态的检查者,利用其结构化的核心和柔性的尾部来感知重链是否能够正确折叠并与潜在靶标产生有效相互作用。成功的组合被折叠、稳定化并被允许到达细胞表面,在那里它们发出信号,促使B细胞继续成熟。缺陷组合则被滞留并最终清除。对非专业读者来说,结论是你的免疫系统运行着一个复杂的“试验台”来检测未来的抗体,这个系统由相互将彼此折叠成形的蛋白构成,以确保只有表现良好的抗体核心得以继续前行来保护你。
引用: König, J., Sarmiento Alam, N.C., He, R. et al. Association-induced folding governs surrogate light chain and pre-B cell receptor core assembly. Nat Commun 17, 1202 (2026). https://doi.org/10.1038/s41467-026-68965-5
关键词: B细胞发育, 抗体折叠, 替代轻链, 蛋白质质量控制, 前B细胞受体