Clear Sky Science · zh
通过设计的光酶实现结构多样的全烯底物的酶促去外消旋化
为什么“混搭”分子很重要
许多药物只有当其原子以非常特定的三维构型排列时才具有活性,就像左手只能套进左手手套而不能套进右手手套一样。化学家常能合成这些“单手”分子,但当构建模块复杂时很难做到高效且洁净。本文针对一类棘手的扭曲结构——全烯,采用定制的光驱动酶来应对这一挑战。研究展示了生物学与光化学如何结合,从混杂的混合物中筛选出所需的分子“手性”,为未来药物与材料提供更快更干净的合成路线。
回报丰厚的扭曲构件
全烯由三个碳原子线性相连并包含两个相邻的双键,这种简单排列会在空间上产生扭曲,从而使整个分子表现出手性(轴手性)。这种轴向扭曲出现在天然产物、作物保护剂以及高级催化剂中。不幸的是,传统制备手性全烯的方法往往高度专一:对一种全烯非常有效的催化剂,面对结构略有改变的另一种全烯时常常失效。即便是新近开发的光驱动化学催化剂也难以克服这一问题。因此,化学家在探索新全烯时常需重新从零设计催化剂,既拖慢发现速度又增加浪费。
借用自然的选择性并加入光能
生物体内的酶在识别和转化特定构型方面表现出惊人的精确性,但它们是为天然底物进化的,而不是为人工合成的全烯而设计。作者着手创造一种“光酶”,将酶样选择性与利用光作为能量源的能力结合起来。他们以名为 CTB10 的蛋白骨架为起点,通过基因改造引入一种非天然氨基酸,该残基像一个微小的内置光天线。当这个特殊基团吸收紫外光时,它可以将能量传递给邻近的全烯,使其暂时处于激发态并允许其构象扭转被打乱。通过重复这一过程多次,酶能够从50:50的混合物中选择性地去除一种手性,并留下主要为另一种手性的产物。 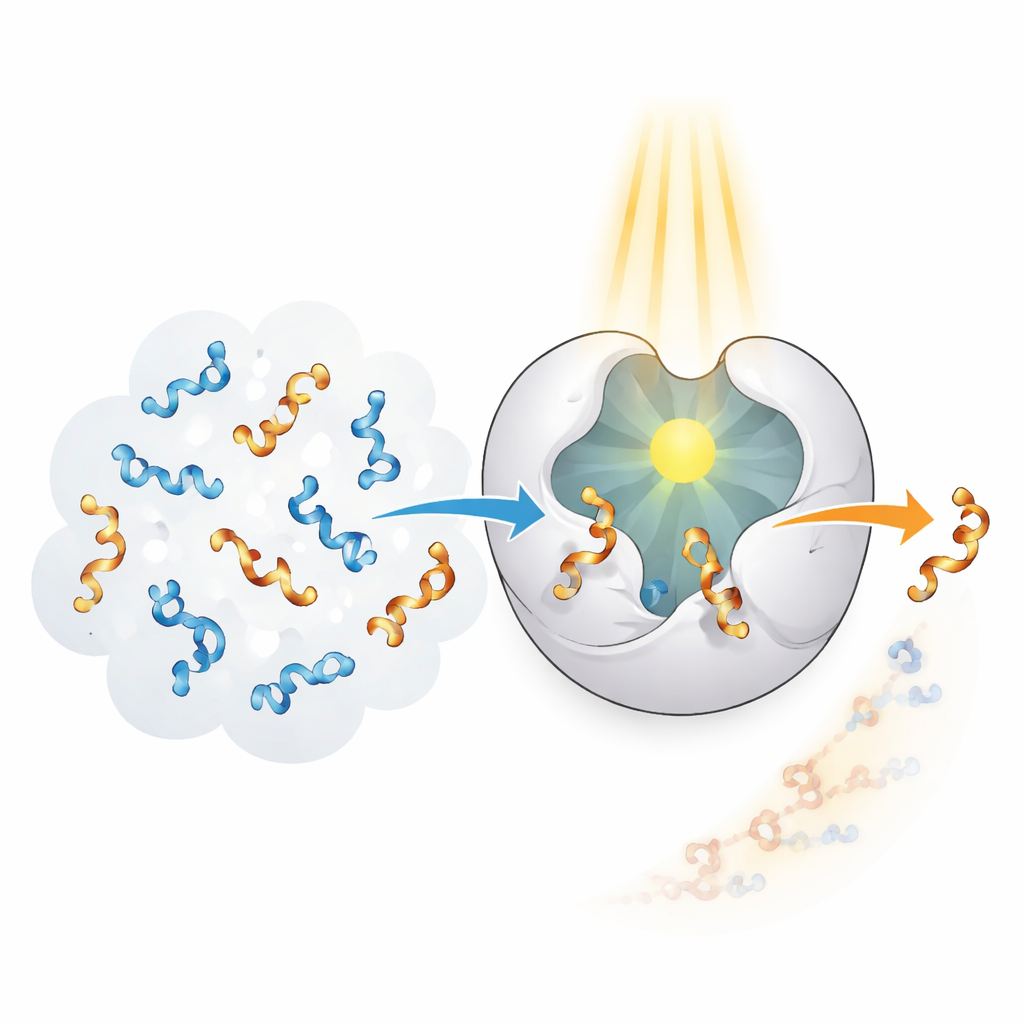
为多种客体雕刻合身口袋
设计这样的系统并不像对蛋白打光那么简单。研究团队使用计算建模、策略性突变和 X 射线结构快照来雕塑出数个光酶变体,每个变体内部口袋略有不同。这些口袋以特定姿态将全烯固定在光天线旁,通过氢键和细微的堆积相互作用稳定分子关键部位。研究者逐步提高了底物结合强度和酶与全烯之间的对位,这两点对高效的能量转移至关重要。最终的变体表现优异,将全烯羧酸、酯和酰胺转化为高纯度的单一手性产物,常常超过99%的一种手性,并且在空气中即可进行,无需非常娇气的反应条件。
以原子分辨率观察机理
为理解新光酶为何偏好某一手性,作者结晶化了酶–底物复合体并以原子分辨率对其进行了分析。他们发现,被偏好的全烯手性位靠近光收集基团,且可以采取几种略有不同的构象,这些构象都利于高效的能量转移。而不被偏好的手性要么结合较弱,要么距离较远,从而很难被激发。利用纯的右手或左手起始物进行的额外实验证实了这种偏向:酶会快速将被偏好的手性转化为一个反应性中间体,该中间体在溶液中再弛豫回到一个使对映体相反累积的混合物。本质上,蛋白像一个分子旋转门,不断激发并消耗一种手性,同时让另一种手性逐渐积累。 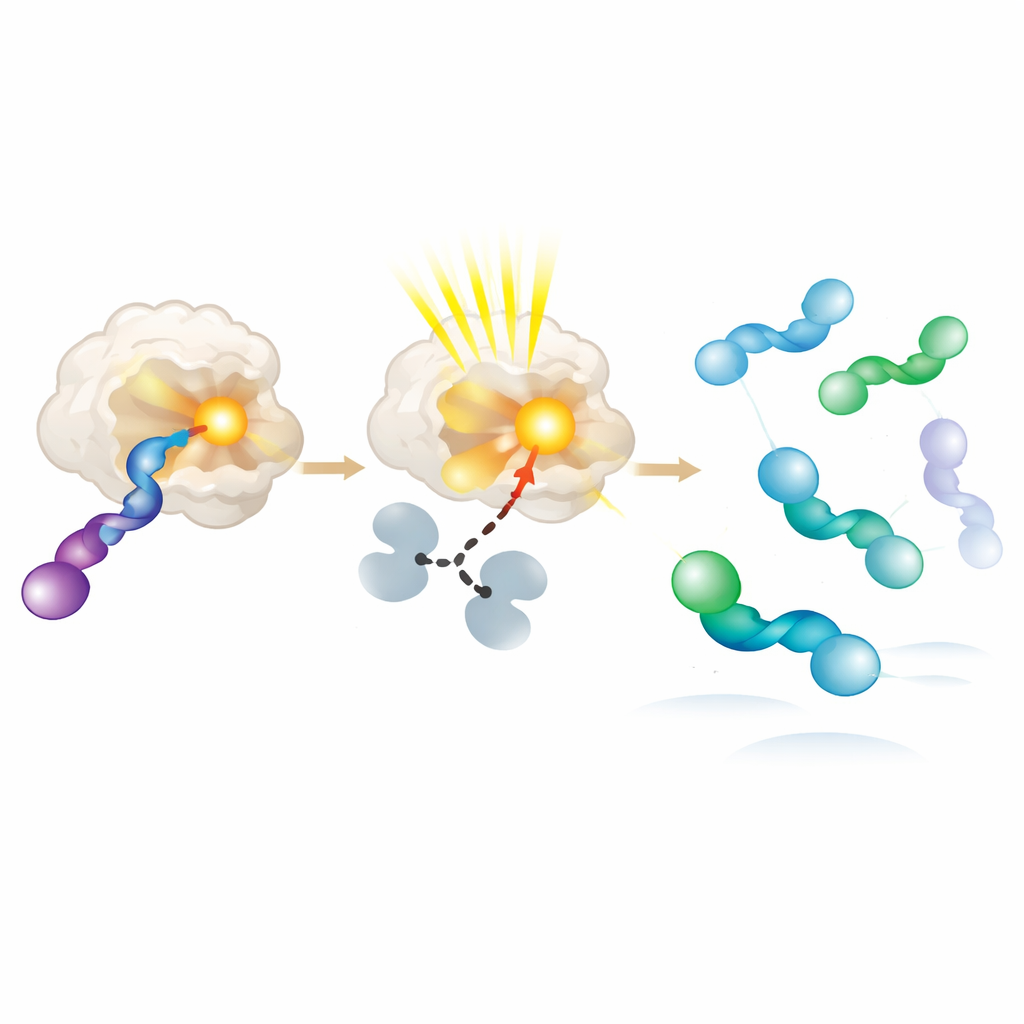
对未来化学的意义
对非专业读者来说,主要信息是该团队创造了一个可编程的蛋白分子机器,利用光对扭曲分子进行分选和升级,展现出前所未有的多功能性。研究者无需为每一靶标重新设计全新的化学催化剂,而是可以从这个光酶平台出发,通过调整其内部口袋来接受多种不同的全烯。这一方法缩小了自然的精细控制与化学工业对广泛、稳健方法的需求之间的差距。从长远看,这类光驱动的酶有望帮助化学家更高效地制备用于药物和材料的复杂单手性构件,步骤更少、废弃更少。
引用: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
关键词: 光酶, 去外消旋化, 手性全烯, 生物催化, 三重态能量转移