Clear Sky Science · zh
HCMV 感染破坏屏障功能并在胆管类器官模型中促进上皮-间质转化
为什么这则肝脏中病毒的故事很重要
人类巨细胞病毒是一种非常常见的病毒,大多数人携带时并不知情。但在新生儿和免疫系统脆弱的人群中,它可能与严重的肝脏和胆管问题有关,包括一种罕见但破坏性的儿童疾病——胆道闭锁。本研究利用实验室培养的微型人体胆管,展示了该病毒如何直接损伤这些脆弱的管道并触发可能解释感染与终生肝病之间长期争议联系的瘢痕化变化。
更近一步看这种常见却沉默的病毒
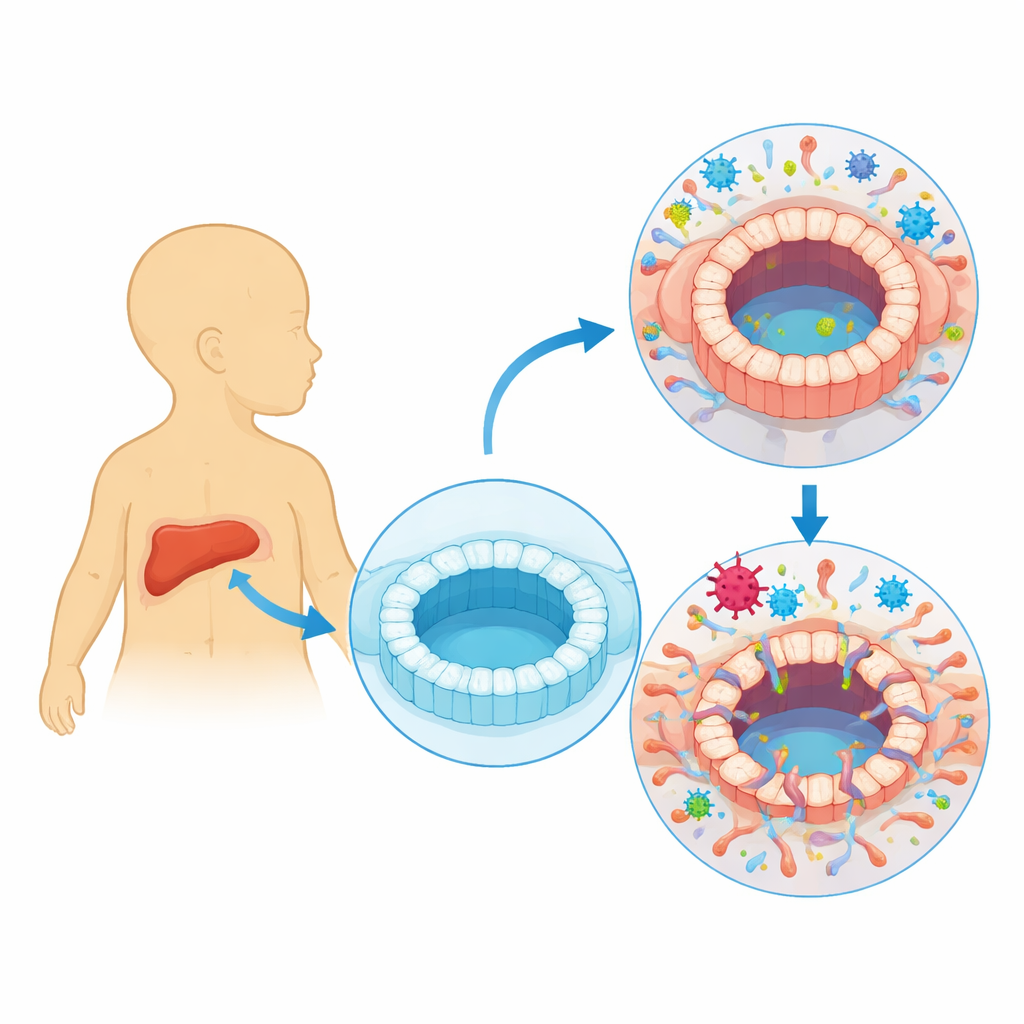
人类巨细胞病毒(HCMV)通常在人体内处于潜伏状态,在活跃复制和静默潜伏之间切换。临床上长期观察到,明确的 HCMV 感染者可能出现胆管损伤和胆汁淤积,即胆汁无法正常流动。许多患有胆道闭锁的婴儿,在出生后不久胆管阻塞并瘢痕化的同时,也显示出近期 HCMV 感染的迹象。然而,目前尚不清楚该病毒是否真的感染了胆管上皮细胞,还是在疾病过程中仅作为旁观者存在。
在培养皿中构建微型胆管
为了解答这一问题,研究人员构建了模拟人体胆管的三维“类器官”。他们以从人类血液重编程获得的诱导多能干细胞为起点,引导其分化为类胆管细胞(胆管上皮样细胞)。这些细胞自组装成具有中央腔和紧密细胞间连接的空心球,类似缩小版的胆管。研究团队随后用带有荧光标记的 HCMV 菌株感染这些类器官——当病毒活跃复制时标记会发光,从而使他们能够追踪被感染的细胞并测量类器官随时间的变化。
感染如何扭曲结构并削弱屏障
一旦被感染,类器官停止正常生长并变得畸形,壁变厚且不规则。部分细胞强烈发光,表明病毒活跃并产生新病毒颗粒;另一些细胞则携带较低水平的病毒遗传物质,提示更静默的潜伏样状态。功能测试显示,感染的类器官丧失了关键的胆管功能。它们在对依赖离子通道的刺激应答中不再正常膨胀,在测量屏障紧密性的电阻实验中更容易渗漏。通常封闭细胞间隙的蛋白(如紧密连接组分)减少,染料进出腔体的转运也异常。综上,这些变化表明 HCMV 可直接破坏胆管壁,使其变得渗漏且功能失常。
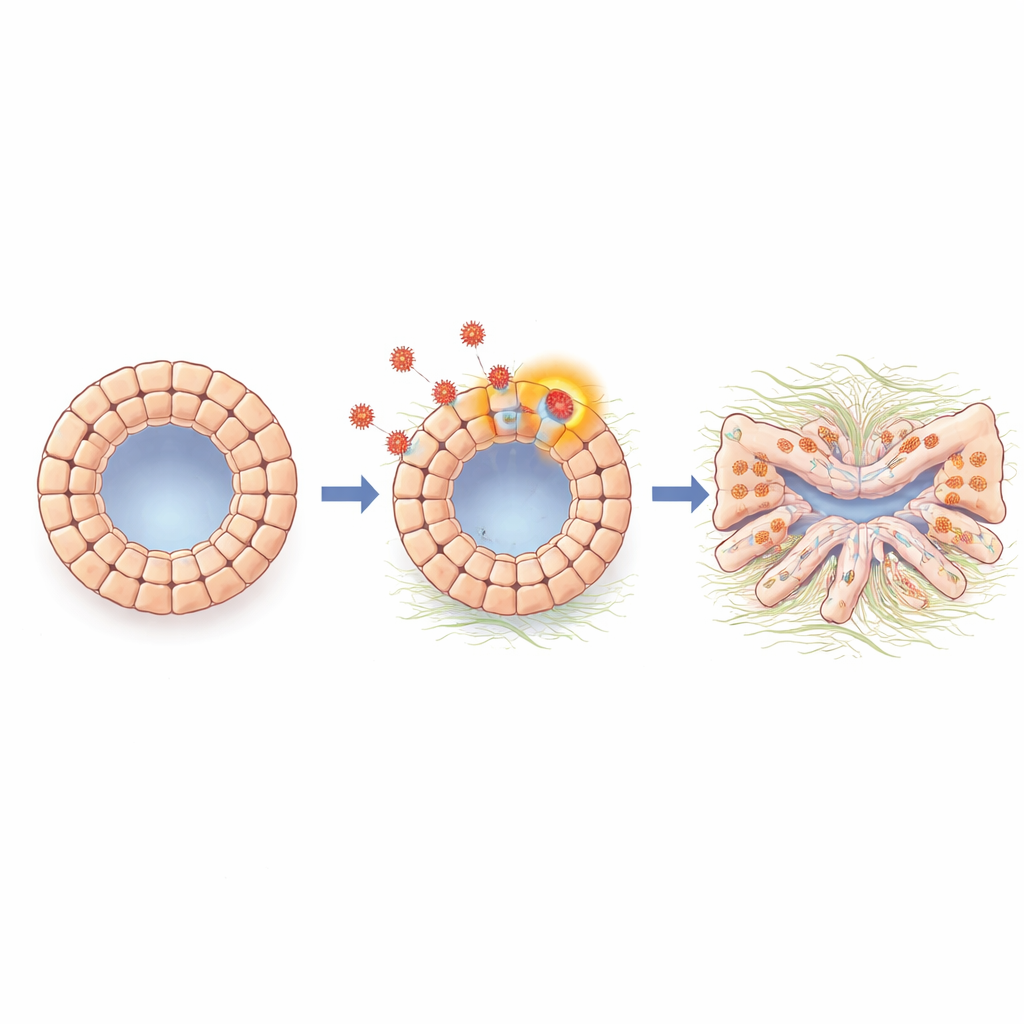
细胞向瘢痕化状态转变
进一步分析中,科学家在整体和单细胞分辨率上检测了类器官的基因活性,发现强烈激活了一种类似上皮–间质转化(EMT)的程序——在该过程中紧密相连的表面细胞松动连接,获得更多移动性和纤维样特性,并开始产生与组织瘢痕相关的分子。感染的类器官中观察到 N-钙粘蛋白和其他与这一转变相关的标志物增加,以及参与纤维化和基质生成的基因上调。一种被广泛认为推动多种器官瘢痕化的信号分子 TGF-β 在感染期间也被增强。当研究组用小分子抑制剂或抗体阻断 TGF-β 信号时,类器官恢复了更正常的形态,许多与瘢痕化和转化相关的基因表达回落至接近基线,说明 TGF-β 是连接病毒存在与有害细胞变化的重要中介。
从体外培养模型回到生病的儿童
为了确认这些实验室观察是否与真实疾病相关,研究者检查了患有胆道闭锁以及其他小儿肝病的儿童肝组织。使用高灵敏探针,他们在约三分之二的胆道闭锁样本中的胆管上皮细胞检测到 HCMV DNA,而在非胆道闭锁的肝脏中则远少见。在检测到病毒 DNA 的同一区域,胆管细胞显示出更高水平的 TGF-β 和 N-钙粘蛋白,吻合类器官中观察到的转化与瘢痕化模式。这提示,在至少一部分儿童中,HCMV 能直接感染胆管细胞并通过激活 TGF-β 驱动的通路将它们推向纤维化状态。
这对理解和治疗胆管疾病的意义
简而言之,这项工作表明,一种常见病毒可以入侵衬里胆管的细胞,松解它们的紧密连接,并通过以 TGF-β 为基础的信号将其推向瘢痕化、低分化的身份。这些变化削弱了胆管的屏障和转运功能,可能促成像胆道闭锁等疾病中观察到的阻塞性、纤维化胆管。尽管并非所有胆管疾病病例都由 HCMV 引起,该研究加强了这样一种观点:在易感婴儿中,病毒感染可能是病因学中的一环——且未来针对 TGF-β 相关通路的干预或许有助于保护或修复脆弱的胆管。
引用: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
关键词: 巨细胞病毒, 胆道闭锁, 胆管类器官, 上皮间质转化, TGF-β 信号