Clear Sky Science · zh
铜催化消旋α-卤酰胺对称转化的N-烷基化:制备富集对映体的联氮化合物
为什么这些微小分子很重要
许多现代药物和实验性类药物化合物包含一个小而关键的基团,称为联氮。若该基团具有“手性”——即主要以一种镜像形式存在,而非50:50的混合——会显著改变分子在体内的行为。本文所述的研究提出了一种新颖且高效的方法,从廉价且广泛可得的起始物出发制备这种单一手性(手性富集)联氮,可能会简化新药及生物活性分子的开发流程。
从简单原料到精确产物
作者的研究集中在两类简单的构建模块:联氮和消旋的α-卤酰胺。联氮含有一对氮–氮键,在药物、类肽结构及含氮富集的环系中很常见。消旋的α-卤酰胺是易于制备的化合物,其中一个反应性碳原子同时邻接卤素(如氯或溴)和酰胺基。如果能以受控方式将这两类组分连接起来,就能直接获得手性联氮,而无需预先构建更复杂的中间体。然而迄今为止,现有方法要么需要多步合成、使用不稳定的氧化试剂,要么局限于在实际分子中不常见的特殊反应伙伴。
铜作为分子引导的新角色
为解决这一问题,团队设计了一种基于铜的催化体系,能够将杂乱的消旋α-卤酰胺混合物与联氮结合时,选择性地形成单一优先生物手性产物。不同于难以与这些亲核且会毒化催化剂的联氮相容的传统“双电子”成键路线,他们采用了自由基–极性交叉途径。在第一阶段,铜配合物通过单电子化学去除α-卤酰胺上的卤素,生成一个短寿命的与金属配位的自由基。该自由基随后在铜中心重组,形成一个高度活泼、带正电极化的铜中间体。在第二阶段,联氮从被精心控制的一侧攻击该活化的伙伴,从而以高选择性只生成一种镜像构型。
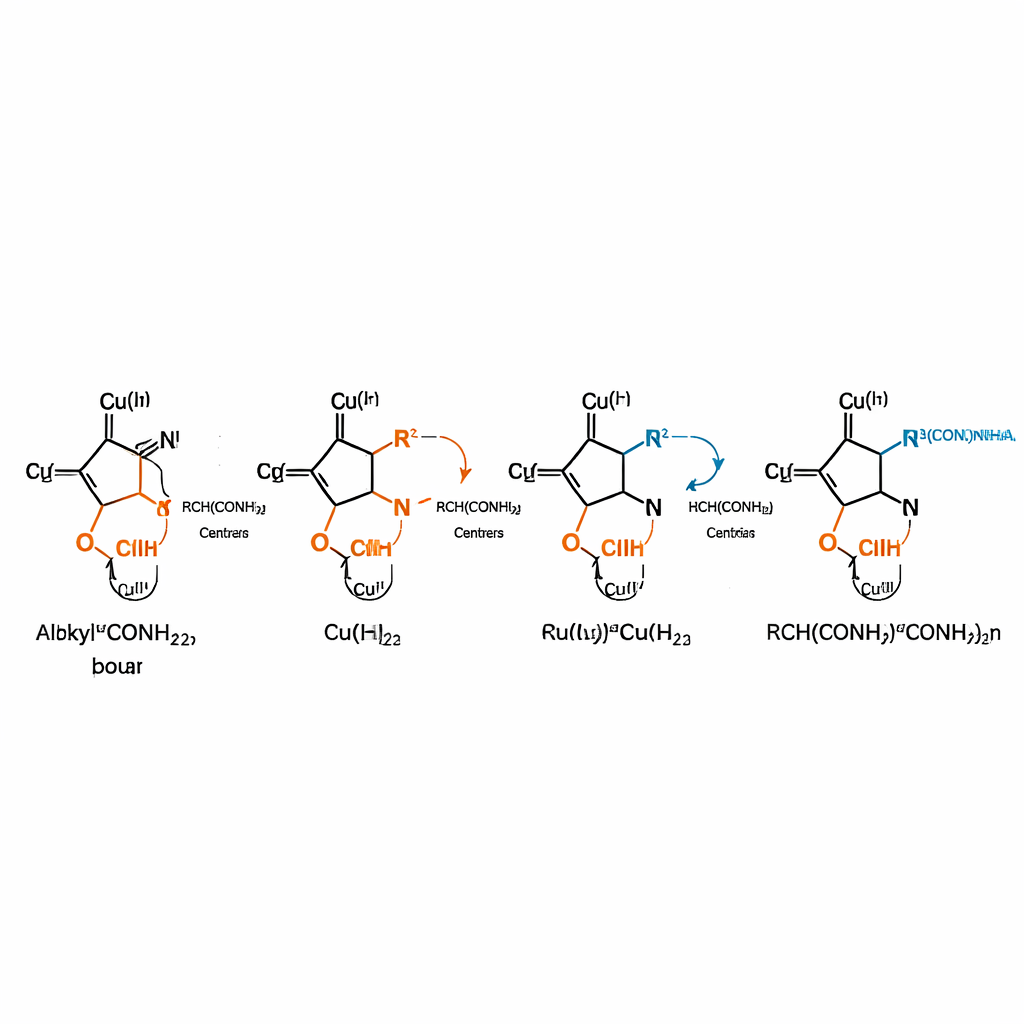
调配配方以实现广泛且实用的应用
这一进展的关键在于包裹铜原子的手性配体设计。研究者发现,三齿负电性的N,N,N配体——一种三臂、富含氮的骨架——至关重要。它能牢固配位,提高铜的还原能力使自由基迅速形成,并稳定决定选择性的高能铜(III)阶段。通过系统测试不同的联氮保护基,他们确定N,N-二Boc联氮是理想的伙伴:它能指向单一的氮位点、耐受反应条件,并可在后续温和去保护以得到游离的手性联氮。在优化的温和反应条件下,该体系可将多种消旋α-卤酰胺高产率并以优异的对映纯度转化为手性联氮,无论起始碳连接的是芳香环还是普通烷基链。
以精确形状构建肽和环状结构
当应用于更复杂的构建模块时,该平台的威力显现出来。利用源自天然氨基酸的α-卤酰胺,团队合成了N-氨基二肽——其中一个氮被联氮取代的短肽样片段。已知这些N-氨基单元能稳定非典型的肽构象并提高对酶降解的抵抗力,使其在药物设计中具有吸引力。值得注意的是,通过将手性配体的常规或镜像形式与任一手性的氨基酸起始物配对,化学家们能够获得特定N-氨基二肽的全部四种可能的立体异构体。这种“立体可逆”控制意味着从相同的简单输入可以制备一整套形态变体以供生物测试。
从构建模块到复杂结构
在形成保护态联氮后,可去除保护基得到作为稳定盐的游离手性联氮。随后这些联氮可与简单的羰基化合物顺利反应,构建一系列富含氮的环系——例如联氮唑、邻苯二唑酮和并接的肽–环杂化物——并在此过程中保持其单一手性。作者还证明了该化学可放大规模而不损失效率,这是走向实际应用的重要一步。总体而言,这项工作提供了一条从现成材料到精细调控的手性联氮及其衍生物的直接、模块化路线。
对未来的意义
对非专业读者而言,核心信息是研究者教会了一种廉价金属催化剂——铜——将一组混杂的起始片段按需组装成精确的“单一手性”产物。由于这些手性联氮可以方便地转化为许多药物所依赖的肽和富氮环系,该方法为药物化学家和化学生物学家提供了强有力的捷径。它应能更容易、更快速地探索分子形状如何影响生物活性,最终有助于发现新的治疗候选分子和功能材料。
引用: Li, N., He, SY., Wang, PF. et al. Copper-catalysed enantioconvergent N-alkylation of hydrazines with racemic α-haloamides to access enantioenriched hydrazines. Nat Commun 17, 2070 (2026). https://doi.org/10.1038/s41467-026-68961-9
关键词: 手性联氮化合物, 铜催化, 自由基–极性交叉, 对映选择性合成, N-氨基肽