Clear Sky Science · zh
基于人工智能的多组学分析揭示了个体化心血管疾病预测中互补的组学贡献
为何更早预测心脏问题至关重要
心脏病和中风仍然是全球首要的致死原因,常在看似健康的人身上毫无预警地发生。医生目前使用年龄、血压、胆固醇和吸烟等清单来评估风险,但这些工具可能漏掉许多未来的患者,也可能高估其他人的危险性。本研究提出了一个及时的问题:如果我们更深入地查看血液中循环的分子并用人工智能加以分析,能否在数年前就发现心血管疾病的迹象——并为每个人量身定制预防措施?
在血液中寻找隐藏的预警信号
研究人员利用了英国生物样本库(UK Biobank),这是一个追踪数十万志愿者多年健康状况的大型项目。在其中一部分参与者中,科学家们对血样中的数千种分子进行了精确测量:与脂肪、糖和氨基酸相关的小分子代谢物,以及参与炎症、凝血和其他生理过程的蛋白质。研究团队关注六类主要心血管疾病——冠状动脉疾病、中风、心力衰竭、房颤、周围动脉疾病和静脉血栓,探查这些分子指纹是否能够预测谁会发展出哪种疾病。
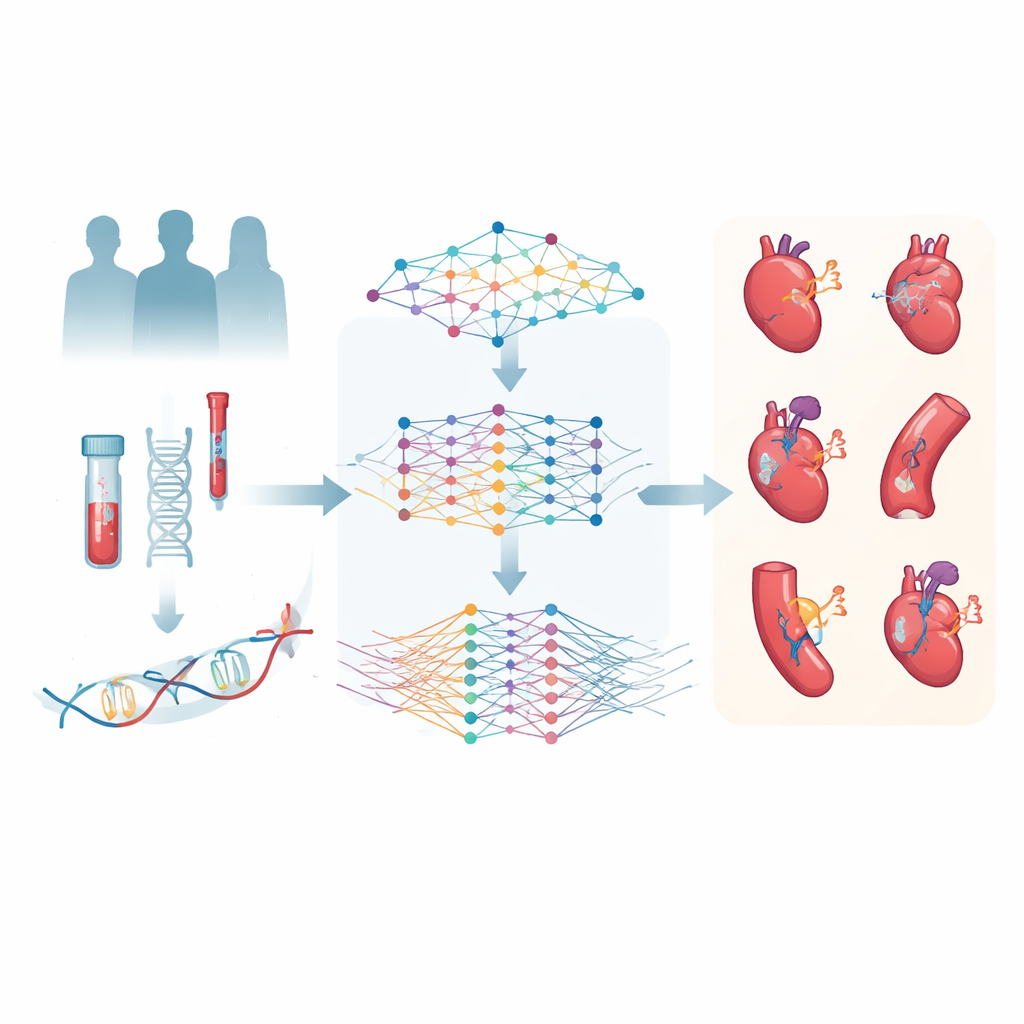
教人工智能读取分子模式
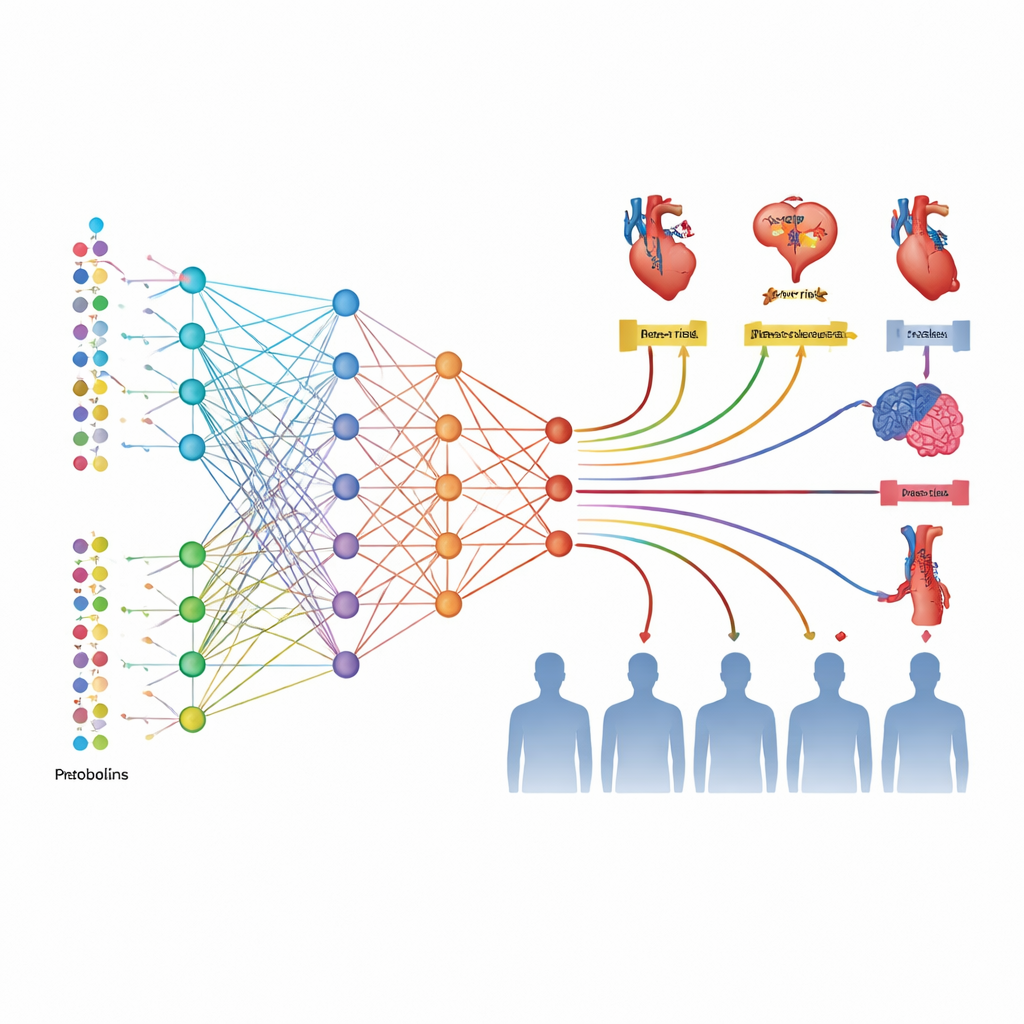
为了理解近3,000种蛋白质和168种代谢物,作者构建了两个深度学习模型:MetNet和ProNet。这些模型不是一次预测一种疾病,而是同时学习与所有六类心血管结局相关的模式。基于代谢物数据,MetNet生成了一个综合风险评分称为MetScore;基于蛋白质数据,ProNet生成了ProScore。因此,每个人在每个系统下都得到六个评分——对应每种心血管疾病——将数百万种可能的分子相互作用浓缩为几项数字,供标准统计模型连同年龄、血压、用药和遗传风险等临床变量一并使用。
这些分子风险评分到底提高了多少预测能力?
当团队在一组独立的24,287名同时具备各类数据的受试者中验证这些评分时,MetScore和ProScore单独就表现为强有力的预测因子,能够在15年随访期内清楚地区分低、中、高风险组。基于蛋白质的评分表现最佳,经常大幅优于传统的多基因(基于DNA)风险评估。将ProScore和MetScore加入常规临床因素后,各项心血管结局的预测准确性均有所提高,即便基线模型已较为详尽。在某些情形下,尤其是对周围动脉疾病和房颤,性能提升尤为显著,决策曲线分析表明医生在决定谁应接受预防治疗时可以做出更有益的选择。
分子揭示的疾病生物学信息
除了预测,研究人员还使用一种称为SHAP的解释方法,探查哪些特定分子在人工智能模型中最具影响力。他们确认了熟悉的标志物的重要性,例如肌酐和白蛋白(反映肾功能和整体健康)、以及像GlycA这样的炎症信号和NT-proBNP等心脏应激蛋白。与此同时,模型也突出了与炎症、凝血、血管重塑甚至神经损伤相关的一些较少为人所知的蛋白质和代谢物,呈现出部分共享、部分疾病特异性的模式。有趣的是,没有单一分子能匹配MetScore或ProScore的预测能力,这强调了心血管风险源于许多微妙变化的共同作用,而非单一罪魁祸首。
从大数据走向更个性化的心脏护理
研究得出的结论是,将遗传学、详尽的血液分子谱和常规临床信息结合起来,可以显著提升我们识别未来可能发展为主要心血管疾病个体的能力,往往能提前十年甚至更久发现高风险人群。尤其是蛋白质测量,似乎携带着关于正在进行的生物学应激的丰富且可操作的信息,远在症状出现之前。尽管现阶段所需检测尚未普及或便宜,但成本正在下降,作者已将他们的CardiOmicScore方法作为原型工具公开。经过在更多多样化人群中的进一步验证,这种基于人工智能的多组学分析有望帮助临床从千篇一律的检查表转向真正的个性化预防——更早识别高风险个体、将治疗与潜在生物学机制匹配,并有可能降低全球心血管疾病的负担。
引用: Luo, Y., Zhang, N., Yang, J. et al. AI-based multiomics profiling reveals complementary omics contributions to personalized prediction of cardiovascular disease. Nat Commun 17, 2269 (2026). https://doi.org/10.1038/s41467-026-68956-6
关键词: 心血管风险预测, 蛋白质组学, 代谢组学, 深度学习, 生物标志物