Clear Sky Science · zh
通过变构抑制剂靶向寨卡病毒 NS2B-NS3 蛋白酶并在小鼠模型中显示口服疗效
用一种新的方式智取危险病毒
十年前,当孕妇感染寨卡病毒与新生儿小头畸形和脑损伤相关联时,该病毒成为全球媒体关注的焦点。然而,至今仍无获批的药物可用于治疗或预防寨卡病毒感染。本研究描述了一种有前景的新型口服类化合物,它通过出人意料的机制关闭关键病毒酶,并能保护小鼠免受严重寨卡感染,这为未来可能保护易感人群、特别是在暴发期间的防护药物指明了方向。
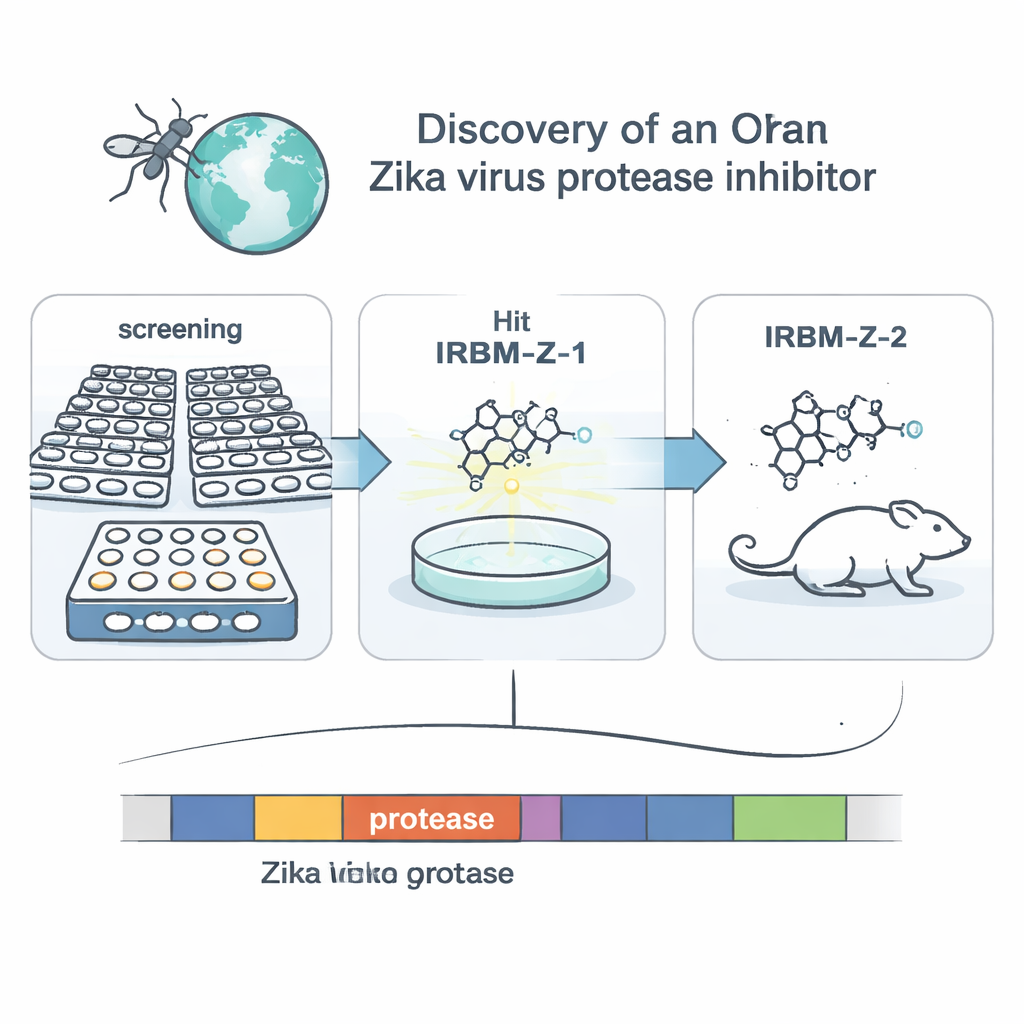
为何寨卡仍然重要
寨卡病毒主要经伊蚊传播,属于与登革热和西尼罗河病毒同一家族。大多数感染者症状轻微或无明显不适,但约五分之一的人会出现从发热、皮疹到严重并发症(如眼损伤、器官衰竭和神经系统疾病)等问题。对胎儿而言危险最大:孕期感染可导致小头畸形和终身残疾。由于尚无获批疫苗或抗病毒治疗,临床上只能提供支持性护理。因此,科学家将寨卡列为流行病防备的优先目标,寻求既可保护高风险人群又能遏制新一轮暴发的药物。
寻找隐藏的薄弱环节
研究者将注意力集中在一种名为 NS2B–NS3 的病毒蛋白酶上。这种分子“剪刀”将病毒的长前体蛋白切割成构建新病毒所需的片段,使其成为有吸引力的药物靶点。团队没有直接针对显而易见的切割位点设计药物,而是使用了一种模拟寨卡在猴肾细胞内复制的细胞筛选系统。他们构建了一个缺失结构基因但携带萤光素酶报告基因的改造寨卡基因组(复制子),以通过发光量来追踪病毒复制。筛选了来自国家化学库的超过12万种小分子后,挑选出那些能强烈降低发光信号且不损害细胞的化合物,随后对每个命中化合物进行了使病毒复制子产生抗性变体的培育。该遗传学线索指向了蛋白酶,表明其中一类化合物的关键靶点是该酶,其代表性起始分子被命名为 IRBM-Z-1。
将酶锁定在错误的构象
生化试验证明 IRBM-Z-1 并不与常规底物在切割位点竞争。相反,它表现为非竞争性或变构抑制剂——在一个独立的口袋结合,阻止酶采用其活性构象。高分辨率 X 射线晶体学显示,该化合物嵌入了一个先前未知、远离催化中心的口袋。在那里,它那不寻常的“N-酰基硫唑啉亚胺”核心通过一系列氢键和堆积相互作用,将蛋白酶的关键区域推入一种开放的、无活性的构象。该区域位于第156位的单个氨基酸变化即可使病毒产生抗性,强调了该化合物对这一隐藏位点的精确利用。这个口袋也不同于在相关黄病毒中描述的变构位点,为药物设计提供了真正新的落脚点。
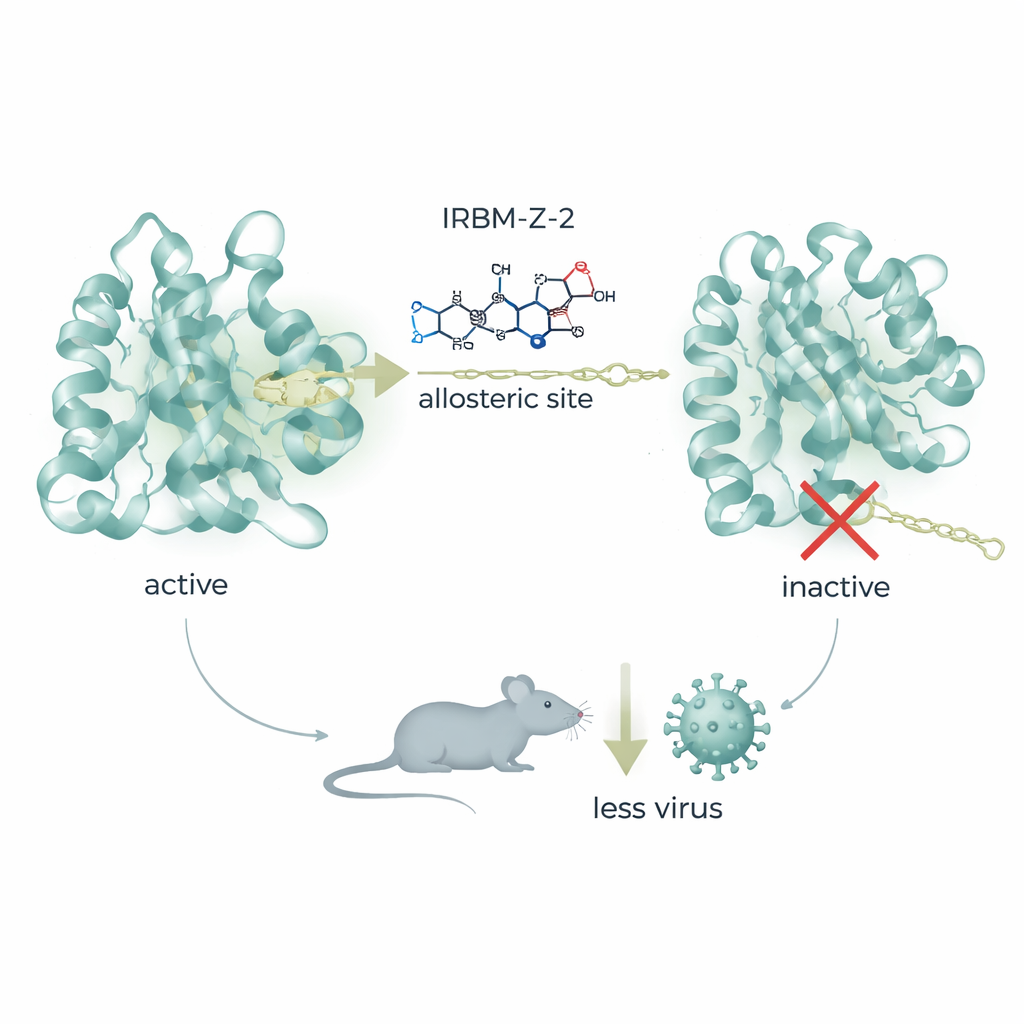
从命中化合物到在小鼠中显示保护的药物
在结构学见解的指导下,团队将 IRBM-Z-1 优化为更强效的分子 IRBM-Z-2。改良后的化合物在纳摩尔浓度下阻断寨卡蛋白酶,强效抑制多种细胞类型内的病毒复制,并对相关的登革热和西尼罗病毒蛋白酶显示活性,同时对人类酶的影响较小。在动物研究中,IRBM-Z-2 展现出良好的“类药物”特性:在体内稳定、口服吸收良好且血药浓度显著高于抑制病毒所需的水平,且未见明确毒性信号。在高度易感的 AG129 小鼠感染寨卡后,每日给药(注射或口服)能显著降低血液中的病毒 RNA 水平,防止体重下降和疾病症状,并使所有接受治疗的动物存活,而未治疗的对照组则死于感染。
这对未来暴发意味着什么
综上,这些发现引入了一类新型寨卡抗病毒药,其作用机制是将关键病毒酶锁定在无活性的构象而不是直接阻断其活性位点。由于 IRBM-Z-2 可口服,在严格的小鼠模型中表现出强有力的保护效果,且到目前为止具有良好的安全特性,它作为进一步开发的预防性药物候选物显得格外有前景——有可能在寨卡卷土重来时保护孕妇、医护人员和旅行者。更广泛地说,新发现的变构口袋可能激发针对相关病毒的类似药物,为对抗蚊媒疾病开辟新的战线。
引用: Ontoria, J.M., Torrente, E., Missineo, A. et al. An allosteric inhibitor of the Zika virus NS2B-NS3 protease with oral efficacy in mouse models. Nat Commun 17, 1439 (2026). https://doi.org/10.1038/s41467-026-68943-x
关键词: 寨卡病毒, 抗病毒药物, 蛋白酶抑制剂, 变构调节, 蚊媒疾病