Clear Sky Science · zh
FCHo2,而非talin,使整合素ɑvβ5在弯曲粘附处实现由内而外的激活
细胞如何感知周围的形状
我们的身体由不断与周围环境抓握、拉动和推动以移动、分裂或定位的细胞构成。本文揭示,细胞不仅能感知环境的刚度——它们也能读取环境的形状。作者发现了一种特殊的粘附系统,仅在细胞膜高度弯曲的部位开启,表明细胞在平坦与纤维状的环境中使用不同的内部“抓取”机制,这对组织形成和癌症扩散具有重要影响。
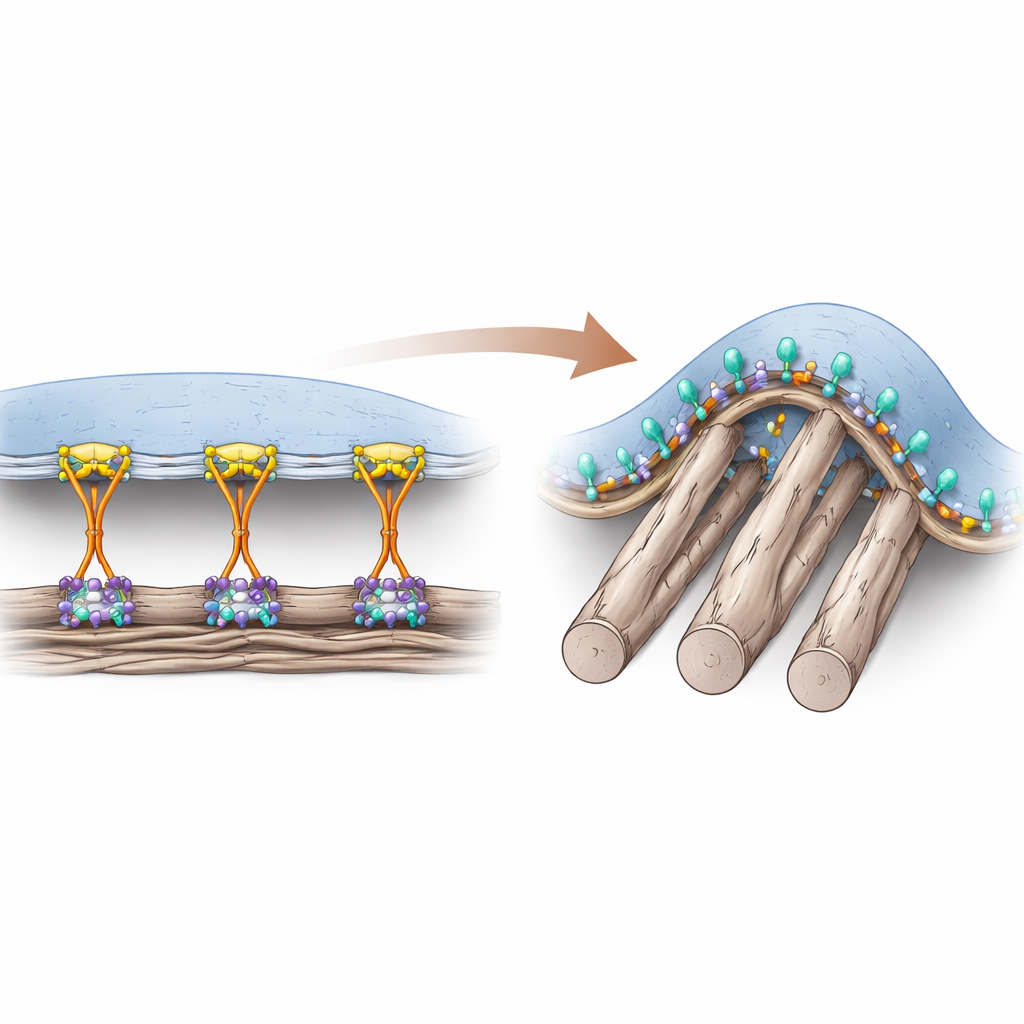
两种细胞的抓握方式
细胞通过称为整合素的表面受体附着于富含蛋白质的周围基质。多年来,研究者认为一种名为talin的辅助蛋白对从细胞内部“打开”整合素至关重要,从而在经典的锚定位点(即焦点粘附)中实现强连接。这些粘附主要在平坦、刚性的表面形成,并通过细胞骨架传递很大的拉力。然而在活体组织中,许多周围纤维既柔软又呈圆柱状,形成的接触点具有曲率,难以支持这些承受大力的结构。作者此前发现了一种不同类型的粘附结构,称为弯曲粘附,正好出现在膜绕薄纤维弯曲处,并依赖于一种特定的整合素αvβ5。
弯曲抓握采用不同的辅助蛋白
在这项新研究中,团队表明talin虽然仍然存在,但并非在弯曲粘附中激活整合素αvβ5的关键。取而代之的是一种感知曲率的蛋白FCHo2承担了该功能。通过使用精确设计的纳米级条状和柱状结构以受控方式弯曲细胞膜,他们观察到αvβ5在弯曲区域强烈聚集,但前提是FCHo2能结合β5尾段内侧的一个非常短的序列——HDRRE基序。当该基序被破坏时,整合素在焦点粘附中仍能发挥作用,但无法形成弯曲粘附。敲低FCHo2会使经典的焦点粘附基本保持完好,却消除了弯曲粘附;而去除talin则严重削弱焦点粘附,但对弯曲粘附影响不大。
一个氨基酸的开关作为形状选择器
一个难题是为何一个密切相关的整合素αvβ3即便其内侧尾段看起来与β5非常相似,仍无法形成弯曲粘附。通过在两种整合素之间交换结构域并引入点突变,作者找到了靠近talin结合位点的一个关键位置:多数β整合素在该位点为色氨酸(W),而β5独特地在位点有酪氨酸(Y766)。当将β5的酪氨酸替换为色氨酸时,该整合素失去了参与弯曲粘附的能力,行为更像β3,只偏向于焦点粘附。相反的改变——在β3样的嵌合体中引入酪氨酸——恢复了对曲率的敏感性。进一步用模拟磷酸化或非磷酸化状态的变体进行的实验表明,该酪氨酸的化学修饰可以使整合素偏向于平坦、高力的焦点粘附或弯曲、低力的粘附。
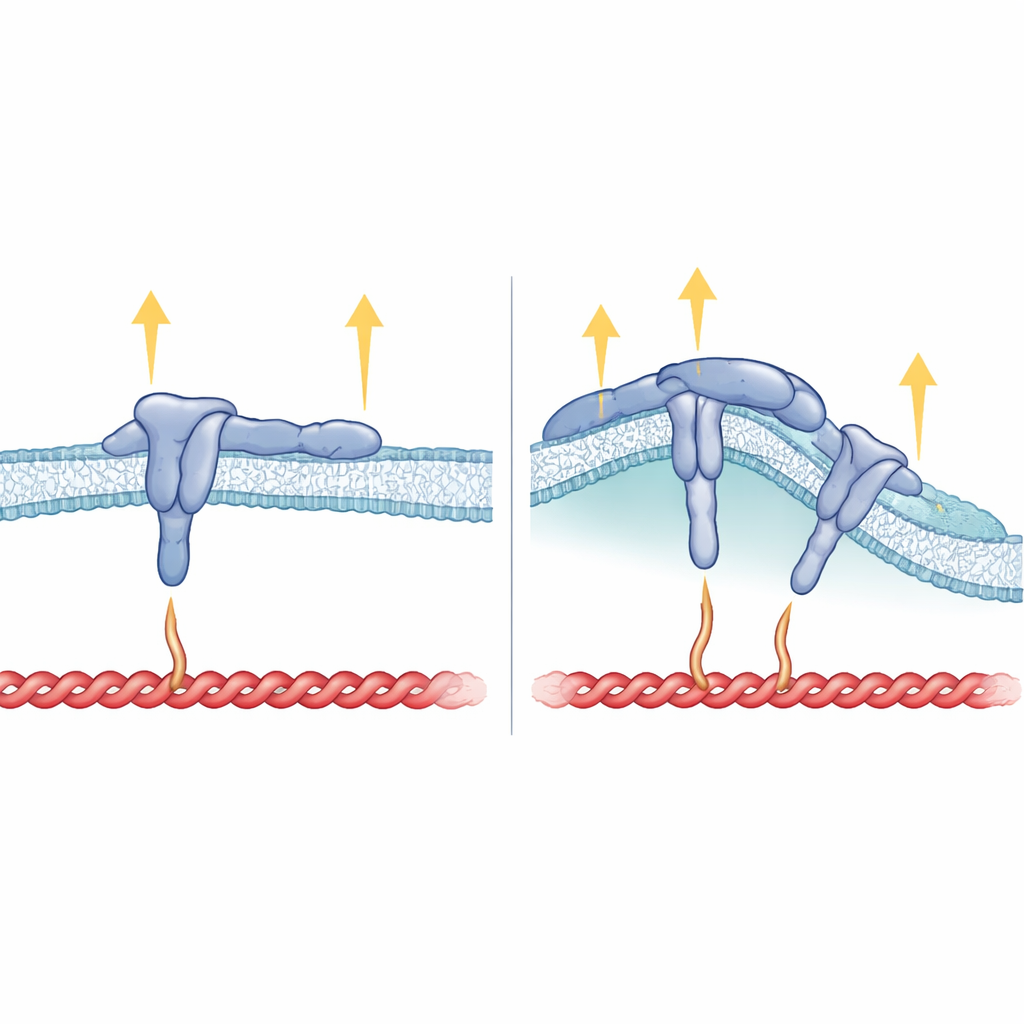
膜形状、整合素结构与力如何契合
除了内侧尾段外,穿膜段的那一段β5也被证明至关重要。当研究者将β5的跨膜片段替换为β3的对应片段时,所得的整合素仍能形成焦点粘附,但不再偏好弯曲位点,也不再与FCHo2同向追踪。这表明整合素在膜中的嵌入方式有助于定位HDRRE基序,使FCHo2能在弯曲区域结合并稳定配体结合的活性αvβ5。在弯曲粘附中,talin似乎仅接触整合素尾段较远的部分,且并不承受高张力,这解释了为何像vinculin、tensin和kindlin等需要大力的成分在这些部位基本缺失。相反,在焦点粘附中,talin同时抓握尾段的近端和远端以及膜,支持强大的牵引力,并阻止FCHo2进入同一区域。
这对细胞行为意味着什么
对非专业读者而言,这项工作的要点是:细胞拥有两种独立的“抓握模式”来粘附周围环境。在平坦、刚性的区域,它们使用由talin驱动的焦点粘附,设计用于强力拉动。在柔软、纤维状且弯曲的结构上,它们切换到由FCHo2驱动的弯曲粘附,以远低于前者的力稳定αvβ5。整合素序列中的微小差异——以及该位点是否被化学修饰——有助于决定采用哪种模式。这种双重系统使细胞能够在三维环境中同时解读刚度与形状,从而影响它们的迁移、组织构建以及在疾病过程中可能的侵袭行为。
引用: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
关键词: 整合素, 细胞粘附, 膜曲率, FCHo2, 细胞骨架