Clear Sky Science · zh
基于实验的聚合物模型揭示基因座的高分辨率组织结构
DNA 折叠如何塑造细胞身份
你体内的每个细胞基本上携带相同的 DNA,但脑细胞、皮肤细胞和干细胞的行为却大相径庭。一个关键原因是这些 DNA 在细胞核内的折叠和打包方式。本研究引入了一种能够以惊人细节“看到”这种折叠的新方法,将 DNA 的物理排列与关键基因的开/关状态联系起来。通过将实验数据与基于物理的计算机模拟相结合,作者揭示了看似作为基因组组织基本构件的隐匿基因物质簇。
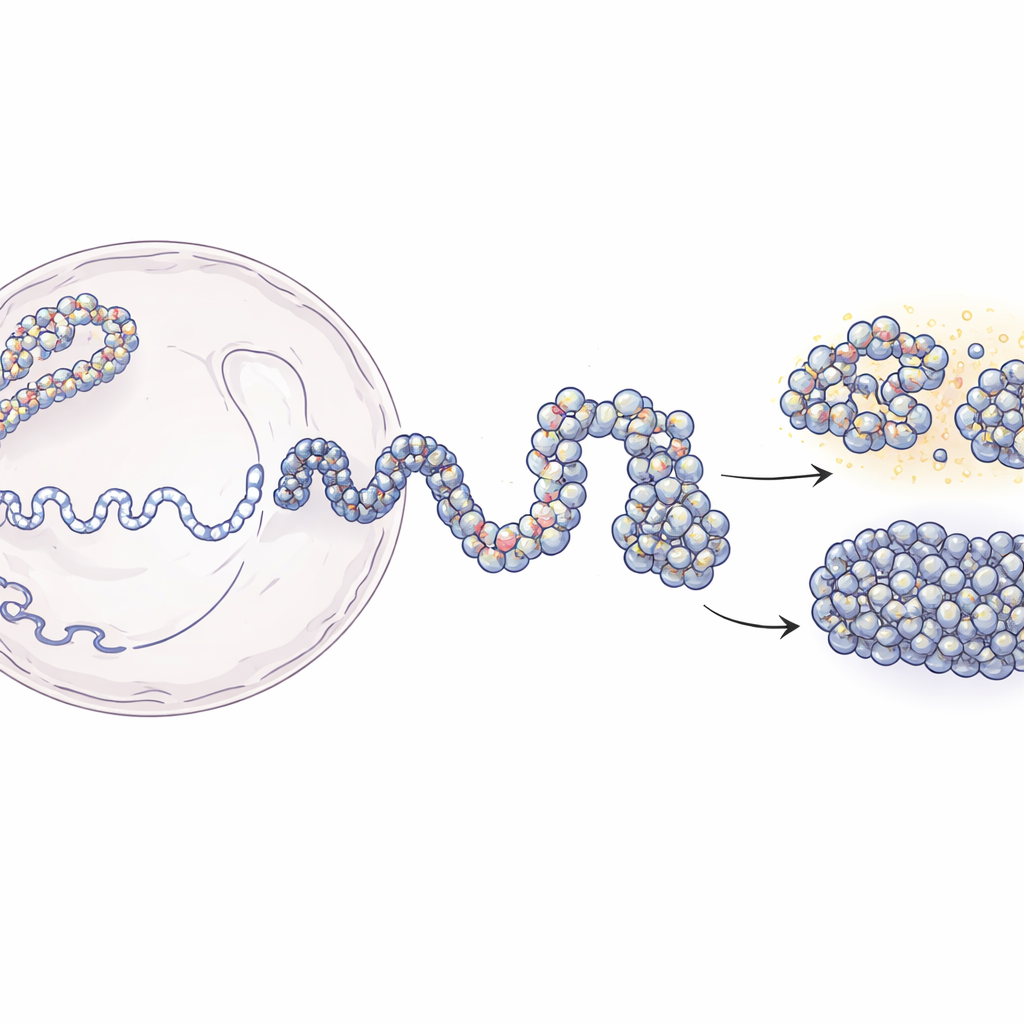
从长链 DNA 到三维基因组图谱
在细胞核内,DNA 绕着称为核小体的蛋白线轴缠绕,形成类似串珠的染色质结构。现代技术如 Hi-C 和 Micro-C 能告诉我们哪些 DNA 片段在三维空间中靠近,但这些方法通常给出模糊的、基于群体的平均图像。另一方面,定位单个核小体的实验能提供清晰的局部细节,却难以反映更大尺度的结构。本工作弥合了这一鸿沟。作者从报告远端 DNA 片段接触频率的低分辨率接触图出发,将其与核小体位置的实验图谱结合。利用聚合物物理学的原理,他们构建了符合实验数据的染色质三维模拟集合,同时将结构解析度提升到数十个碱基对的尺度。
重建染色质的两步策略
该建模方法分为两个主要阶段。首先,团队使用 Hi-C 数据生成大量可能的、大尺度的 20 万碱基长的 DNA 形态, 将染色质视为一条柔性的链,其中 5,000 碱基的片段被温和地引导以形成或避免实验中观察到的接触。这些粗粒度结构捕捉了细胞内蛋白质帮助形成的整体折叠模式。在第二阶段,每个大颗粒被替换为由单个核小体及其间短 DNA 连接片段组成的更精细链条。核小体的位置来自一种基于酶切的定位方法(MNase-seq),该方法揭示了它们在基因组上的典型分布。随后允许这些精细链在保持宏观架构约束的情况下折叠。当研究者将他们的高分辨率模型“模糊”回实验的分辨率时,能够高精度地重现 Hi-C 和 Micro-C 的接触图谱。
发现作为结构单元的核小体簇
当作者放大观察模拟结构时,出现了一个显著模式:核小体并非均匀分布,而是聚集成不规则簇,作者将其称为核小体簇(nucleosome blobs)。这些簇类似于超分辨率显微镜在真实细胞中观察到的块状结构。通过分析成千上万张模拟快照,团队表明这些簇呈细长形而非球形,通常包含数个紧密堆积的核小体。关键是,簇内部的接触对应于实验数据中看到的类似域的相互作用区块,这表明簇并非随机现象而是染色质三维组织的基本单元。模拟还预测了实验中难以检测到的额外微弱域边界,表明这一物理模型能从有噪声的数据中发现精细特征。
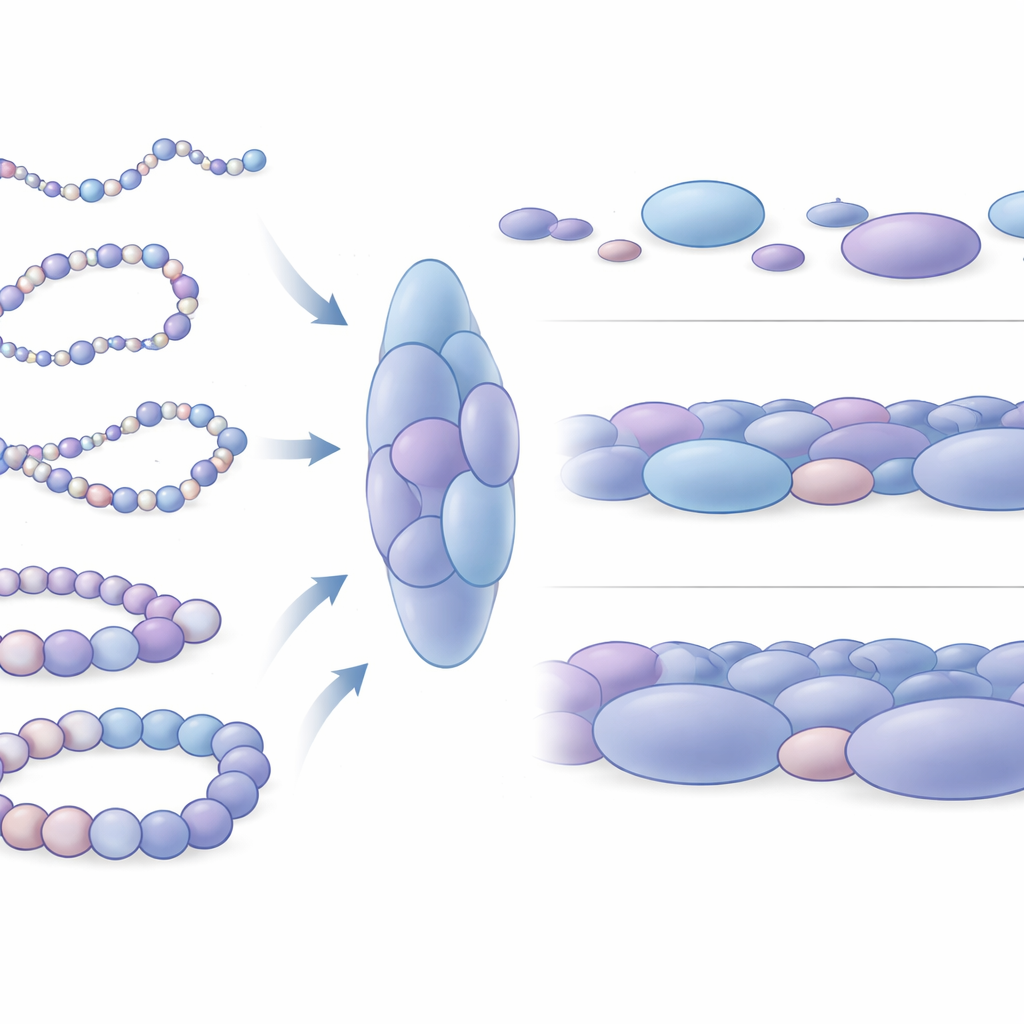
包装差异如何反映基因活性
接着,研究者考察了这些簇在活跃基因与沉默基因周围有何不同。他们聚焦于人类四段研究充分的 DNA 区域,包括两个位于干细胞中保持可塑性与未分化状态的基因(Nanog 和 Lin28A)以及两个位于同一细胞中被关闭的发育控制基因(HoxB4 和 HoxA13)。在不活跃基因周围,簇平均更大且更紧密,核小体形成更为封闭的局部排列。相反,活跃基因附近的簇更小、较松散且多样性更高。在更大的尺度上,活跃基因周围的 DNA 采样到更多不同的形状,力学上也更易弯曲,而沉默基因周围的区域则表现得像更僵硬的染色质片段。这种力学差异可能影响远端调控 DNA 元件相遇并与基因开关协同工作的难易程度。
这对理解基因控制为何重要
综合来看,这些发现描绘出这样一种图景:基因组由动态的核小体簇构成,其大小、形状和间距帮助决定附近基因是开放可及还是被封锁。该新模型将实验接触数据、核小体图谱和物理原理整合到一个框架中,解释了为何干细胞基因可以保持灵活与互作性,而发育基因则被隔离在更僵硬、更致密的邻域。对非专业读者来说,关键思想是基因活性并非仅由 DNA 序列决定;它还依赖于 DNA 如何折叠成三维结构。通过将核小体簇揭示为该折叠的基本构件,这项工作为将微观基因组结构与发育、细胞身份和疾病等大尺度过程联系起来提供了有力途径。
引用: Mittal, R., Heermann, D.W. & Bhattacherjee, A. An experimentally-informed polymer model reveals high resolution organization of genomic loci. Nat Commun 17, 2338 (2026). https://doi.org/10.1038/s41467-026-68928-w
关键词: 染色质折叠, 核小体簇, 三维基因组组织, 基因调控, 聚合物建模