Clear Sky Science · zh
硝基还原酶触发的吲唑形成
将简单原料转化为有价值的药物
许多现代药物都建立在少数几种常用的分子“骨架”上,这些结构能够可靠地与人体靶点结合。其中一种称为吲唑的骨架出现在用于抗癌和治疗严重恶心的药物中。到目前为止,合成吲唑通常需要使用强烈的化学药剂、高温以及对环境不友好的金属催化剂。本研究展示了科学家如何诱导天然酶在水相中温和地构建吲唑,从而为更绿色的制药方法打开了大门。
为何这些环状分子重要
药物设计者经常重复使用某些环状结构,因为它们能可靠地与体内蛋白质发生相互作用。吲唑就是这样一种受青睐的结构,存在于获批的抗癌药物和化疗引起的恶心治疗药物中。化学家已经掌握了几种合成吲唑的方法,但标准路线往往依赖活泼的构件、强碱或强酸以及如铜、钯等金属催化剂。这些方法虽然有效,但会产生废物、消耗能量并带来安全风险,与制药行业日益增长的可持续制造要求相冲突。
作为温和建造者的酶
作者没有用高温和强试剂强行将原子拼接在一起,而是采用生物催化——利用酶(大自然的催化剂)在水相、室温下促成反应。他们聚焦于称为硝基还原酶的酶,这类酶通常通过逐步还原帮助细胞解毒含硝基的化合物。研究团队推测,如果能在还原路径的某个恰当时刻释放出特定的中间体,该中间体就会自发折叠并形成典型的吲唑环体系。利用两种不同的硝基还原酶,他们证明了简单的2-硝基苄胺起始物在温和的水相条件下可以高效、顺利地转化为吲唑,转化率常常超过99%。
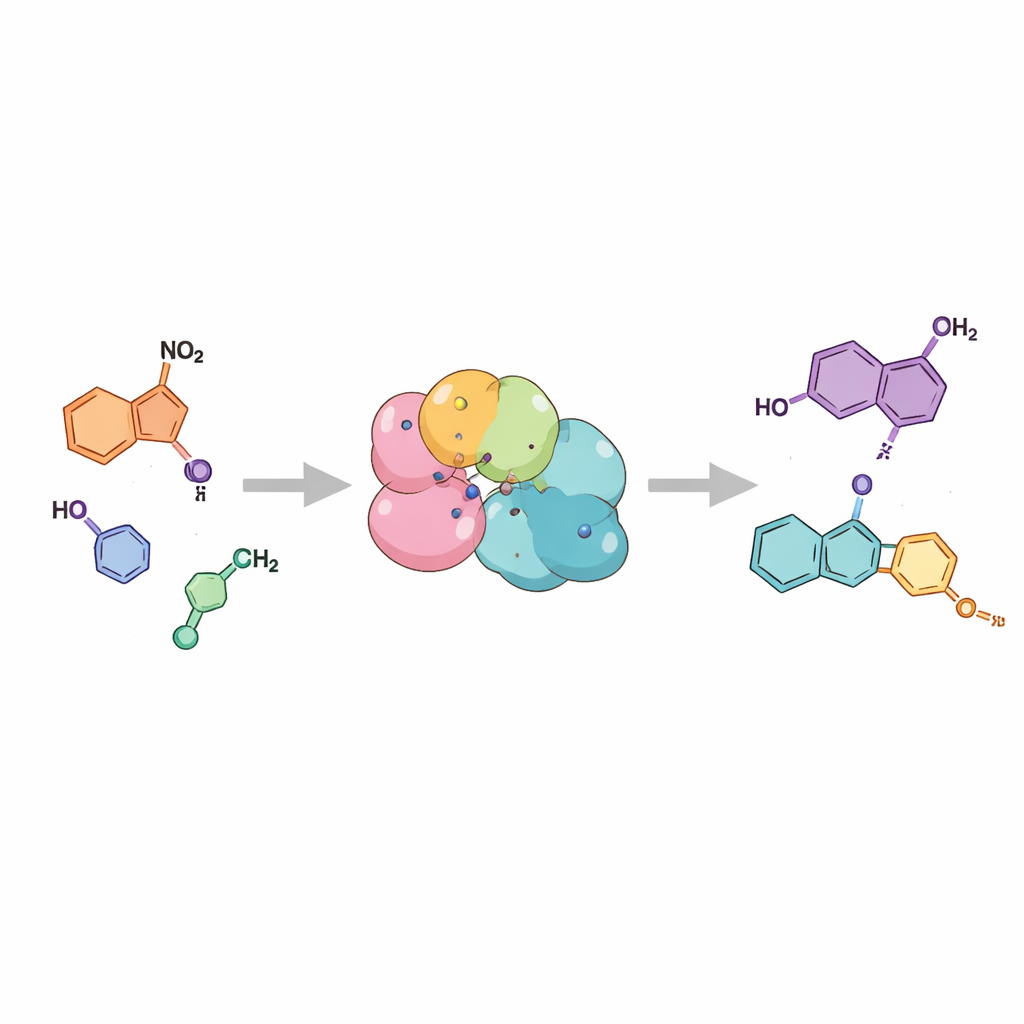
绘制酶的能力图谱
为了测试这一策略的通用性,研究者向酶提供了一系列带有不同取代基和位点的相关起始物。他们发现两种酶能够耐受广泛的化学修饰,从甲基等小基团到更庞大的环系,以及各种氯、溴和甲氧基取代。在许多情况下,反应能干净地生成目标吲唑,并且分离得率高到具有实用价值。起始物的取代方式还影响生成哪一种密切相关的吲唑异构体,这一点很重要,因为在药物设计中两种异构体都可能具有意义。同样的概念甚至可以扩展以合成吡啶并邻类的更大同系物——辛诺林,凸显了该方法的多功能性。
构建两步酶促装配线
文中所用的吲唑并非直接来自特殊试剂;相反,团队从廉价起始块出发,构建了一个短的酶促装配线。第一步,另一类酶——亚胺还原酶,将简单的醛和胺联结形成所需的2-硝基苄胺。第二步,硝基还原酶将该中间体转化为吲唑环。通过精细调节酶的用量和为其辅因子再生的体系,作者在制备用规模上运行了这个两酶级联反应,从水相中以50毫克醛为起始物。他们获得了几种吲唑产物,整体产率良好,包括具有不同侧链的实例,这些侧链以后可进一步修饰以用于药物发现。
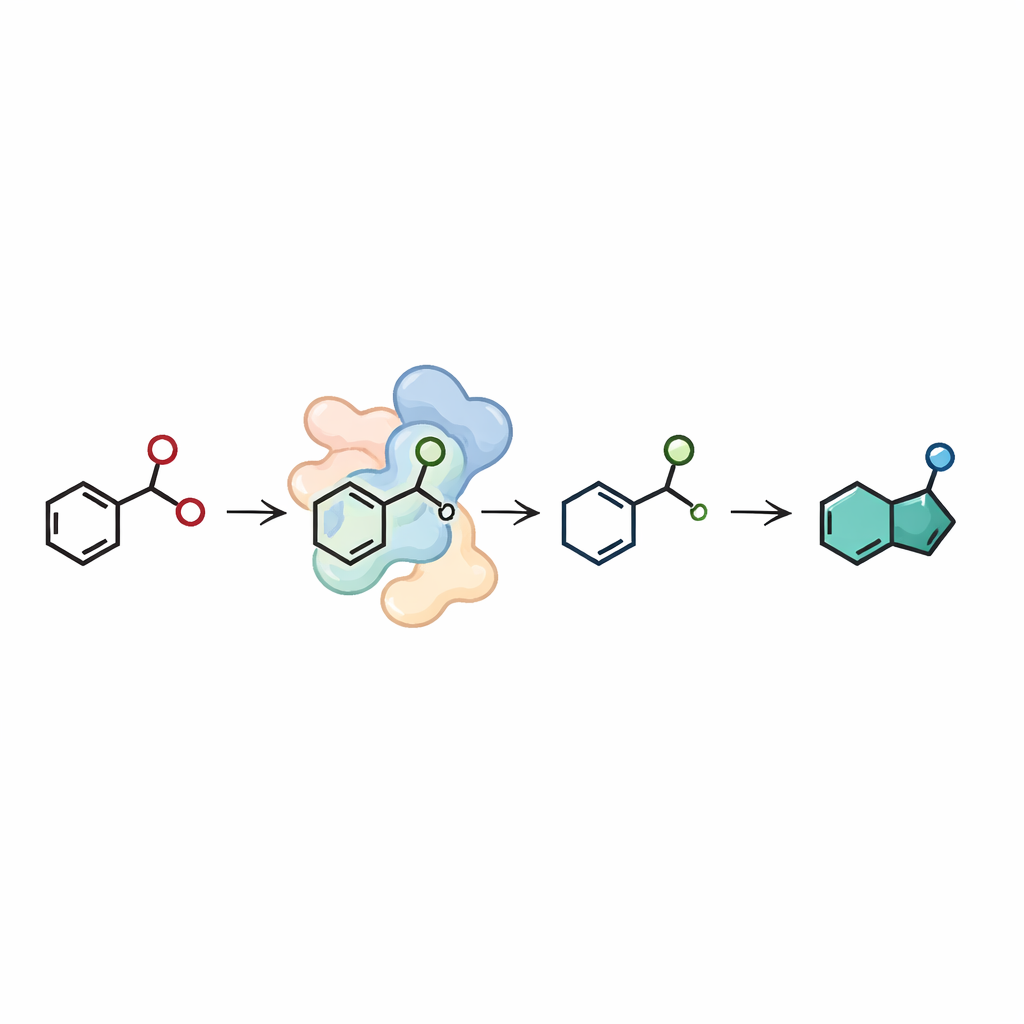
通往复杂药物构件的更清洁路线
对非专业读者而言,关键信息是研究者教会了天然催化剂以一种对工人和环境都更温和的方式组装一种具有药用价值的环系。他们的酶促路线避免了危险的氮—氮试剂和贵金属催化剂,在水相和适中温度下操作,并可与其他酶组合成高效的小型“工厂”。这项工作为化学家的工具箱增添了一个强有力的新手段,在为制药业提供多功能的吲唑构件以推动未来药物研发的同时,也使可持续制造更进一步。
引用: Terholsen, H., Medema, L., Chernyshova, E. et al. Nitroreductase-triggered indazole formation. Nat Commun 17, 2261 (2026). https://doi.org/10.1038/s41467-026-68926-y
关键词: 生物催化, 吲唑合成, 硝基还原酶, 绿色化学, 酶级联