Clear Sky Science · zh
新皮层第4层神经元对阿尔茨海默病抗逆性的分子特征
为什么有些脑细胞能战胜阿尔茨海默病
阿尔茨海默病以夺走记忆和思维功能闻名,但其破坏并非在整个大脑均匀分布。有些神经细胞早期丧失,而另一些即便在疾病晚期也出人意料地保持健康。本研究提出了一个充满希望的问题:这些更耐受的细胞有何不同?它们的生存策略能否转化为新的治疗方法?
三块大脑区域的故事
研究者聚焦人类大脑皮层的三个区域:两个在阿尔茨海默病早期受累(前额叶皮层和楔前叶,参与计划与记忆)和一个在晚期才受累(初级视觉皮层,负责视觉处理)。他们使用来自46具捐赠大脑的超过40万个分离细胞核,通过单核RNA测序读取单个细胞的基因表达,并利用空间转录组学将这些细胞映射回真实组织切片中的位置。两者结合使他们不仅能识别存在的细胞类型,还能精确看到易损与耐受细胞在分层皮层结构中的具体分布。
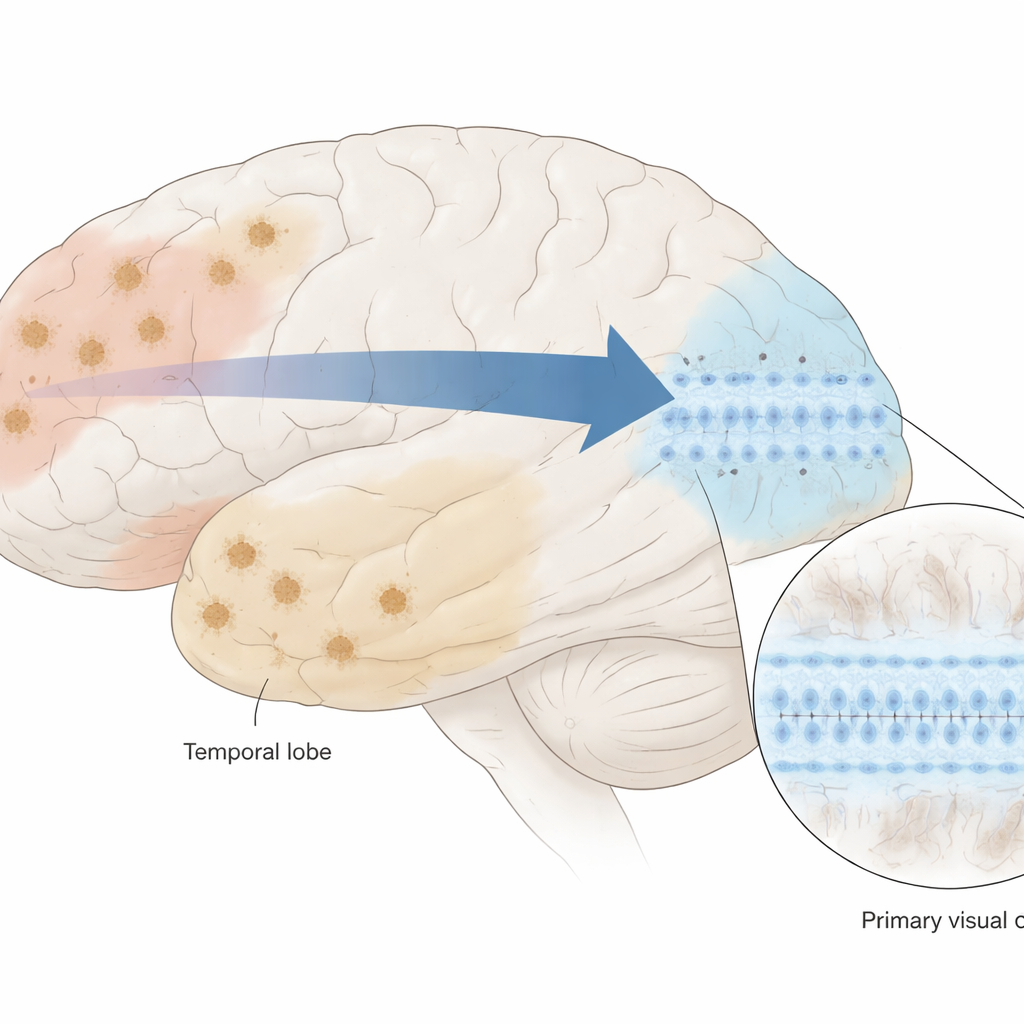
第4层神经元的隐秘韧性
在视觉皮层中,研究团队将注意力集中在第4层——一条密集的小胞体带,接收传入的感觉信号。这一层长期被注意到在阿尔茨海默病中相对保留,即使在存在黏性淀粉样斑块时亦然。团队发现了第4层中一类特定的兴奋性神经元——在其分析中称为Ex5——该类细胞在初级视觉皮层中特别丰富,但在其他皮层区域也有分布,尽管更稀少。随着阿尔茨海默病理的加重,许多其他神经元类型数量下降,而这些Ex5细胞保持稳定,甚至在残存神经元中占比上升,这强烈表明其具有细胞水平的抗逆性。
早期启动的保护性基因程序
为了解Ex5神经元为何能持久,科学家将这些耐受细胞的基因活动与更脆弱的相邻细胞进行了比较,尤其是涉及思维与记忆的上层易损神经元群。跨越疾病阶段与大脑区域,Ex5细胞上调了一组与保持突触完整性、微调电活动以及严格管理细胞内钙稳态相关的基因。其中许多基因在遗传学研究中已被证明会影响阿尔茨海默病风险。该模式表明,耐受神经元是主动在疾病早期启动一套防护程序,而不是仅靠偶然避开伤害。
聚焦于一种钾通道伴侣
一个名为KCNIP4的基因被确立为驱动抗逆性的强有力候选基因。它编码一种与神经元钾通道结合并帮助控制神经元发放易感性的蛋白。在人脑样本中,随着阿尔茨海默病理的加重,KCNIP4在耐受的第4层神经元中特异性上调,而在疾病晚期更脆弱的神经元类型中则下降。研究团队随后直接验证其效应:他们使用病毒载体在培养的小鼠皮层神经元和一个被基因工程改造成出现阿尔茨海默样变化的小鼠模型中增强了该基因的小鼠同源基因(Kcnip4)。在细胞培养中,表达额外Kcnip4的神经元在暴露于有毒淀粉样片段时仍表现出更少的钙活动爆发。在小鼠中,过表达Kcnip4减弱了皮层中神经元过度活动的标志物,同时并未加重淀粉样沉积,并伴有小幅减少的炎性小胶质细胞反应。
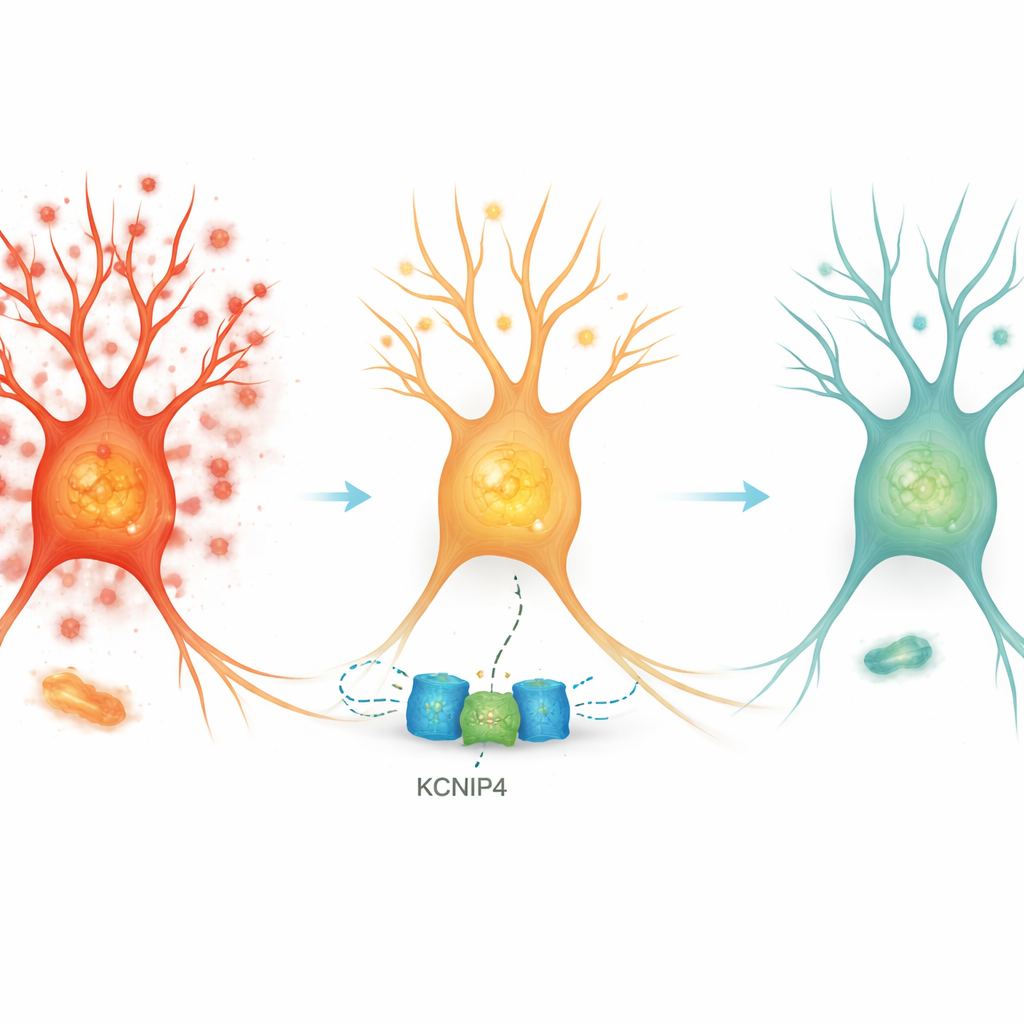
从耐受细胞走向未来疗法
综上所述,这些发现勾勒出这样一幅图景:某些视觉皮层神经元通过上调一套保护性基因网络来保持其连接稳定并抑制电活动,从而在阿尔茨海默病中幸存。KCNIP4位于该网络的中心,类似一种内置的刹车,抑制神经元过度兴奋——而这种过度兴奋被越来越多地认为是阿尔茨海默病及其他脑病早期损伤的驱动因素。尽管在将这些见解转化为治疗手段之前仍需大量工作,本研究提供了一张耐受性皮层细胞类型及其生存所用分子工具的详细图谱。那些相同的工具——尤其是安全微调神经元兴奋性的策略——或许有朝一日能帮助保护更易损的大脑区域免受阿尔茨海默病的侵扰。
引用: Dharshini, S.A.P., Sanz-Ros, J., Pan, J. et al. Molecular signatures of resilience to Alzheimer’s disease in neocortical layer 4 neurons. Nat Commun 17, 2223 (2026). https://doi.org/10.1038/s41467-026-68920-4
关键词: 阿尔茨海默病 抗逆性, 皮层第4层神经元, 单细胞转录组学, 神经元过度兴奋性, KCNIP4