Clear Sky Science · zh
通过表观遗传学对抗性FOX蛋白控制疱疹病毒裂解—潜伏平衡
隐匿的疱疹病毒为何重要
许多人终生携带单纯疱疹病毒,往往浑然不觉。这些病毒可以在神经细胞内静默多年,然后突然爆发,导致唇疱疹、眼部疾病,或在免疫功能低下者引发更严重的问题。是什么让病毒大多数时间处于“睡眠”状态,又是什么将其重新唤醒,这一直是个未解之谜。本研究揭示了该控制系统的一个关键组成部分:两组相互对抗的人类蛋白之间的拉锯战,这些蛋白重新塑造病毒DNA并决定疱疹是保持沉默还是开始复制出新病毒。
两个朝相反方向拉的细胞团队
作者将注意力集中在一大家族人类DNA结合蛋白——FOX蛋白,它们通常在发育和代谢中调控自身基因。通过在类神经细胞中筛查多种FOX家族成员,研究人员发现了两股明显对立的阵营。一组(包括如FOXF1等蛋白)显著增强了1型单纯疱疹病毒(HSV‑1)及若干相关“alpha”疱疹病毒的复制。另一组(FOXK1和FOXK2)则相反,强烈抑制病毒生长。这种平衡在不同细胞类型中并不相同:非神经细胞和受应激的神经元倾向于产生更多激活型FOX蛋白,而处于静息状态的感觉神经元几乎不产生这些激活蛋白,但表达大量抑制型FOXK蛋白。
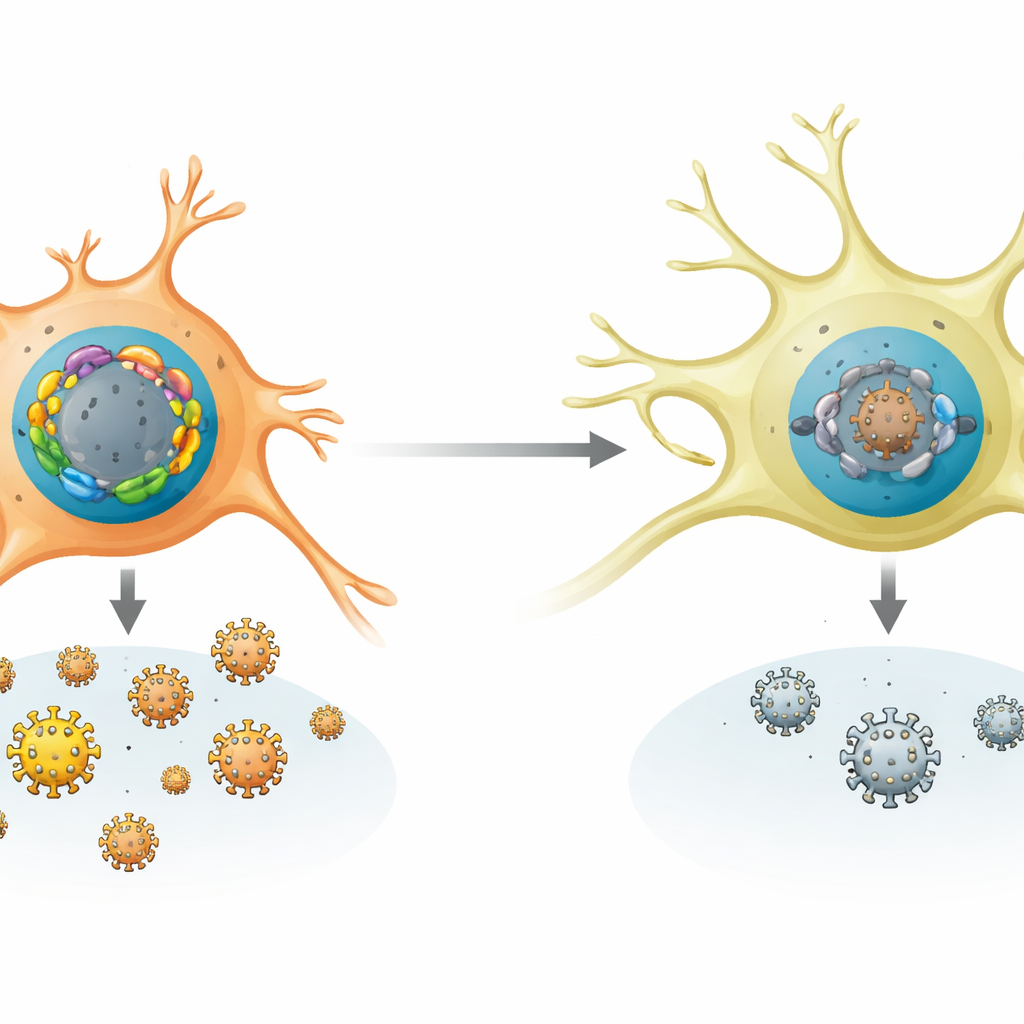
为什么神经细胞有利于沉默状态
研究团队比较了多种人类和小鼠细胞类型以及受感染动物中的FOX基因活性。感觉神经元——HSV‑1自然的潜伏宿主——显示出一种有利于沉默的模式:高表达FOXK1和FOXK2,而多数激活型FOX基因表达很弱。在小鼠体内,早期感染以及后续的应激信号(如发热或组织损伤)选择性地提高了若干激活性Fox基因的水平,但并未降低抑制性基因的表达。在培养的小鼠神经元和活体小鼠中,删除或敲低FOXK蛋白使HSV‑1更容易复制并从潜伏状态重新激活。相反,强迫神经元产生额外的激活型FOX蛋白即足以在没有化学触发的情况下诱导再激活,显示出病毒状态对这种FOX平衡的敏感性。
抓取病毒DNA并将其打开或关闭
为理解潜在机制,研究者绘制了FOX蛋白在病毒基因组上的结合位点。他们发现激活因子FOXF1和抑制因子FOXK1都广泛结合于HSV‑1 DNA上,而不仅仅局限于少数特定序列基序。此类结合依赖于FOX蛋白中保守的一部分,该部分抓握DNA骨架而非单个碱基,使它们几乎可以在任何位置附着。一旦就位,两派蛋白招募不同的分子伙伴来重塑染色质——DNA及其包裹蛋白的组合。激活型FOX蛋白,尤其是FOXF1,与CBP和P300等酶相关联,这些酶可将乙酰基添加到组蛋白上并松开染色质,从而使病毒DNA更易被访问并增强早、中、晚期病毒基因的表达。相比之下,FOXK1与SIN3A和MAX等因子协作,这些因子与组蛋白去乙酰化和基因压制相关,收紧病毒染色质并维持基因沉默。
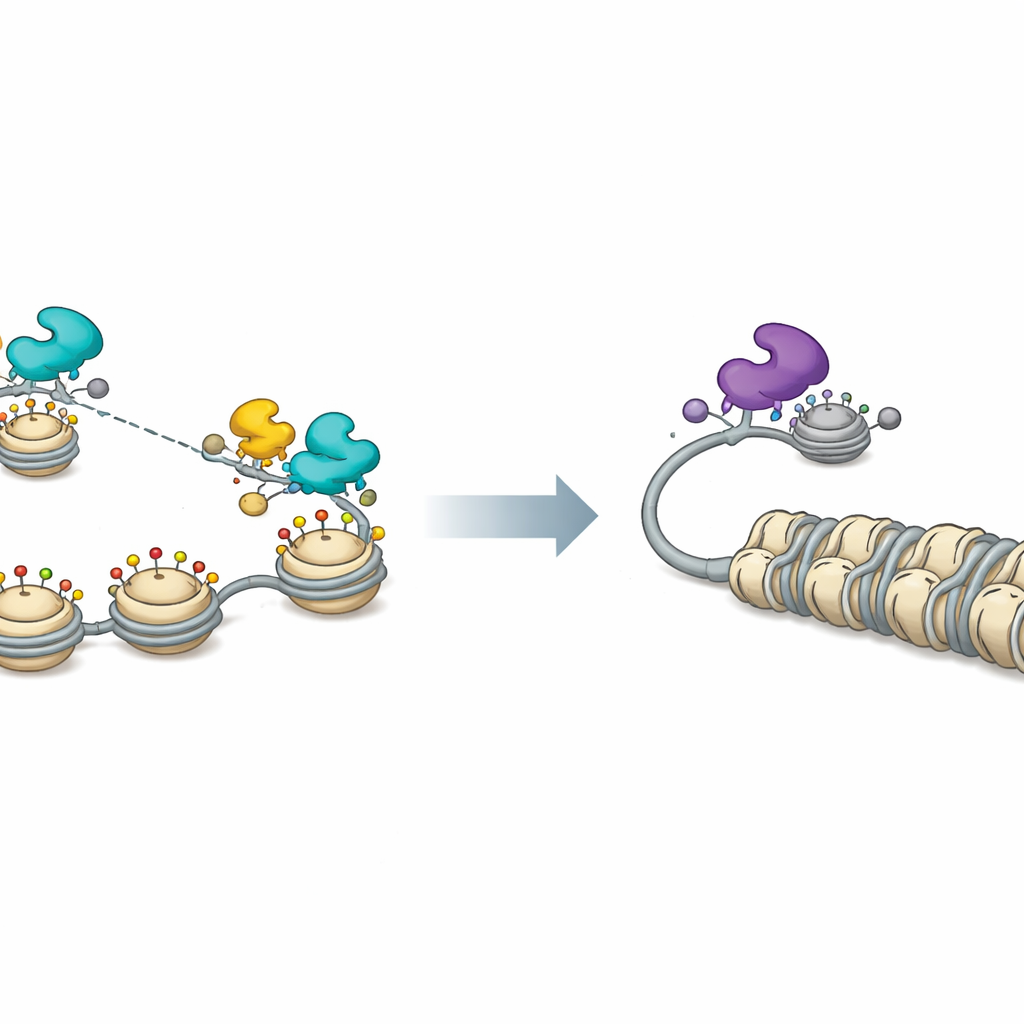
决定病毒睡眠与觉醒的染色质开关
对病毒染色质的测量证实了这一图景。当存在FOXF1时,病毒DNA上的组蛋白被去除或出现与开放、活跃染色质相关的化学标记,病毒启动子的整体可及性在基因组范围内增加。FOXF1的表达还使通常帮助保持病毒DNA受抑的小型核结构PML核体分散。阻断CBP和P300抹去了许多这些激活效应并降低了FOXF1驱动的病毒基因表达。在抑制方面,研究者显示FOXK1相关的伙伴和组蛋白去乙酰化活性对于维持低水平HSV‑1复制很重要;化学抑制去乙酰化酶既增加了病毒产量,也削弱了FOXK1介导的抑制。
对控制终生感染的意义
综合来看,这项工作表明HSV‑1处于活跃或休眠状态在很大程度上取决于其宿主神经元内FOX蛋白的组成。静息的感觉神经元天然偏向以FOXK为主导的抑制状态,将病毒推入一种高度沉默、染色质致密的形式。应激或其他条件若提高激活性FOX蛋白,可使这一平衡倾斜,打开病毒染色质并允许裂解周期重新开始。通过揭示这种表观遗传的拉锯战,研究强调了未来科学家或许可以通过新的方式将疱疹病毒更稳固地推入无害的潜伏状态,或在受控条件下将其迫出藏匿位置以便清除。
引用: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
关键词: 单纯疱疹病毒潜伏, FOX转录因子, 病毒染色质, 表观遗传调控, 病毒再激活