Clear Sky Science · zh
代谢硫酮酶复合体的进化性再利用使抗生素生物合成成为可能
日常微生物如何重塑它们的化学能力
我们依赖的许多抗生素和药物,都是由细菌在背后悄然合成的。这些微小的化学家利用酶——分子机器——构建复杂的防御性化合物。本研究揭示了一种核心代谢酶复合体如何在口腔细菌中被进化性地改造,用来制造一种高效抗生素。理解这一转变不仅展现了自然如何开创新的化学反应,也为设计下一代药物和生物催化剂提供了线索。
从基础代谢到化学武器
所有生物细胞都依赖一组保守的酶来维持中心代谢,例如分解脂肪和合成必需分子。其中一类称为硫酮酶超家族,通常帮助处理诸如乙酰辅酶A等小而富能的分子,并支持合成脂类和其他细胞成分的重要途径。作者发现,在若干口腔链球菌(Streptococcus)物种中,一个由三部分组成的基于硫酮酶的复合体——由与HMGS、ACAT相关的蛋白及第三种辅助蛋白构成——已放弃其祖先的代谢角色。取而代之的是,该复合体完成了一种名为重粘菌素A(reutericyclin A)的抗生素的生物合成,这有助于这些细菌在拥挤的口腔环境中竞争。
在抗生素骨架上发生的新型酶促反应
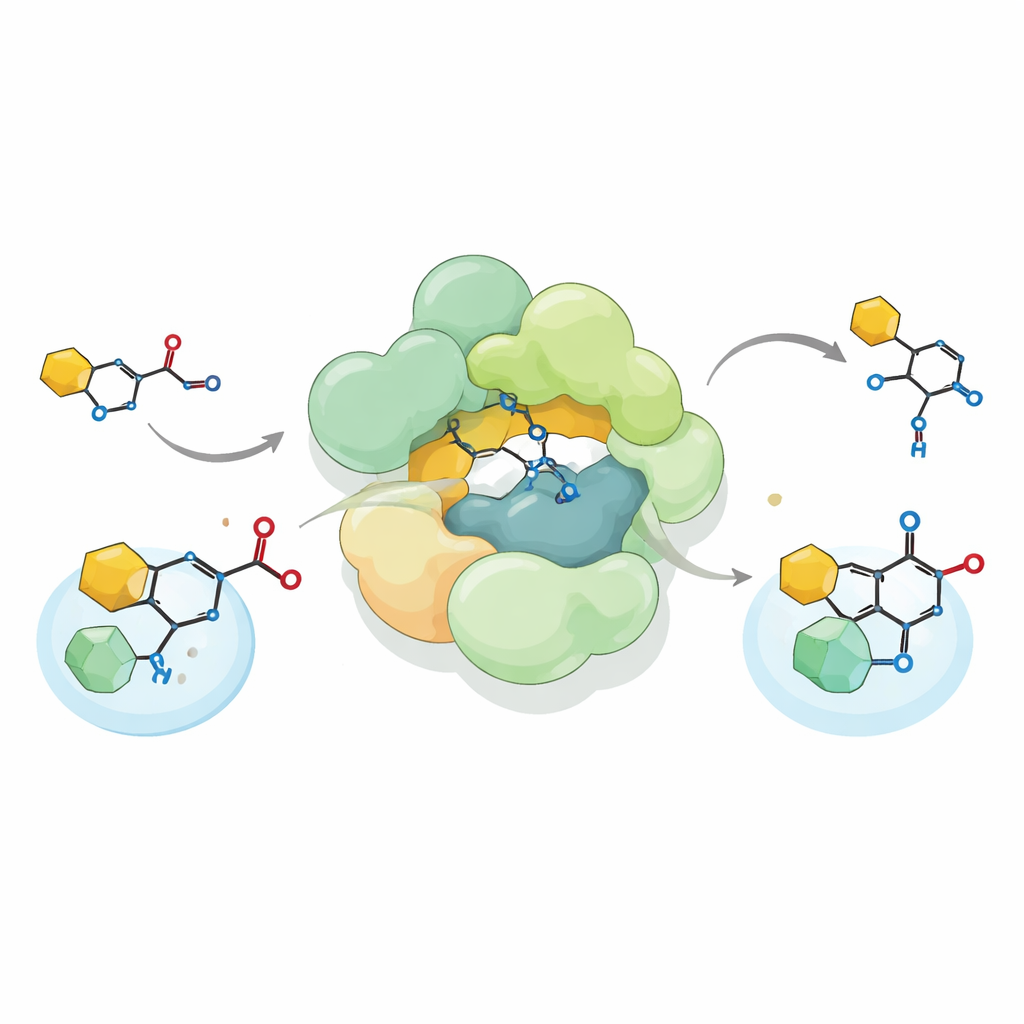
通过在实验室中重建该链球菌复合体并向其供给化学合成的重粘菌素A前体,研究者表明该复合体执行了一种不寻常的碳–碳键形成反应,即Friedel–Crafts C-酰基化。与许多将乙酰基连接到氧原子的酶不同,它直接将乙酰基安装到吡咯烷-2,4-二酮环的碳原子上——这是重粘菌素骨架的重要组成部分。该复合体既能接受天然的乙酰供体(如乙酰辅酶A),也能使用若干人工供体,甚至可以逆向运行该反应,断开其形成的键。这种灵活性扩展了已知生物酰基转移酶的功能谱,并暗示了如何将此类酶改造用于合成多样化的化学产物。
对保守蛋白骨架的再利用
研究团队使用高分辨率冷冻电镜解析了该链球菌复合体的三维结构,称为SmaATase。尽管功能已改变,SmaATase在整体结构上仍与参与异戊二烯脂类合成的甲羟戊酸通路中的古菌相关复合体有显著相似性。两者都是由重复模块构成的大型多聚体装配体,并具有一个共享腔室,辅因子CoA可以在活性位点之间结合并移动。然而,许多对原始代谢反应必不可少的催化残基在细菌版本中缺失或发生改变。生化测试证实SmaATase不再能合成祖先产物HMG-CoA,而是将乙酰辅酶A纯粹作为其新小分子底物的供体。
从代谢到抗生素的进化轨迹
为理解这种再利用如何演化,作者比对了多种细菌和古菌中相关复合体的序列与活性。他们鉴定出超过一千个含有同一三类酶的基因簇。有些仍支持经典的硫酮酶化学;另一些,如假单胞菌(Pseudomonas)中的基因簇,则参与合成不同的小分子抗生素。来自假单胞菌荧光假单胞菌(Pseudomonas fluorescens)的一个代表性复合体似乎处于这一路径的中间状态:其类HMGS结构域已失能,但类ACAT单元仍对CoA连接底物执行更常规的反应。在SmaATase及其产生作物保护化合物DAPG的假单胞菌同源体中,活性位点周围的进一步改变使这些酶能够识别非标准的受体,如芳香环或四氢吡咯酮(tetramic acid)核心。
为何一个微小的乙酰基能产生巨大差异
从生物学收益来看,这一分子改造的意义十分明确。当团队将乙酰化的抗生素重粘菌素A和DAPG对一系列革兰氏阳性菌进行测试时,这些分子表现出强烈的杀伤活性,而其未乙酰化的前体则弱得多或几乎无活性。正是这个被再利用的酶复合体在恰当位置放置的微小乙酰基,将原本平庸的骨架转变为强有力的武器,使口腔中的链球菌或植物根系附近的假单胞菌能够击败邻居。该研究展示了进化如何通过少量但策略性突变回收现有酶框架,将常规代谢机制转化为专门的化学防御工具——同时为工程师设计新的碳–碳键形成催化剂以应用于药物发现和合成生物学提供了蓝图。
引用: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
关键词: 酶进化, 天然产物生物合成, 抗生素化学, 代谢再利用, Friedel–Crafts 酰基化