Clear Sky Science · zh
用合成复制起始序列构建质粒
为何重写微生物 DNA 很重要
现代生物技术背后的许多工具,从胰岛素生产到前沿的基因电路,都依赖于被称为质粒的小型环状 DNA。这些遗传“马车”把工程化基因传递到细菌中,但它们的基本设计数十年来几乎未变。该研究显示,质粒的核心——告诉细胞何时以及以何频率复制质粒的序列——可以被完全重新设想。通过从头重建这个“拷贝引擎”,作者们创造了更易调节、组合和编程的质粒,为更灵活的诊断、生物制造和合成生物学打开了大门。
老工具的隐藏局限
质粒天然进化为可移动的 DNA,帮助细菌分享抗生素抗性或新的营养利用方式等性状。在实验室中,工程师借用这些质粒来携带有用基因,但大多数仍依赖 1980 年代发现的几种经典设计。这些老设计中隐藏着相互重叠的基因部件网络,这些部件控制每个细胞内质粒的拷贝数以及不同质粒是否能共存。由于这些部件是融合在一起的,改变一个特性可能会不可预测地破坏另一个。因此,科学家被局限于少量具有固定拷贝数和有限兼容性的质粒,限制了工程系统可达到的复杂度。
从头重建拷贝引擎
研究人员聚焦于广泛使用的 pMB1 质粒家族中的一个复制起始序列。在其天然形态中,该起始序列通过两种 RNA 之间微妙的对话来维持质粒数量——一种启动 DNA 复制,另一种将其关闭。研究团队首先对该系统进行了“重构”:拆分重叠基因,禁用一个埋藏的启动子,并将关键片段放到分离且简洁的遗传盒中。仅此一步就显示出,起始序列的核心功能可以在简化布局的同时得以保留,将一个由进化塑造的混乱部件转变为更像具有可访问组件的模块化机器。
替换为合成控制旋钮
在暴露原始控制逻辑后,作者用完全合成的调控元件替换了它们。他们将复制引物连到工程化的 RNA 开关上,这些开关像调光旋钮:小型控制 RNA 可以切换这些开关,允许或阻止引物的产生,从而控制质粒复制。通过选择不同的开关变体并与强度不同的启动子配对,他们将质粒拷贝数调节了超过两个数量级。他们还探索了控制盒在 DNA 上的不同物理布局,发现了一些能提高稳定性、并使复制区收缩为紧凑功能核心的排列,同时添加了防止质粒纠缠的天然辅助系统。
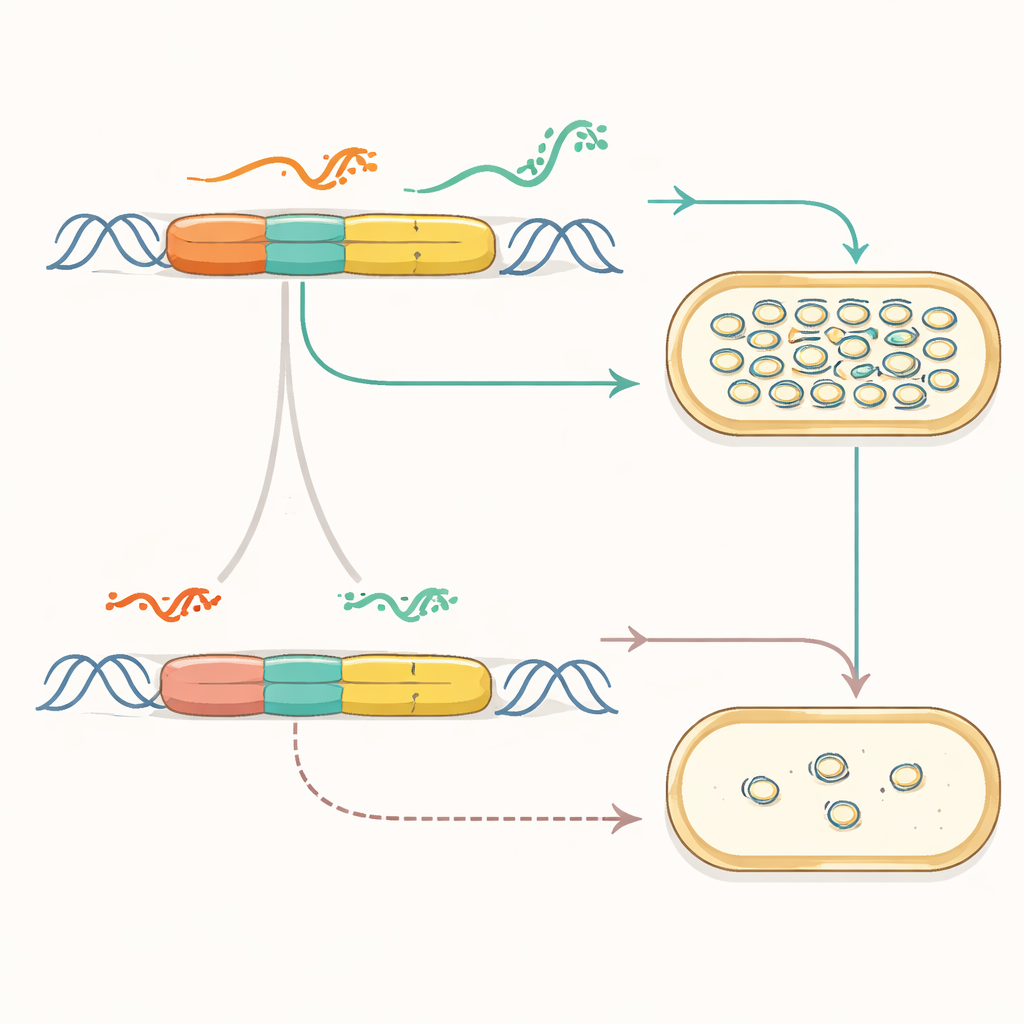
将化学信号转为 DNA 拷贝数
一旦拷贝引擎模块化,团队展示了它可以与外界传感连接。他们把合成起始序列接到可诱导启动子和称为核糖开关的 RNA 结构上,核糖开关会对小分子改变构象。在这些新质粒中,加入如 IPTG 或 cumate 之类的化学物质会导致质粒拷贝数——从而报告信号——上升或下降。多个信号可以组合使用,一个化学物质驱动复制而另一个抑制复制。研究者甚至构建了成对的质粒,每个响应不同化学物质,并使用 DNA 测序追踪它们在同一细胞中随时间变化的拷贝数,实际上将质粒计数变成了环境历史的条形码。
一种细胞内的多种定制质粒
该方法的一个关键测试是多个独立控制的质粒能否共存。借助一组正交 RNA 调控器,团队构建了六种不同的质粒,每种都有各自的合成起始序列和抗生素标记,并将这六种同时引入大肠杆菌(E. coli)。对全质粒的测序在几天内确认所有六种质粒都保持存在,尽管它们的相对丰度发生了变化。尝试用六种传统质粒做同样的实验则失败了,这凸显出重构设计和新增稳定系统使新质粒在同一细胞内拥挤时更具兼容性和鲁棒性。
对未来生物技术的意义
对非专业读者来说,结论很直接:作者们已将质粒从僵化的一刀切工具转变为可定制的平台。他们的合成复制起始序列像即插即用的引擎,其速度、灵敏度和输入可以按需选择。这使得构建将化学暴露记录为 DNA 拷贝数变化的细菌成为可能,通过将多条遗传通路分布到多个质粒上并行测试许多路径,或在工业菌株中精细平衡生长与产量成为可行方案。尽管仍存在一些稳定性权衡,这项工作表明质粒复制的核心机制已不再是工程禁区,为合成生物学创新开辟了新空间。
引用: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
关键词: 合成质粒, 复制起始序列, RNA 调控因子, 拷贝数控制, 合成生物学