Clear Sky Science · zh
PRMT3介导的禁食后翻译后适应调节代谢灵活性
为何进餐时间与体内燃料重要
许多人尝试禁食或限时进食以减重或改善血糖,但效果常常参差不齐。本研究深入代谢机制,试图解释原因。研究者以小鼠的腹部脂肪和人类样本为对象,发现了一个分子开关,帮助脂肪组织决定是燃烧还是储存燃料,并展示了进餐时间和一种药物如何将该开关翻向更利于健康的一侧。
脂肪中的可调节引擎
当身体能在禁食时燃烧脂肪、进食后燃烧糖类之间顺畅切换时,运作最佳。这种“代谢灵活性”在肥胖中常常丧失,使得应对能量供需波动变得困难。团队研究了内脏白色脂肪——与糖尿病和心脏病密切相关的深层腹部脂肪,发现蛋白质上的特定化学标记(称为甲基基团)会随进食与禁食而变化。在小鼠和人类中,两种此类标记(MMA和ADMA)在内脏脂肪中随体重和体质指数上升而积累,表明它们是代谢迟缓、适应性差的标志。
让代谢变僵化的进食信号
研究者聚焦于脂肪细胞中的一种酶PRMT3,它可添加这些甲基标记。在小鼠中,内脏脂肪的PRMT3水平在夜间(动物进食时)升高,在白天(禁食时)下降,与MMA和ADMA的变化紧密同步。这一节律依赖于胰岛素和一个关键信号蛋白AKT:当食物或注射胰岛素激活AKT时,PRMT3被开启并更强地修饰,进而增加被甲基化的蛋白数量。阻断AKT或直接抑制PRMT3会迅速抑制这一甲基化信号,甚至能模拟更长时间禁食的效果。
将脂肪细胞从储存改为燃烧
这些化学标记究竟有何作用?研究表明,PRMT3稳定线粒体中的一款转运蛋白SLC25A1——线粒体是细胞的能量工厂。SLC25A1将柠檬酸(一种关键代谢中间体)从线粒体运出到细胞质,供脂肪合成使用。PRMT3在SLC25A1的两个特定位点甲基化精氨酸,使该转运蛋白更稳定,促进柠檬酸外运与脂肪合成。当PRMT3被抑制时,SLC25A1水平下降,柠檬酸外运减少,脂肪细胞转向分解糖类而非合成更多脂肪。在高脂饮食小鼠中,抑制PRMT3的药物降低了体脂、改善了血糖控制,并提高了呼吸商(respiratory exchange ratio),显示动物更容易切换到燃烧碳水化合物。
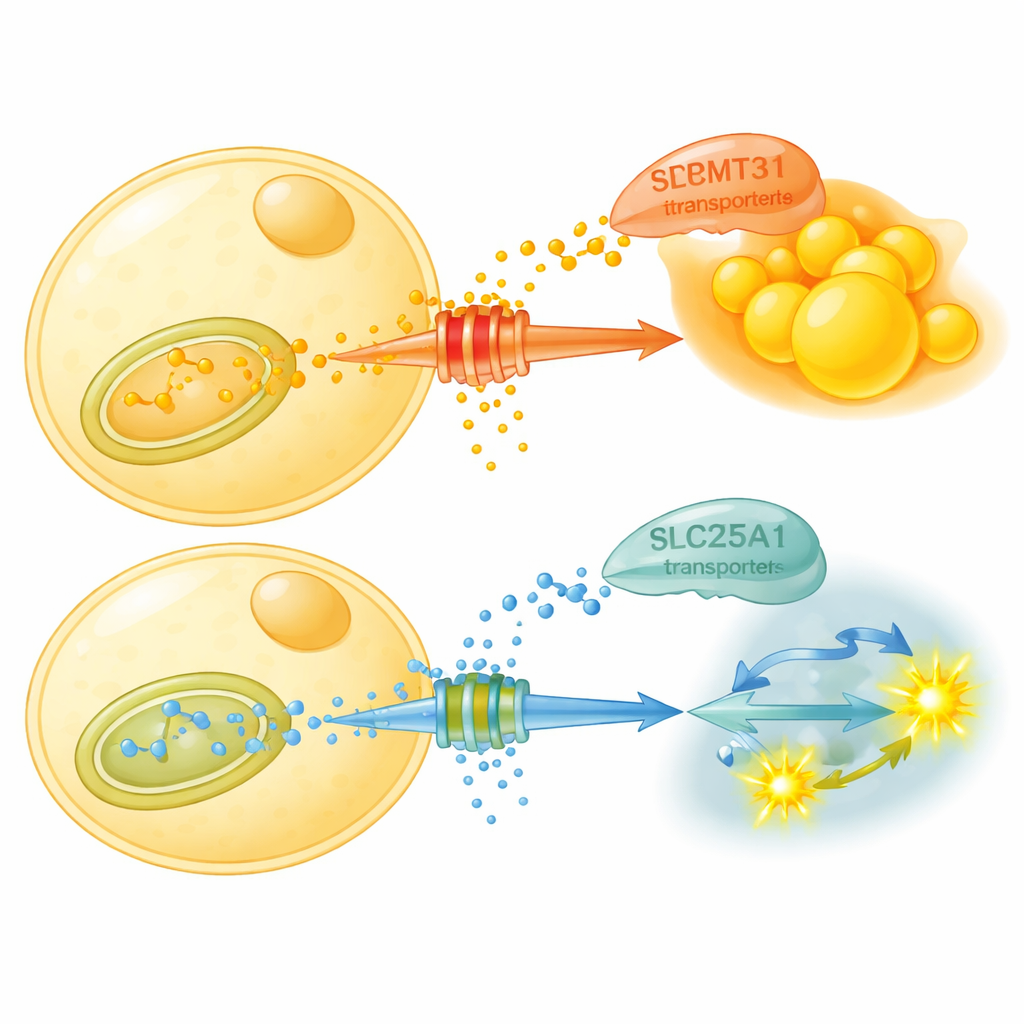
禁食时间表与基因改造指向同一路径
研究者接着询问常见的禁食模式是否也通过这一相同开关起作用。在16:8限时进食(16小时禁食、8小时进食)下,小鼠在不减少总食量的情况下体重下降并更好地处理葡萄糖。它们的内脏脂肪中PRMT3、SLC25A1和甲基化蛋白水平均降低,燃料使用变得更灵活,尤其在夜间(通常进食时)表现明显。值得注意的是,在特定时间给予抑制PRMT3的药物可以产生许多与16:8相似的益处。仅在脂肪细胞中基因性删除SLC25A1也能保护小鼠免受饮食引起的高血糖和脂肪肝,机制同样是通过增强脂肪中糖类分解和能量消耗,即便脂肪量并未明显减少。
对未来疗法的意义
综上,研究结果表明深层腹部脂肪存在一个对时间敏感的开关,由胰岛素、AKT、PRMT3和SLC25A1控制,决定我们的身体是保持代谢灵活还是陷入储存模式。限时进食似乎通过降低PRMT3及其下游效应将该开关推向灵活一侧。抑制PRMT3的药物能在肥胖小鼠中复制许多这种益处,提示未来可能出现一种将禁食代谢益处更易获得的药物。对普通读者而言,重要信息是:何时进食——而不仅仅是吃什么——可以重塑脂肪组织处理燃料的方式,对体重、血糖和长期健康有重要影响。
引用: Huang, Z., Liu, X., Chen, X. et al. PRMT3-mediated post-translational adaptation to fasting regulates metabolic flexibility. Nat Commun 17, 2264 (2026). https://doi.org/10.1038/s41467-026-68883-6
关键词: 代谢灵活性, 限时进食, 内脏脂肪, 蛋白质甲基化, 葡萄糖代谢