Clear Sky Science · zh
一种基于DNA的纳米装置感知嘌呤能信号并推动免疫开关以消除炎症
降低机体的警报系统
当我们的组织受损时,细胞会释放一阵化学“警报信号”,招募免疫细胞来对抗感染并清除碎片。这种反应至关重要,但如果警报声过于响亮或持续过久,就可能在肺、肾等器官中引发有害的炎症。本研究描述了一种微小的、可编程的基于DNA的装置,它能感知警报信号何时过强并悄然将其调低,帮助免疫系统从攻击模式切换到修复模式。
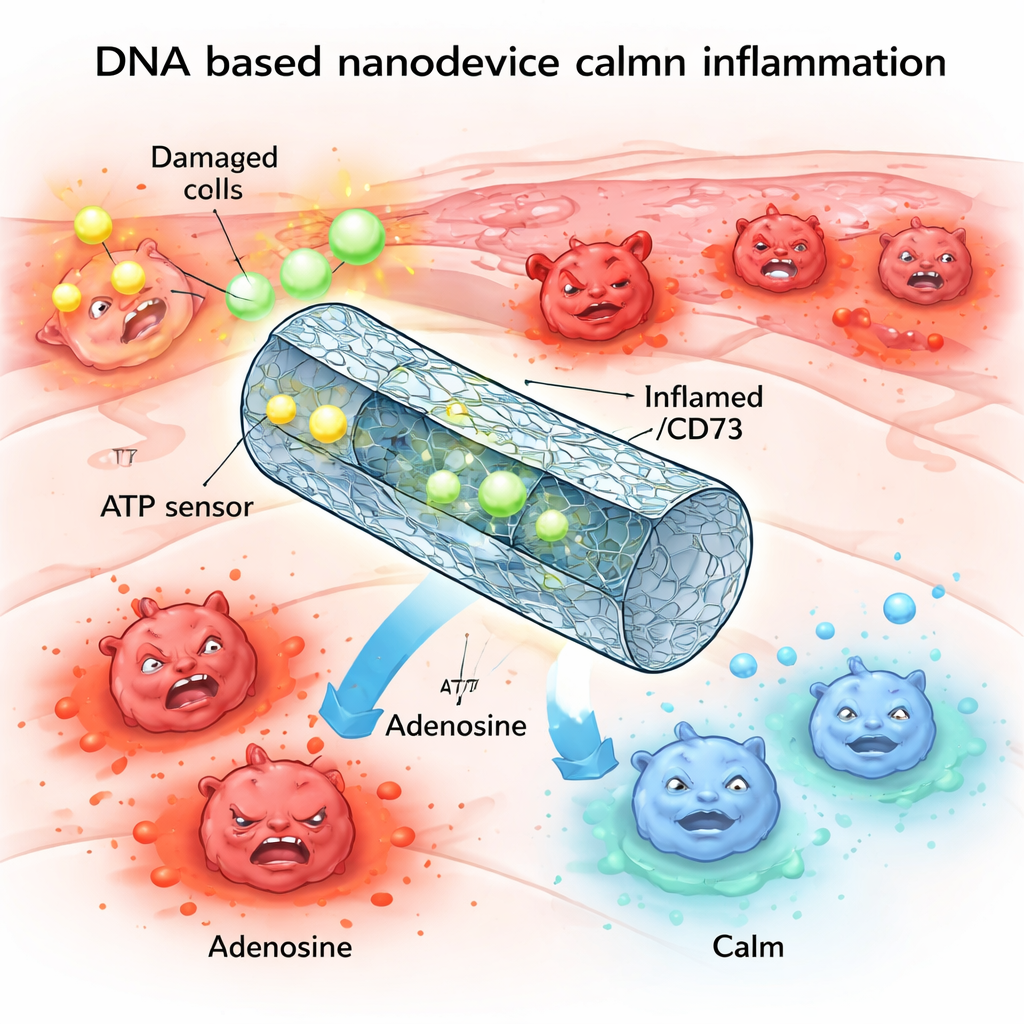
可能失控的化学警报
机体的一种关键警报分子是ATP,通常被认为是细胞内的“能量货币”。在损伤或应激时,大量ATP从受损细胞中泄出到周围空间。在细胞外,这些ATP作为求救信号,结合免疫细胞表面的受体并将其推向高度炎症的状态。在健康条件下,细胞表面的酶会迅速将多余的ATP分解成腺苷,这是一种具有镇静、抗炎作用的相关分子。但在许多慢性或严重的炎症性疾病中,这一分解机制受损,导致ATP水平升高、腺苷降低,组织陷入反复损伤的循环。
构建智能DNA管
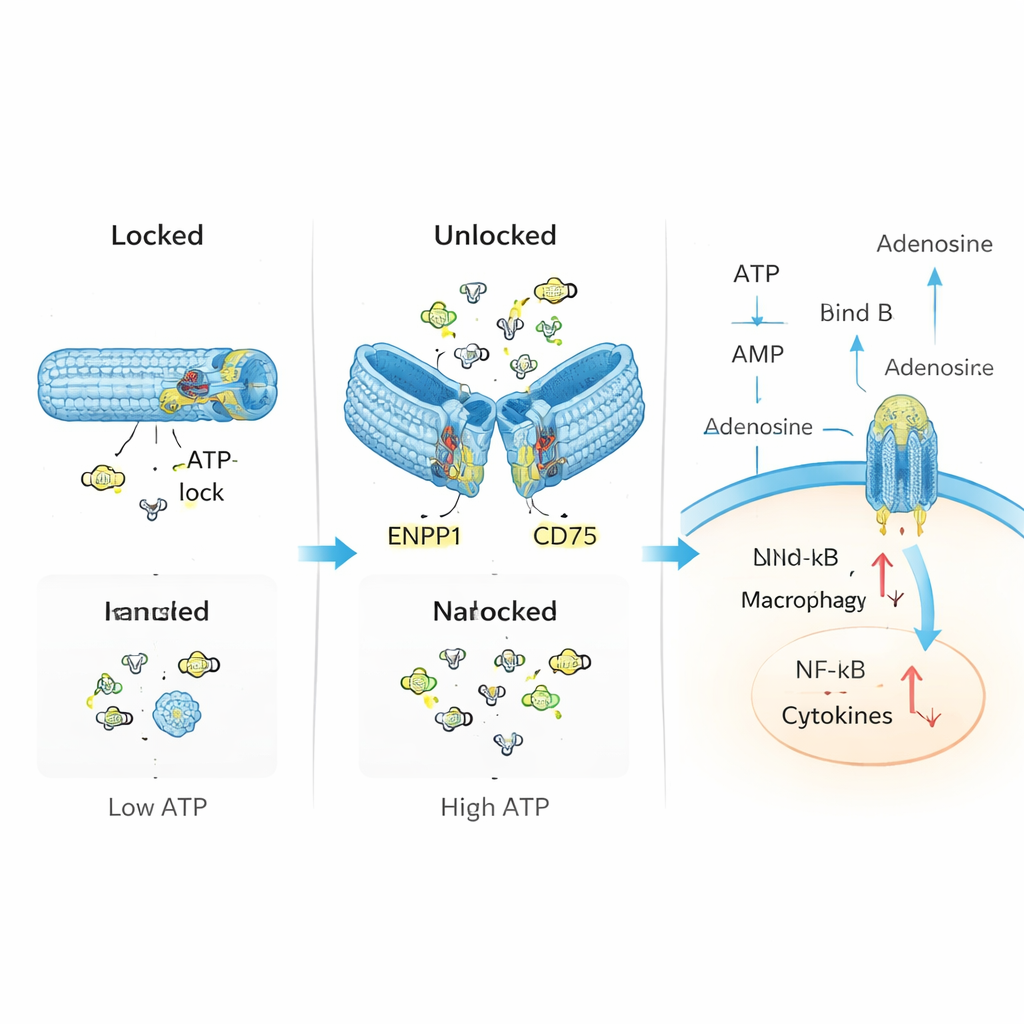
研究人员着手用DNA纳米技术模仿并修复这一天然控制系统。他们用DNA折叠出一个空心管,类似折纸,并配备了两个主要部件:“传感器”用于识别ATP,以及将ATP转化为腺苷的酶。在静息、锁定状态下,管由充当ATP传感器的短DNA片段保持关闭。当ATP水平升高超过受损组织典型的阈值时,ATP与这些片段结合,促使管打开并露出内部的ENPP1和CD73酶。随后这些酶分解多余的ATP并生成腺苷,温和地将局部化学平衡从危险信号移向消除状态。
验证开关的有效性
在受控的体外实验中,团队证实他们的DNA管在低ATP水平时保持关闭,而在ATP丰富时可靠打开,类似一个紧急阀。一旦解锁,该器件持续地将ATP转化为中间产物并最终生成腺苷,同时并未显著损害酶的活性。在暴露于高ATP的免疫细胞中,该纳米装置降低了线粒体中的有毒副产物,减弱了诸如NF-κB和NLRP3炎性小体等炎症通路的激活,并增强了与腺苷镇静作用相关的信号。换言之,该装置不仅清除ATP,还主动重塑细胞的行为,使之从炎症性转为调节性。
搭乘至受伤部位
设计一个智能开关是一回事,把它送到机体的正确位置又是另一回事。为了解决递送问题,研究人员将DNA管附着到循环单核细胞表面,这是一种天然会定向到炎症组织的白细胞。他们使用带胆固醇连接的DNA锚,将大量纳米装置“停靠”在每个细胞膜上,这些装置大多停留在表面而非被细胞吞噬。在急性肺和肾损伤的小鼠模型中,与游离装置相比,这些被装饰的单核细胞在受损器官的积累效率更高,且纳米装置仍能特异性响应受损组织中的高ATP。
帮助组织愈合
在化学诱导的肺或肾损伤小鼠中,用DNA装置治疗可减少组织损伤、免疫细胞积聚和炎性信使分子的水平。携带纳米装置的单核细胞效果最好,其保护作用优于游离装置或单独使用酶。对肺组织的深入基因和代谢分析表明,这一方法不仅抑制了炎症基因,还帮助恢复细胞中受扰的能量代谢。重要的是,装置表现出低毒性,在健康动物中未触发有害的免疫反应。
这对未来疗法的重要性
对非专业读者来说,关键信息是:这项工作展示了一种可编程的、分子级的“温控器”来调节炎症。由DNA和天然酶构成的纳米装置能够感知危险信号何时过强并自动将其转换为平静信号,帮助免疫细胞平息并促使组织修复。尽管仍处于早期实验阶段,这一策略暗示了一类新型治疗方法——它们并非在全身范围内简单阻断免疫通路,而是在受伤部位局部重建化学信号的平衡,可能为多种疾病中的有害炎症提供更精确的控制。
引用: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
关键词: DNA纳米装置, 细胞外ATP, 炎症, 腺苷信号, 纳米医学