Clear Sky Science · zh
Olig2 在体内星形胶质细胞向神经元转化中充当一种可诱导的屏障
将大脑的支持细胞转变为神经元
成年大脑替代丢失神经元的能力有限,这在中风、阿尔茨海默病和脊髓损伤等疾病中是一个主要障碍。一个有前景的思路是通过基因治疗,直接将邻近的“支持细胞”——星形胶质细胞——转化为新的神经元。本研究提出了一个关键问题:是什么阻碍了在活体大脑中高效实现这种转化?是否可以松开这些制动?
细胞变化中的隐藏刹车
星形胶质细胞通常有助于为神经元提供营养、维持脑内化学平衡并在受伤时做出反应。在某些疾病状态下,它们会表现出类似干细胞的特征,因此有人希望能够在原位将其重编程为神经元。科学家已经知道,一类称为易神经元转录因子的基因——例如 Ngn2、Ascl1 和 NeuroD1——可以推动星形胶质细胞向神经元谱系转变。然而在动物体内,这种星形胶质细胞向神经元的转化仍然令人沮丧地低效。作者怀疑,除了已存在的防御机制外,当触发重编程时,星形胶质细胞可能会启动一种新的、可诱导的屏障。
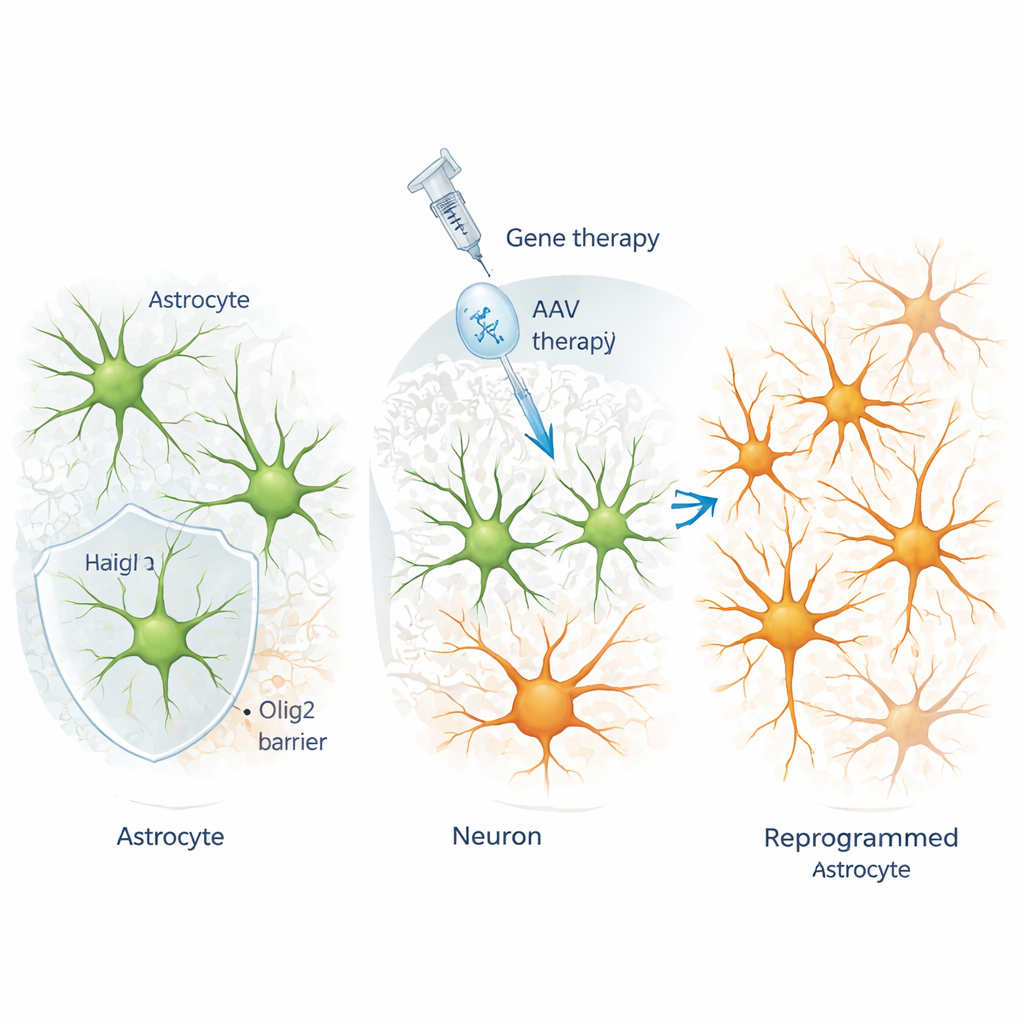
一种名为 Olig2 的蛋白介入以抵制改变
研究人员在成年小鼠皮层中工作,使用对星形胶质细胞高度选择性的工程病毒将重编程因子递送至这些细胞。他们发现,每当将基本螺旋-环-螺旋(bHLH)因子如 Ngn2、Ascl1 或 NeuroD1 强制表达于星形胶质细胞时,另一种 bHLH 蛋白 Olig2 会被显著诱导。在正常情况下,Olig2 存在于少突胶质细胞谱系中,而不在成熟的皮层星形胶质细胞中。仔细的追踪实验显示,处理后新增的 Olig2 阳性细胞并非由少突前体细胞增殖产生——相反,正被靶向以进行转化的那些星形胶质细胞在响应重编程信号时自身开启了 Olig2 表达。
去除刹车使转化率增加三倍并产生功能性神经元
为了检验 Olig2 是否真的是一个屏障,团队使用短发夹 RNA(shRNA)在同时给予 Ngn2 的星形胶质细胞中特异性下调 Olig2。沉默 Olig2 将这些细胞中的蛋白水平几乎降至零,并产生了显著效果:被标记的星形胶质细胞转变为神经元的比例相比仅给予 Ngn2 时大约提高了三倍。在数周内,许多细胞经历了一个中间阶段,先失去典型的星形胶质细胞标志物,然后完全获得神经元标志物。来自脑切片的电生理记录显示,转化细胞能够发放动作电位,并且在约半数情况下接收到兴奋性和抑制性突触输入——这些都是功能性整合入局部回路的标志。
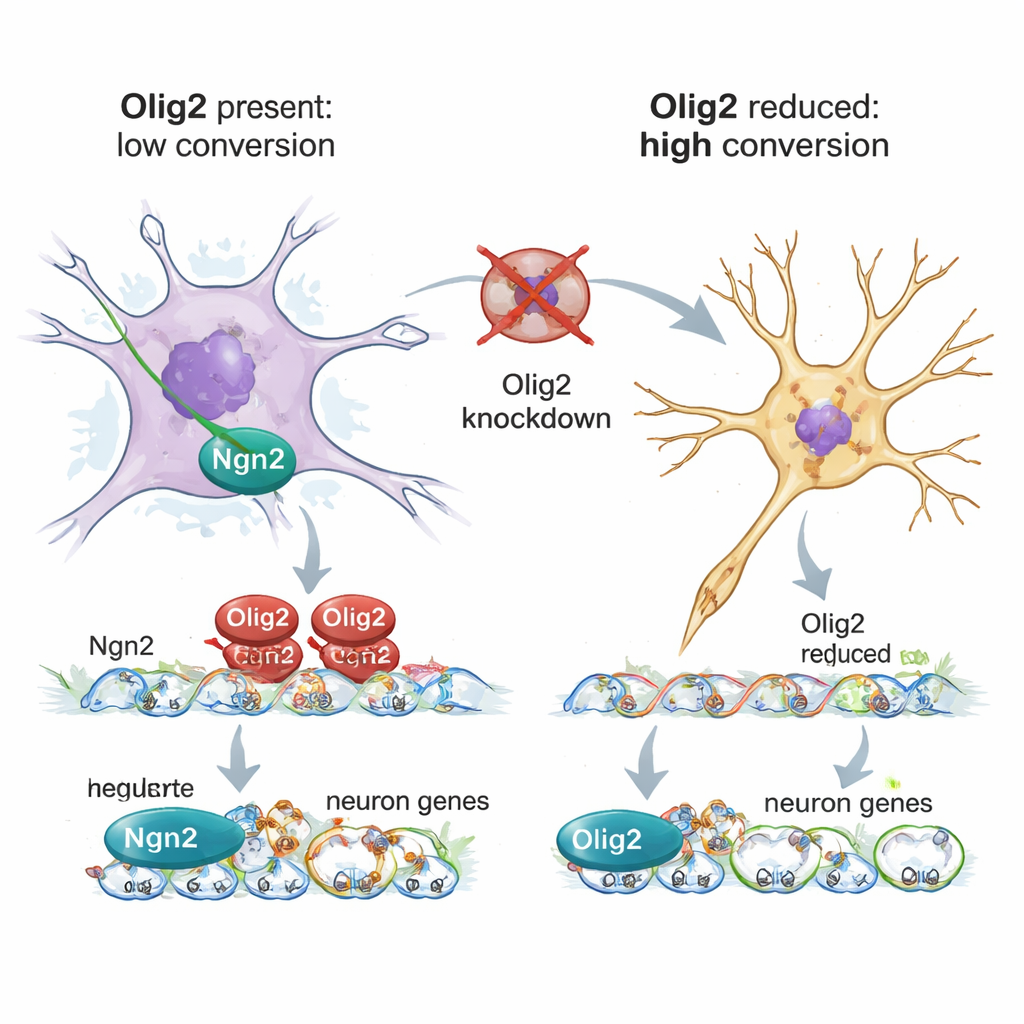
Olig2 如何阻断转向神经元程序
作者使用单细胞 RNA 测序对数千个暴露于 Ngn2 的单个星形胶质细胞进行了谱系分析,比较有无 Olig2 下调的情况。当 Olig2 存在时,星形胶质细胞的基因表达仅部分转变:一些代谢和蛋白合成通路发生改变,但核心的星形胶质细胞基因仍然活跃,许多构建神经元的基因仍然被抑制。当 Olig2 被减少时,星形胶质细胞更完全地压制了其成熟支持细胞程序,并上调了与神经干细胞、神经发生和轴突生长相关的基因。一种补充方法 CUT&Tag 映射了 Olig2 在这些重编程星形胶质细胞的 DNA 上的结合位点。Olig2 定位于许多促神经基因的调控区——包括 Ngn2 本身——这与其作为直接压制子、既抑制重编程因子又保持神经元基因不被激活的角色相一致。
通过解除可诱导的防御来改写细胞身份
总之,这项工作表明,星形胶质细胞对被转变为神经元会启动一种主动的、可诱导的防御:一旦引入像 Ngn2 这样的易神经元因子,它会触发 Olig2,而 Olig2 随后抑制 Ngn2 并阻断关键的神经元基因。禁用 Olig2 并不能解决所有问题——转化效率仍然适中——但它显著提高了功能性新生神经元的产量,并将星形胶质细胞的代谢与基因表达朝向类神经元状态转变。对非专业读者而言,结论是成功的大脑修复可能不仅需要通过促神经因子踩油门,还需要释放像 Olig2 这样的新发现的刹车,细胞用它们来保护自身身份。
引用: Lai, C., Hou, K., Li, W. et al. Olig2 acts as an inducible barrier to in vivo astrocyte-to-neuron conversion. Nat Commun 17, 2033 (2026). https://doi.org/10.1038/s41467-026-68869-4
关键词: 星形胶质细胞向神经元的转化, 细胞重编程, Olig2, 基因治疗, 神经再生