Clear Sky Science · zh
NKG2D上调使肿瘤对联合抗PD1和抗VEGF治疗更为敏感并预防听力丧失
这项研究对听力受损人群的重要性
一些人遗传有称为NF2相关鞘瘤病的疾病,导致良性肿瘤在内耳神经上生长,并常引起逐渐且不可逆的听力丧失。现有治疗可以缩小肿瘤,但可能损害听力或随时间失去疗效。本研究探索了一种新药物组合,在实验模型中不仅减缓肿瘤生长,还帮助保护听力,指向对患者更温和且疗效更持久的治疗选择。
理解导致沉默的肿瘤
在NF2相关鞘瘤病中,称为前庭神经鞘瘤的肿瘤在颅内负责平衡和听觉的神经上形成。随着这些肿瘤增大,它们会损伤将声音信号传递到大脑的细小神经纤维,在严重情况下还可压迫脑干。外科和放疗可以挽救生命并去除或控制肿瘤,但二者均存在真实风险:听力恶化、眩晕和面神经无力。一种名为贝伐单抗的药物,通过阻断血管生长信号(VEGF)有时可缩小这些肿瘤并改善听力,然而只有大约三分之一的患者受益且效果常会消退。这促使人们寻找既更安全又更持久的疗法。
将免疫系统拉来做同盟
过去十年,免疫检查点抑制剂——能释放免疫细胞“刹车”以更有效攻击肿瘤的药物——改变了癌症治疗。其中一种“刹车”PD-1位于免疫细胞表面,一旦被激活就能抑制其功能。作者探讨阻断PD-1(使用抗PD1抗体)是否能帮助免疫系统控制前庭神经鞘瘤,以及将其与抗VEGF疗法联合是否会更有效。研究者使用与人类内耳和周围神经肿瘤高度相似的小鼠模型,给予单独抗VEGF、单独抗PD1或两者联合治疗,然后跟踪肿瘤生长、生存和听力情况。
让肿瘤血管更好地工作,而非消失
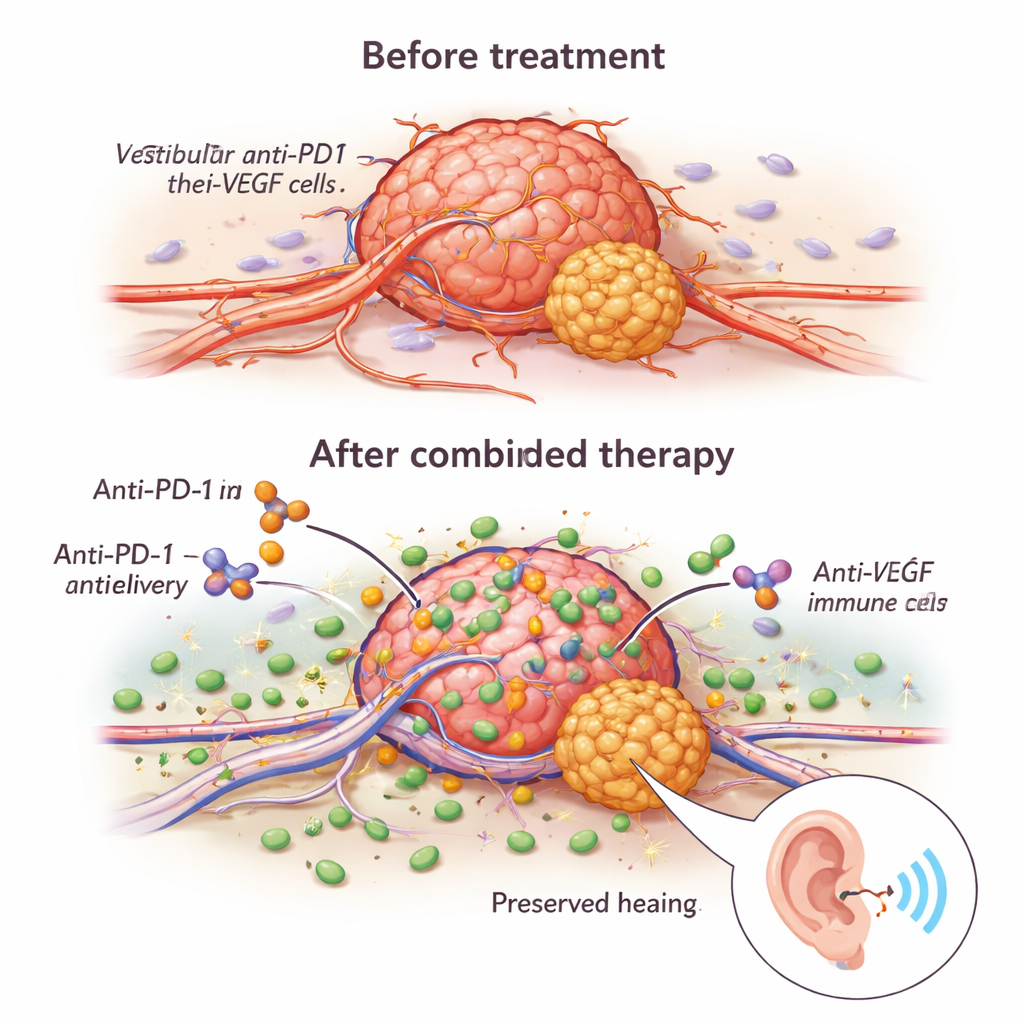
研究团队发现,抗VEGF的作用不仅仅是饿死肿瘤。它使肿瘤中异常、渗漏的血管重塑为更稳定、功能更佳的通道。在显微镜下,接受治疗的肿瘤显示更多被支持细胞覆盖的血管,以及更大比例真正输送血液的血管。这种“正常化”改善了抗PD1抗体进入肿瘤的能力,并允许更多抗癌免疫细胞——尤其是CD8 T细胞和自然杀伤(NK)细胞——进入。在接受联合治疗的小鼠中,肿瘤生长更慢,分裂的细胞更少,处于程序性死亡的细胞更多,且动物的生存期比单用任一药物更长。
增强免疫细胞的杀伤力
联合治疗的益处不仅在于将更多免疫细胞引入肿瘤;这些细胞到达后也更具攻击性。抗VEGF治疗增加了诸如颗粒酶B和穿孔素等分子的存在,这些分子是免疫系统刺穿肿瘤细胞的“子弹”。这一过程中一个关键开关是名为NKG2D的受体,存在于T细胞和NK细胞上。抗VEGF提高了NKG2D及其配对分子在肿瘤细胞上的表达,使免疫细胞在体外试验中更有效地杀伤肿瘤细胞。当研究者阻断NKG2D时,治疗的抗肿瘤效应显著下降,表明该通路对药物协同至关重要。重要的是,接受长期贝伐单抗治疗的人类肿瘤小样本显示的基因活动模式,亦与T细胞和NK细胞更活化、较少“耗竭”的表型一致,提示类似的免疫增强也可能在患者体内发生。
在控制肿瘤的同时保护听力
一个关键问题是这些基于免疫的治疗是否会损害或改善听力。当健康小鼠单独接受抗PD1时,它们的听力阈值保持正常,表明该药物不会对听觉系统造成短期损害。在带瘤小鼠中,单独抗VEGF与无治疗相比改善了听力,与临床观察一致。单独抗PD1以及抗PD1与抗VEGF的联合治疗都将听力阈值恢复到接近正常水平。当研究者模拟真实情形——先用抗VEGF治疗肿瘤,然后选择继续、停用或加入抗PD1时,他们发现改用抗PD1仍可减缓肿瘤生长,但停用抗VEGF会失去其对听力的益处。维持抗VEGF并加入抗PD1在生存和听力保护两方面给出了最佳结果。
这对患者可能意味着什么
对于生活在NF2相关鞘瘤病中的人群,这项工作表明未来的治疗或许不再只是控制肿瘤,它还可能保护听力。在精心设计的小鼠模型中,阻断VEGF与阻断PD-1的联合创造了对免疫细胞更友好的环境,通过NKG2D放大了它们的肿瘤杀伤力,并比任一单独方法更好地保护了听力。尽管仍需临床试验来确认在人类中的安全性和获益,这项研究为将这一药物组合作为管理前庭神经鞘瘤并预防听力丧失的一种潜在更持久策略,提供了清晰的试验路线图。
引用: Lu, S., Yin, Z., Wu, L. et al. NKG2D upregulation sensitizes tumors to combined anti-PD1 and anti-VEGF therapy and prevents hearing loss. Nat Commun 17, 1148 (2026). https://doi.org/10.1038/s41467-026-68865-8
关键词: 前庭神经鞘瘤, NF2, 免疫疗法, 贝伐单抗, 听力保护