Clear Sky Science · zh
病毒模拟在结肠炎中起到肿瘤抑制作用
与癌症作斗争的隐匿 DNA
在我们 DNA 的深处存在大段曾被称为“垃圾”的序列。这项研究表明,其中一部分隐匿的遗传物质实际上可以帮助慢性肠道炎症患者避免发生结肠癌。通过在细胞内模拟假病毒感染,这些 DNA 元件触发一种内部警报系统,从而抑制有潜在致癌风险的干细胞。
可以被唤醒的沉睡 DNA
近一半的人类基因组由称为转座子(重复序列)的片段构成——这些 DNA 片段能够复制并移动。在健康细胞中,这些元件被诸如 DNA 甲基化之类的化学标记严密压制以保持沉默。但在某些疾病状态或经某些抗癌药物处理后,这些元件可能被重新激活。激活后它们会产生异常的双链 RNA,在细胞看来很像来自病毒的遗传物质。
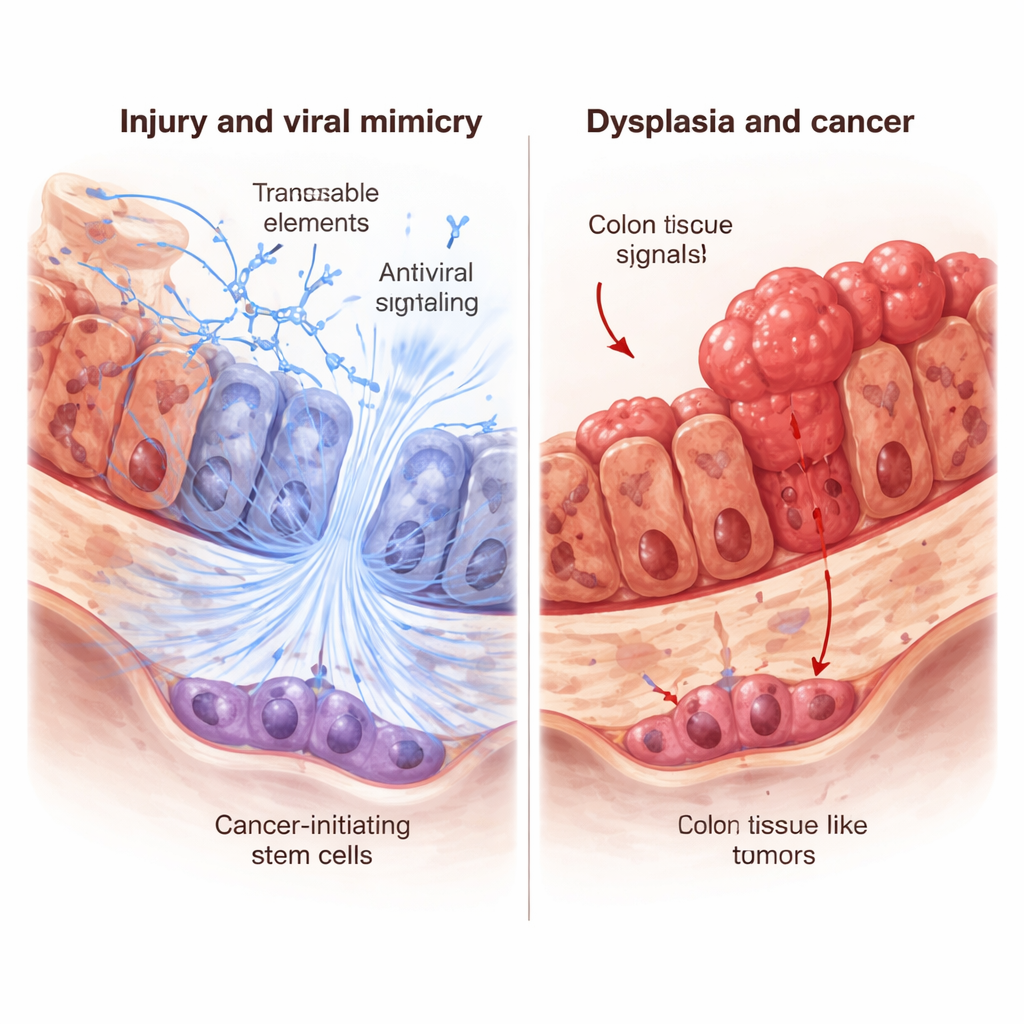
发炎肠道中的假病毒警报
研究人员检查了炎症性肠病(IBD)患者的结肠组织以及实验性结肠炎小鼠的组织。在人和鼠中,活动性炎症都与转座子活性增高和干扰素基因更强的激活相关——干扰素是机体抗病毒警报系统的一部分,这一现象被称为病毒模拟。然而,当他们观察长期 IBD 已进展为不典型增生(癌前病变)或结肠癌的患者时,发现相反的模式:转座子和干扰素相关基因的表达都被降低。这提示关掉病毒模拟反应可能是从慢性炎症到癌变的一个步骤。
降低 DNA 甲基化以阻断肿瘤
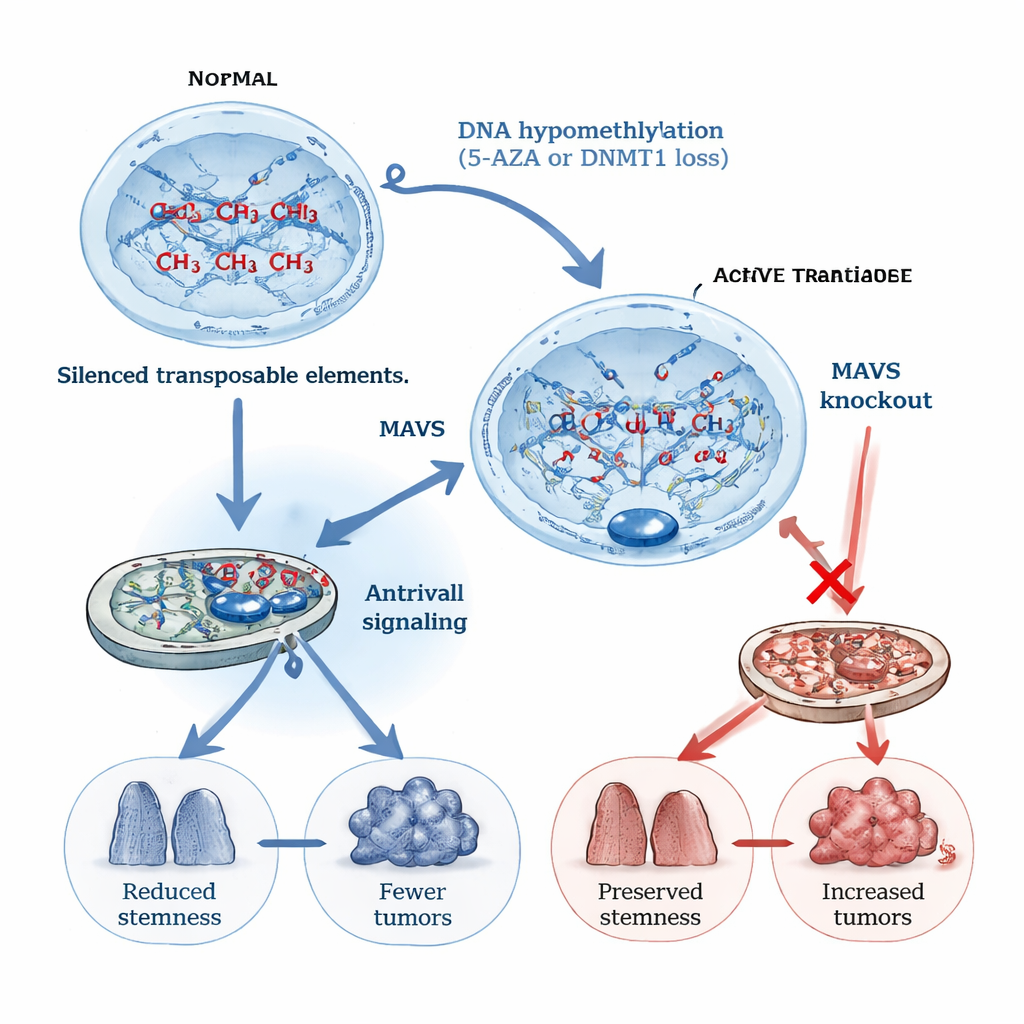
为检验增强这种假病毒警报是否真的能阻止癌症形成,团队采用了两种在结肠中降低 DNA 甲基化的方法。一种是已用于某些血液恶性肿瘤的药物 5‑AZA;另一种是在特定罕见的 DCLK1 阳性细胞中有针对性地删除维持 DNA 甲基化的关键酶 DNMT1,这类细胞可作为致癌起始干细胞。在由化学损伤与炎症共同驱动的结肠癌小鼠模型中,5‑AZA 处理和 DNMT1 缺失均导致肿瘤数量减少,且在部分情况下肿瘤体积也更小。这些变化伴随着广泛的 DNA 去甲基化、多类转座子强烈再激活,以及增强的干扰素与 JAK/STAT 信号通路,证实了病毒模拟被触发。
解除警报释放出致癌起始细胞
抗病毒蛋白 MAVS 位于线粒体上,是将细胞内病毒 RNA 传感器信号传递下去的关键。作者展示了在小鼠中敲除 MAVS 消除了 5‑AZA 和 DNMT1 缺失带来的肿瘤抑制效应:肿瘤数量增加,生存率下降。在体外培养的小型结肠组织(类器官)中,通过 DNA 去甲基化激活病毒模拟显著降低了带有 APC 突变的 DCLK1 细胞作为干细胞形成新类器官的能力。去除 MAVS 则逆转了这一抑制,即使在 DNA 去甲基化时,这些细胞也恢复了干细胞样行为与生长。这些实验表明,病毒模拟能以细胞自主的方式抑制致癌干性,而无需肿瘤周围免疫细胞的参与。
这对患者意味着什么
对于长期患结肠炎的人来说,结肠癌的风险令人担忧。这项工作表明,机体的一部分天然防御是由唤醒的转座子产生的内部“病毒警报”。当该警报活跃时,它限制受损细胞发展成真正的癌症干细胞;当警报被关闭时,肿瘤更容易发生。通过靶向 DNA 甲基化或其调控因子,谨慎地增强病毒模拟的疗法或许有一天可以帮助预防或治疗结肠癌,尤其是对那些长期患炎且高风险的患者。
引用: Larsen, F., Jeong, W., Schep, D. et al. Viral mimicry acts as a tumor suppressor in colitis. Nat Commun 17, 1313 (2026). https://doi.org/10.1038/s41467-026-68850-1
关键词: 病毒模拟, 结肠炎, 结肠癌, 转座子, DNA 甲基化