Clear Sky Science · zh
通过核质移位从死亡细胞提取核 DNA 并激发 cGAS-IFN-I 反应
我们的免疫系统如何“读取”来自死去细胞的 DNA
当细胞在感染、癌症或日常磨损中死亡时,其残骸必须被清理而不引发过度炎症。本文揭示了一种令人意外的方式:免疫细胞能够实质性地深入死亡细胞的细胞核,提取其 DNA,并将其作为危险信号加以利用。理解这一隐蔽的清理与警报系统,可能改变我们对抗病毒药物、自身免疫、癌症治疗和药物副作用的看法。
存在于免疫细胞内的隐匿 DNA 报警系统
我们的细胞内含有一种名为 cGAS 的感应器,它能检测位于不该出现的位置的 DNA——即漂浮在细胞浆中而非安全地封装在细胞核或线粒体中。当 cGAS 遇到此类 DNA 时,会启动强烈的报警程序,产生 I 型干扰素,这些蛋白质在抗病毒和免疫调节中至关重要。科研人员早已知道病毒可以将其遗传物质传入细胞触发该通路,我们自身的 DNA 片段有时也会泄露并引起自身免疫疾病。但有一个基本谜题仍然存在:大量来自自身的 DNA,尤其是来自死亡细胞的 DNA,是如何到达 cGAS 而不被细胞内的“胃”——溶酶体消化掉的?
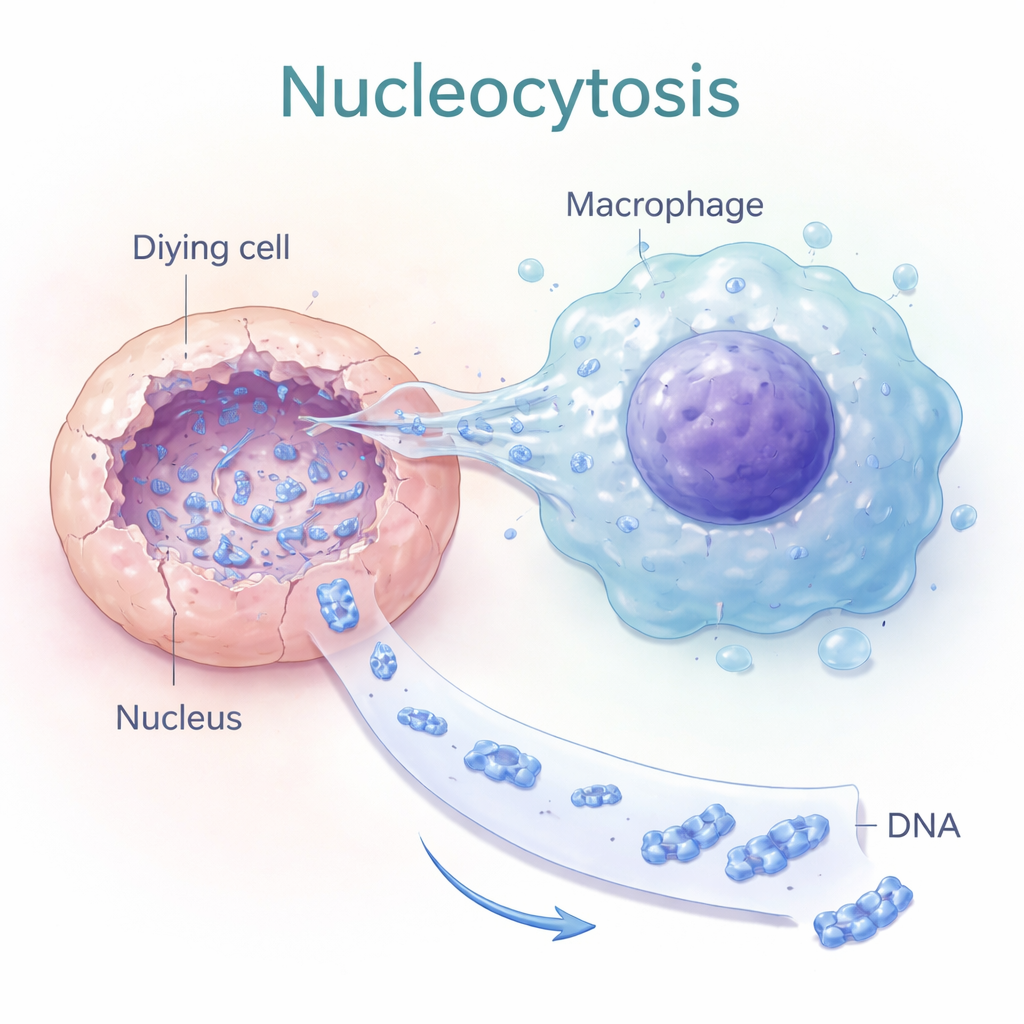
核质移位:向死亡细胞核内打洞提取 DNA
作者发现了一种他们称之为“核质移位”的过程,其中某些巨噬细胞——这类免疫细胞通常负责吞噬碎片——采取了更为定向的行为。它们并不是整体吞噬死亡细胞,而是伸出细长、指状的突起直接进入正在死亡细胞的细胞核。活细胞成像显示,死亡细胞核内的 DNA 强度下降,而与之相连的巨噬细胞内 DNA 强度上升,表明存在主动的核 DNA 提取。该转移依赖于细胞的内骨架(肌动蛋白)和控制细胞形状的信号分子,提示核质移位是一种有目的的机械行为,而非被动泄漏。
抗病毒药物何时会触发 DNA 报警
在 COVID-19 大流行期间,羟氯喹等药物曾被广泛测试作为抗病毒药物,但它们在体内的精确作用机制仍不清晰。研究者发现,羟氯喹及若干相关的“阳离子两亲”药物能够强烈激活 cGAS–STING–干扰素通路——但仅在一部分巨噬细胞中。此类药物通过升高溶酶体 pH 并抑制一种名为 PPT1 的酶(该酶帮助分解蛋白上的脂肪标签)来扰乱溶酶体。综合作用把部分细胞推入一种特殊的死亡形式,在这种情况下,名为钙网蛋白(calreticulin)的蛋白在细胞核中积累。随后,巨噬细胞更倾向于向这些富含钙网蛋白的细胞核伸出突起,通过核质移位提取 DNA,并在少数细胞中引发强烈的干扰素产生——足以形成强烈的局部抗病毒信号,而不会将其扩散到全身。
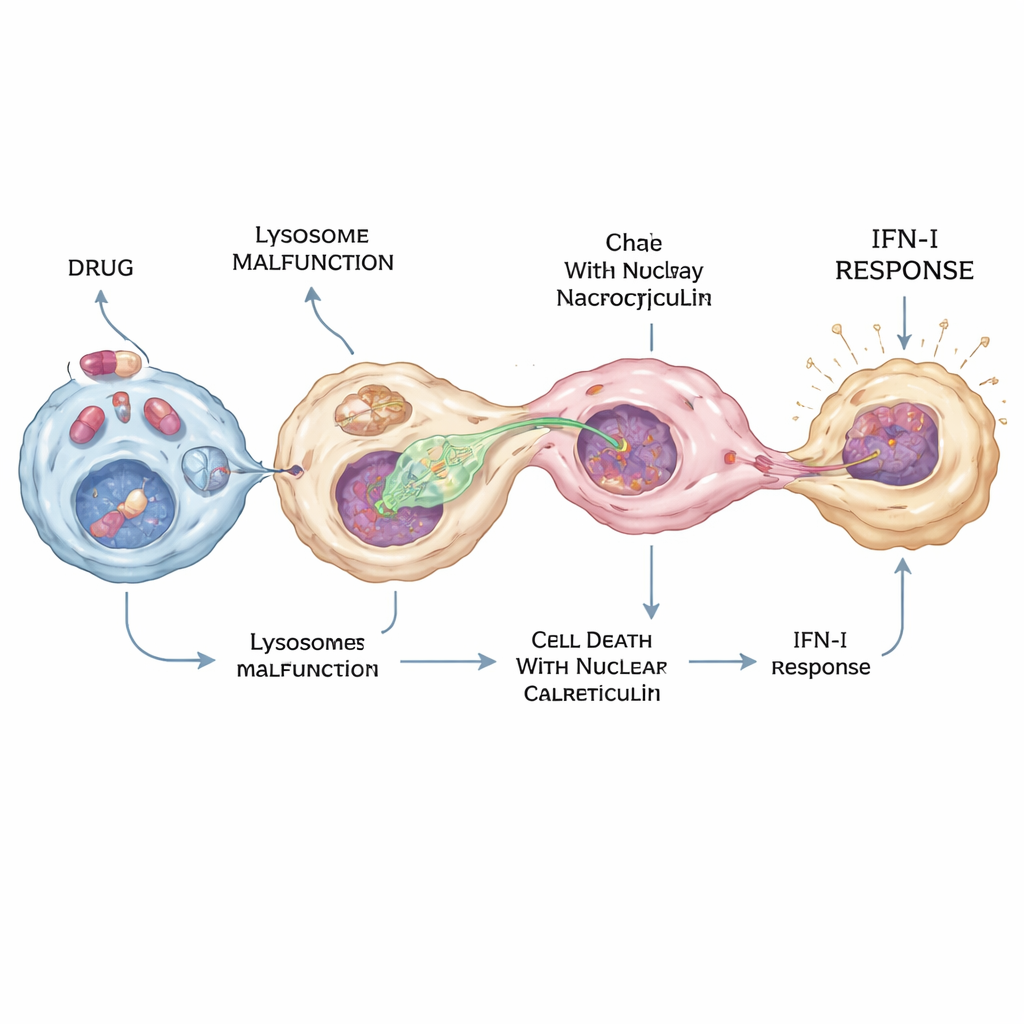
从局部防御到疾病与副作用
通过对细胞培养和小鼠肺组织的研究,团队表明经药物处理的巨噬细胞可引发一种依赖 STING 的干扰素反应,该反应大多局限于局部——例如肺部——而非成为全身性反应。这有助于解释为何羟氯喹等药物在某些组织中可能显示出抗病毒或抗肿瘤益处,但长期使用时又可能导致器官特异性的副作用,如眼或心脏毒性。每当死亡细胞与溶酶体应激同时出现时,同样的核质移位过程也有可能促成自身免疫或炎症性疾病,因为它为自身 DNA 直接激活 cGAS 报警提供了一条通路。
这对未来治疗意味着什么
对非专业读者而言,关键信息是:免疫细胞并非仅被动吞噬死亡细胞;它们可以主动从细胞核“开采” DNA 并将其作为求援信号。核质移位通路解释了我们的自身 DNA 如何以一种集中、局部的方式安全地激活强有力的抗病毒防御,同时也提醒我们扰乱溶酶体或 PPT1 的药物可能会无意间触发这一开关。通过学会调节核质移位——无论是设计更聪明的抗病毒和癌症治疗,还是在自身免疫疾病中避免不必要的自身 DNA 信号——研究者希望能利用这一新发现的机制,开发出更安全、更精确的治疗方法。
引用: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
关键词: 核质移位, cGAS-STING, 羟氯喹, I 型干扰素, 巨噬细胞