Clear Sky Science · zh
启蒙与扩散:当与免疫检查点抑制联用时,α-与β-发射放射性药物在小鼠中产生的不同免疫效应
将放射转化为免疫盟友
肿瘤科医生越来越多地尝试动员免疫系统来对抗癌症,但许多肿瘤仍然对这些药物无动于衷或产生抗性。本研究提出了一个及时的问题:不同类型的靶向放射能否不仅仅通过直接缩小肿瘤来发挥作用,而是通过“指导”免疫系统更好地工作——而且所选放射性药物是否会改变这种指导的方式?
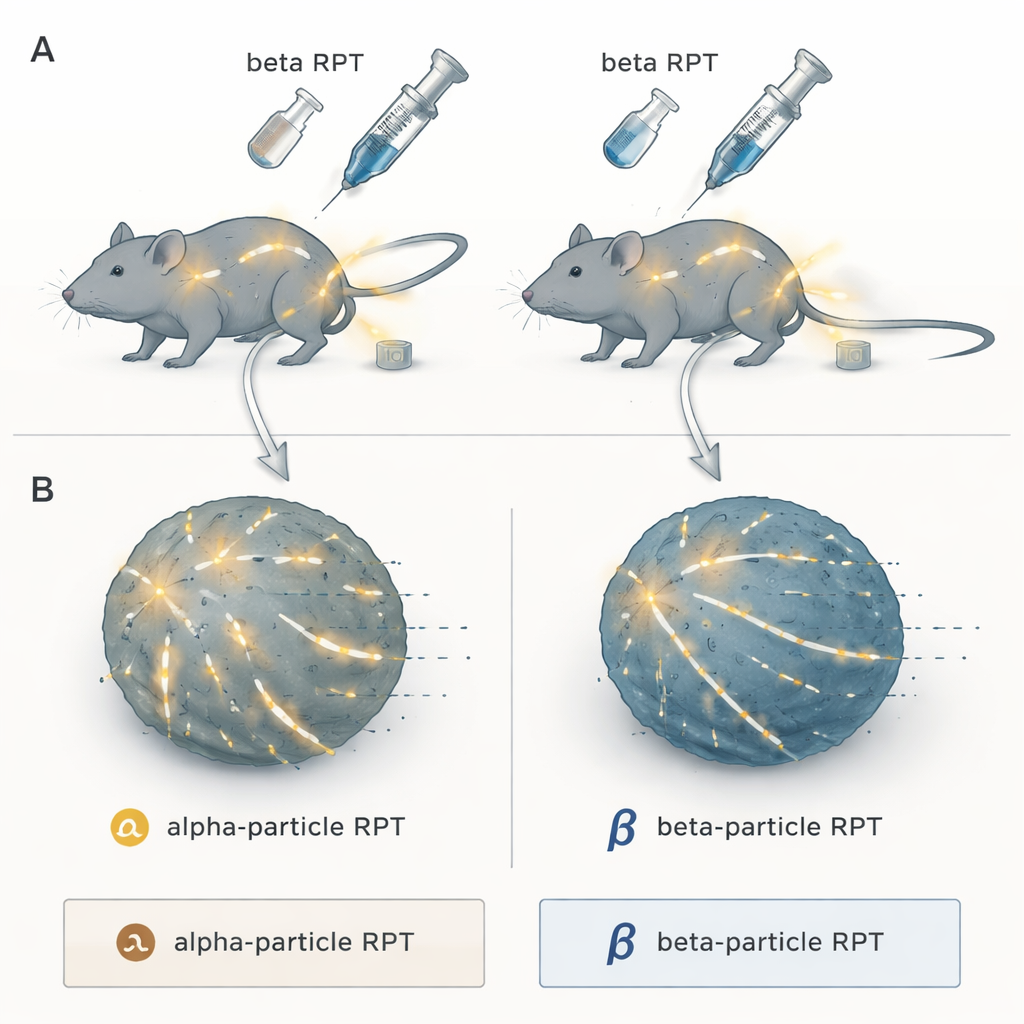
两种精确放射的形态
研究者把注意力放在放射性药物治疗上,这是一种“搜索并摧毁”的方法:将放射性载荷连接到一种自然趋向肿瘤的分子上。注射后,它在体内循环,将辐射传递到癌灶,无论它们藏在哪里,这一点是常规体外放疗难以做到的,尤其是面对广泛性疾病时。团队比较了两大类:α 粒子发射体,释放在极短距离内极高密度的能量爆发;以及 β 粒子发射体,发出密度较低但可在组织中传播更远的辐射。所有放射性核素都连接到相同的肿瘤识别化合物 NM600,因此不同之处仅在于辐射类型,而非靶向性。
将放射与免疫检查点抑制剂配对
单独使用时,抗 PD-L1 和抗 CTLA4 等检查点抑制剂可以解除免疫细胞的制动,但当肿瘤已经为免疫系统所见时效果最佳。在黑色素瘤、前列腺癌和结直肠癌的小鼠模型中,研究者以精心选择的低剂量放射分别使用基于 α 或 β 的 NM600,并有或没有联合检查点抑制剂。他们还改变了免疫药物的给药时机——在放射治疗之前、放射后不久或放射后较晚——以观察时机如何影响肿瘤生长、生存率和长期免疫记忆等结果。
当β 辐射表现出色:增强已有反应
在对免疫治疗已有反应的“免疫热”结直肠癌模型中,效果最好的方案是β 发射型 NM600,尤其在免疫药物较早或在中间时间点开始时。肿瘤缩小更多、小鼠生存期延长且治愈的动物在数月后再次接种同种肿瘤时通常能够排斥。详细的免疫谱分析显示,β 基治疗加上检查点阻断并非创造了一种全新的反应,而是放大了已有的反应:既有的肿瘤特异性杀伤性 T 细胞扩增、活化增强并产生更多攻击信号。简言之,β 发射体在扩散和加强正在进行的免疫反应方面表现出色。
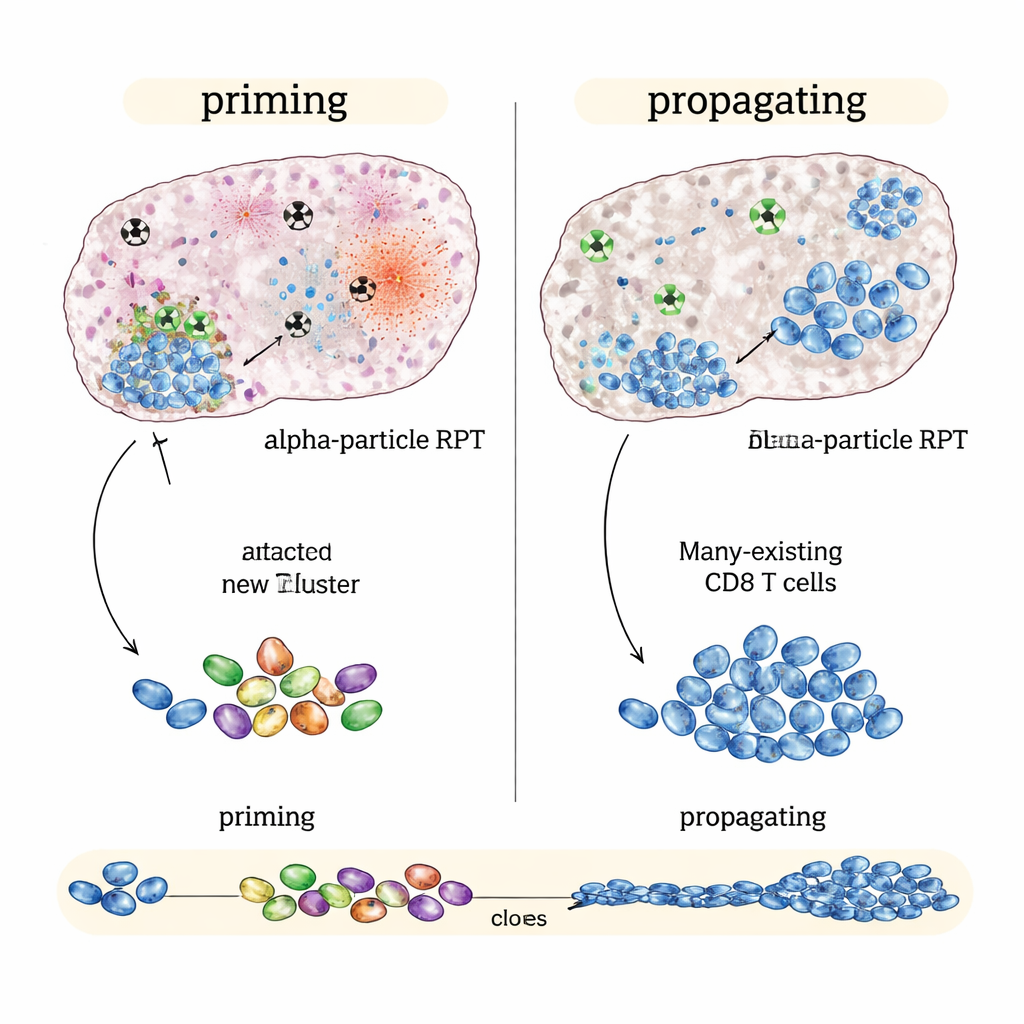
当α 辐射表现出色:点燃新的免疫攻击
相比之下,在对检查点药物几乎无反应的“免疫冷”肿瘤(如某些黑色素瘤和前列腺癌模型)中,平均肿瘤剂量相同的情况下 α 发射型的表现优于 β 发射体。α 基疗法加免疫药物更能减缓肿瘤生长并进一步延长生存期。单细胞基因组学分析提示了原因:α 辐射造成强烈、局部的损伤,似乎在肿瘤内产生了强烈的警报信号,同时相对保留了邻近的免疫结构。这一模式与更广泛且多样化的 T 细胞反应相关,并显示出新的肿瘤识别性杀伤 T 细胞被产生并与长期记忆细胞相连的迹象——这是免疫启蒙(priming)而非单纯扩大的证据。
为何放射的类型与时机至关重要
在不同模型中,检查点抑制剂在放射诱导的危险信号高峰期前后立即或在中间时机给药的效果,普遍优于延迟治疗。这项工作提出了一个实用的经验法则:在已为免疫系统所见的癌症中,低剂量的β 基放射性药物可能是与检查点抑制剂配合的理想选择,因为它们能扩散并增强现有免疫力;在更具免疫抵抗性的癌症中,高冲击力的α 发射体或许更适合启蒙新的 T 细胞反应,将“冷”肿瘤转为“热”。对患者而言,这意味着并非所有放射性药物都可互换;将同位素和给药时间表与肿瘤的免疫特性相匹配,可能使放射-免疫联合疗法既更有效又更持久。
引用: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
关键词: 放射性药物治疗, α 与 β 辐射的比较, 免疫检查点抑制剂, 癌症免疫治疗, 肿瘤微环境