Clear Sky Science · zh
靶向 HIV Gag 的双特异性 T 细胞受体在 HIV 感染男性中的安全性与生物学活性:首例人体试验
这项新 HIV 研究为何重要
得益于现代药物组合,当前感染 HIV 的人可以期待接近正常的寿命。但这些药物,即抗逆转录病毒治疗(ART),并不能清除病毒;它们仅将病毒控制住。体内仍存在隐藏的 HIV 围窝,若停止治疗可重新点燃感染。本研究测试了一种新型的精准免疫疗法——由实验室构建的 T 细胞受体组成——旨在训练免疫系统安全地在已接受良好 ART 控制的个体中寻找并消灭这些隐匿处。
不消失的隐藏病毒
即使血液检测显示“检测不到”病毒,HIV 仍以基因组形式潜伏在寿命较长的细胞中,主要是被称为 CD4 T 细胞的一种白细胞。这些储藏库细胞携带静默但完整的病毒,可能再次被激活,迫使人们终生服药。完全抹除每个感染细胞极具挑战性,仅在少数接受高风险骨髓移植治疗癌症的个体中实现过。许多研究者因此更倾向于追求“功能性治愈”:将储藏库缩小到体内自身免疫可以在不需持续用药的情况下维持 HIV 受控的程度。
重定向 T 细胞的设计分子
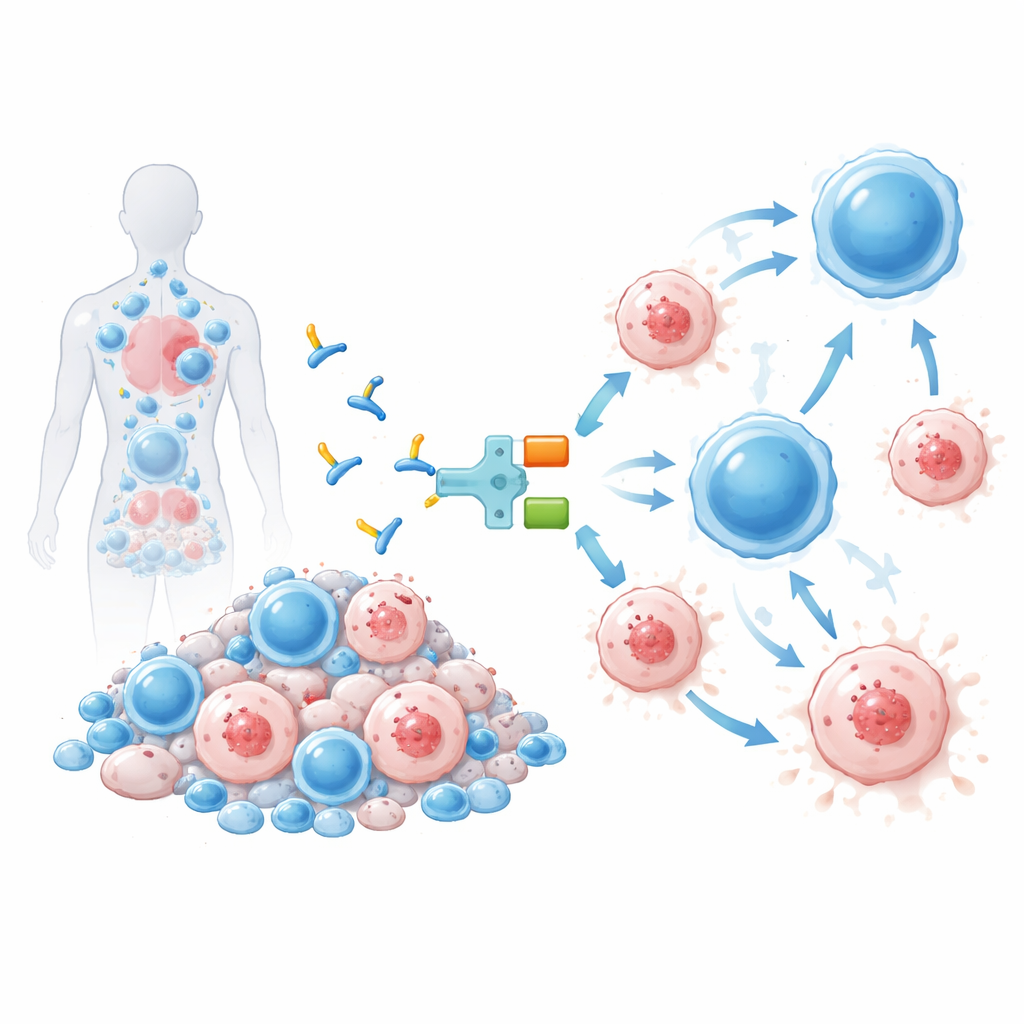
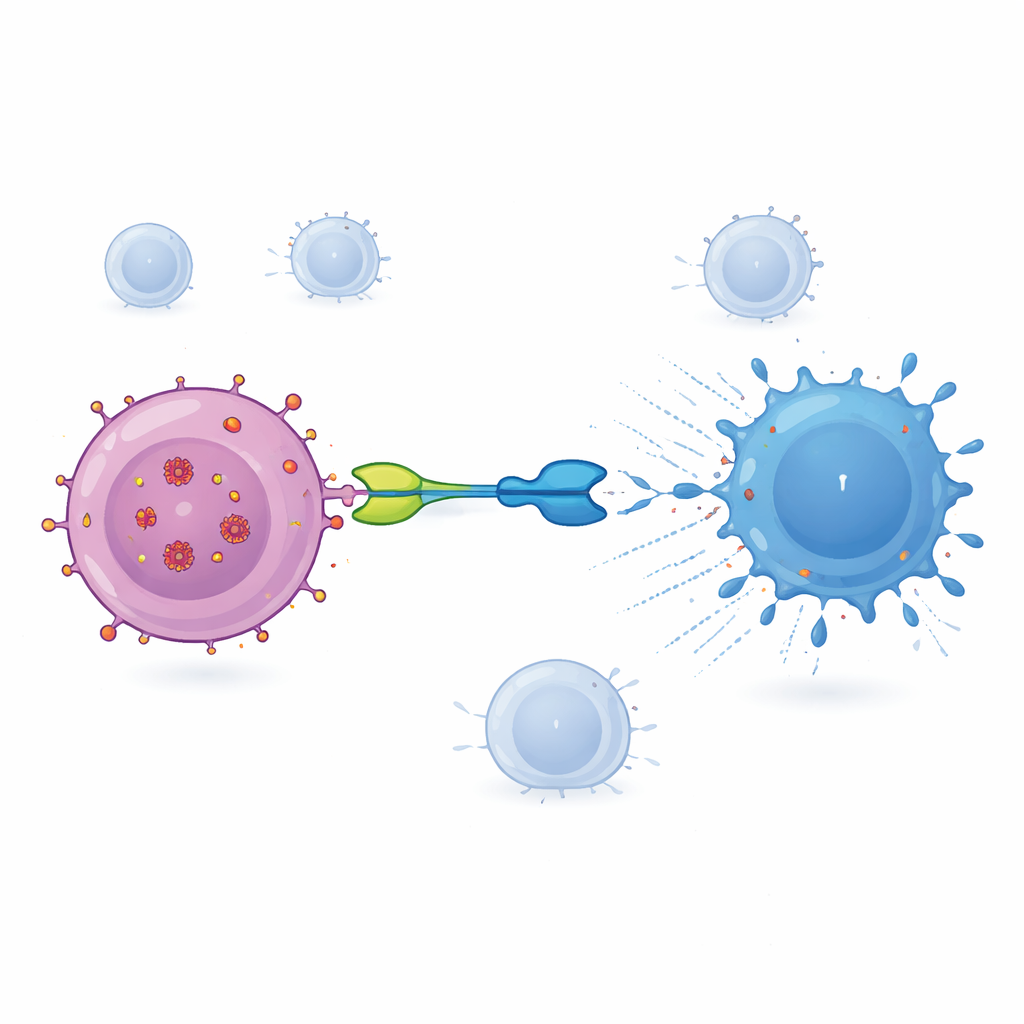
本次测试的疗法称为 IMC‑M113V,是一种小型蛋白,类似于在受感染细胞与免疫系统之间搭建的分子适配器。IMC‑M113V 的一端是经过工程改造的 T 细胞受体,能识别在特定免疫标记(HLA‑A*02:01)背景下呈现在受感染细胞表面的 HIV Gag 蛋白的一段小片段。另一端则结合 CD3,这是一种存在于所有 T 细胞表面的结构。当 IMC‑M113V 同时结合两端时,它将普通 T 细胞拉到接近 HIV 感染细胞的位置并触发其杀伤功能。在体外实验中,该分子高度敏感,能检测到细胞表面仅有少量的病毒片段拷贝,并能有效清除被数种常见 HIV 变体感染的细胞,同时对一组健康人类细胞没有明显激活反应。
首次在 HIV 感染者中的人体测试
为评估该方法在人类中的安全性,研究者在英国、比利时和西班牙对 12 名成年来自 HIV 感染的男性开展了早期临床试验。所有参与者均在 ART 下病毒得到良好控制、CD4 计数较高且携带所需的 HLA 类型。每位受试者静脉注射一次 IMC‑M113V,剂量为三个低剂量水平之一,随后观察一个月。该阶段的主要关注点是安全性:监测诸如发热、严重炎症或神经系统问题等不良反应——这些反应在其他用于癌症治疗的强效 T 细胞拉动药物中可能发生。
临床观察到的情况
在所有剂量范围内,IMC‑M113V 总体耐受良好。半数参与者报告了某些副作用,主要为疲劳或皮肤刺激等轻度问题,且无人出现细胞因子释放综合征或神经毒性等严重并发症。血液检测显示药物水平在大约一天内上升并下降,半衰期约为 15–22 小时。在最高剂量(15 微克)时,若干参与者出现了炎性分子(尤其是白细胞介素‑6)短暂升高,并显示其 T 细胞被激活、并更有能力产生细胞杀伤蛋白的迹象。这些免疫学变化在那些其病毒携带 IMC‑M113V 能特别紧密结合的 Gag 变体的志愿者中最为明显,提示药物在体内确实作用于预期靶点。然而,在单次给药后,基于病毒 RNA 以及 CD4 细胞内完整病毒 DNA 的测定,血液中 HIV 储藏库的规模并未出现可测量的下降。
这对未来 HIV 治疗的意义
对非专业读者来说,主要信息是:这项研究提供了一个重要的初步概念验证:高度特异的免疫“桥接”分子可以安全地给予病情受控的 HIV 感染者,并能唤醒其 T 细胞识别携带病毒的细胞。它并未治愈 HIV 或使人们停止 ART,但这也不是首例人体试验的目标。研究结果支持进一步测试更高剂量和重复给药,可能与能诱导更多感染细胞显露自己的药物联用,并将该方法扩展到覆盖除 HLA‑A*02:01 以外的其他免疫类型。如果后续研究证实这一策略可以在无严重副作用的情况下可靠地缩小病毒储藏库,它可能成为旨在实现长期无药物控制 HIV 的组合疗法中的关键组成部分。
引用: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
关键词: HIV 治愈, T 细胞疗法, 病毒储藏库, 双特异性受体, 临床试验