Clear Sky Science · zh
用于多模态治疗骨关节炎的有机二硒化物水凝胶微球
为何这种新的关节疗法重要
骨关节炎是导致疼痛和功能受限的主要原因之一,但现有大多数治疗仅缓解症状或仅针对关节的单一部位。本文描述了一种智能可注射材料,由携带有机硒的微小凝胶微球构成。该材料被设计为感知并响应关节损伤的早期信号,目标不仅是减轻疼痛,还能同时保护并重建软骨、抑制滑膜的炎症并稳定下方的骨质。
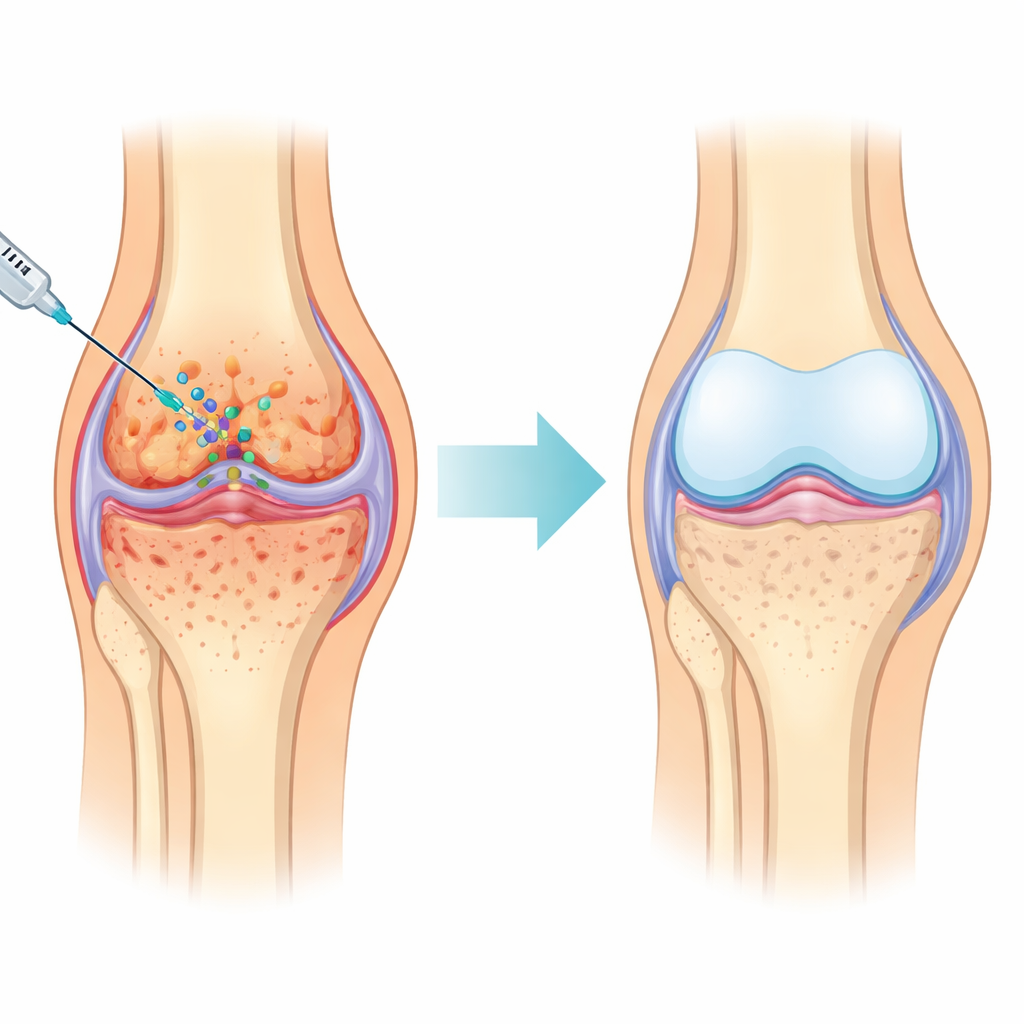
磨损关节内的隐性压力
在骨关节炎中,损伤在整个关节累积:光滑的软骨表面变薄并出现裂纹,下面的海绵状骨异常增密或被侵蚀,关节滑膜增厚并发生炎症。这些问题的共同线索是氧化应激——过量的活性氧分子损伤细胞及其线粒体(细胞的能量工厂)。作者显示,在患有骨关节炎的人类和动物软骨中,依赖硒的关键天然“清道夫”蛋白显著减少,使软骨细胞更易受损,加速关节表面的破坏。
将硒转化为靶向关节药物
先前关于硒纳米颗粒的工作提示,补充硒可帮助关节细胞恢复抗氧化防御并减缓软骨流失,但游离纳米颗粒在安全性、剂量和在关节内滞留时间方面存在顾虑。为了解决这些问题,研究团队将一种有机硒化合物化学接入基于透明质酸(一种天然关节润滑剂)的柔性水凝胶中,然后将该材料制成足够小、可通过针管注射并留在关节内的微球。这些微球包含特殊的化学键,遇到两种早期骨关节炎的标志物时会断裂释放:活性氧暴增和一种称为MMP13的软骨降解酶水平升高。这种双重触发设计使微球在关节处于应激时局部释放硒,而不是一次性全部释放。
智能微球如何帮助关节细胞
在细胞试验中,负载硒的微球表现优于基础水凝胶和传统硒纳米颗粒。在受压的软骨细胞中,它们提高了依赖硒的蛋白产量,改善了线粒体结构与能量产生,并将能量利用从应急的糖酵解转向更高效的呼吸。该转变的一个中心作用因子是名为TXNRD1的蛋白,治疗使其增加,从而帮助激活一个关键的生长与存活通路(PI3K–AKT–mTOR)。随着该通路的恢复,软骨细胞产生更多健康基质的构建成分并减少降解基质的酶,同时清除过量的活性氧物质。
在关节中重新平衡骨细胞与免疫细胞
骨关节炎不仅是软骨磨损;骨吸收细胞和滑膜中的免疫细胞也推动疼痛与损伤。研究人员发现在体外模型中,微球抑制了破骨细胞的形成与活性,在动物中它们减少了早期的骨流失以及随后软骨下骨的硬化。与此同时,治疗促使关节滑膜组织中的巨噬细胞——免疫细胞——从一种侵袭性、促炎的状态转向更具修复性、抑制炎症的状态。这些变化同样与硒驱动的抗氧化效应及对PI3K–AKT–mTOR通路的调节有关,表明不同关节细胞类型间存在共同的控制开关。
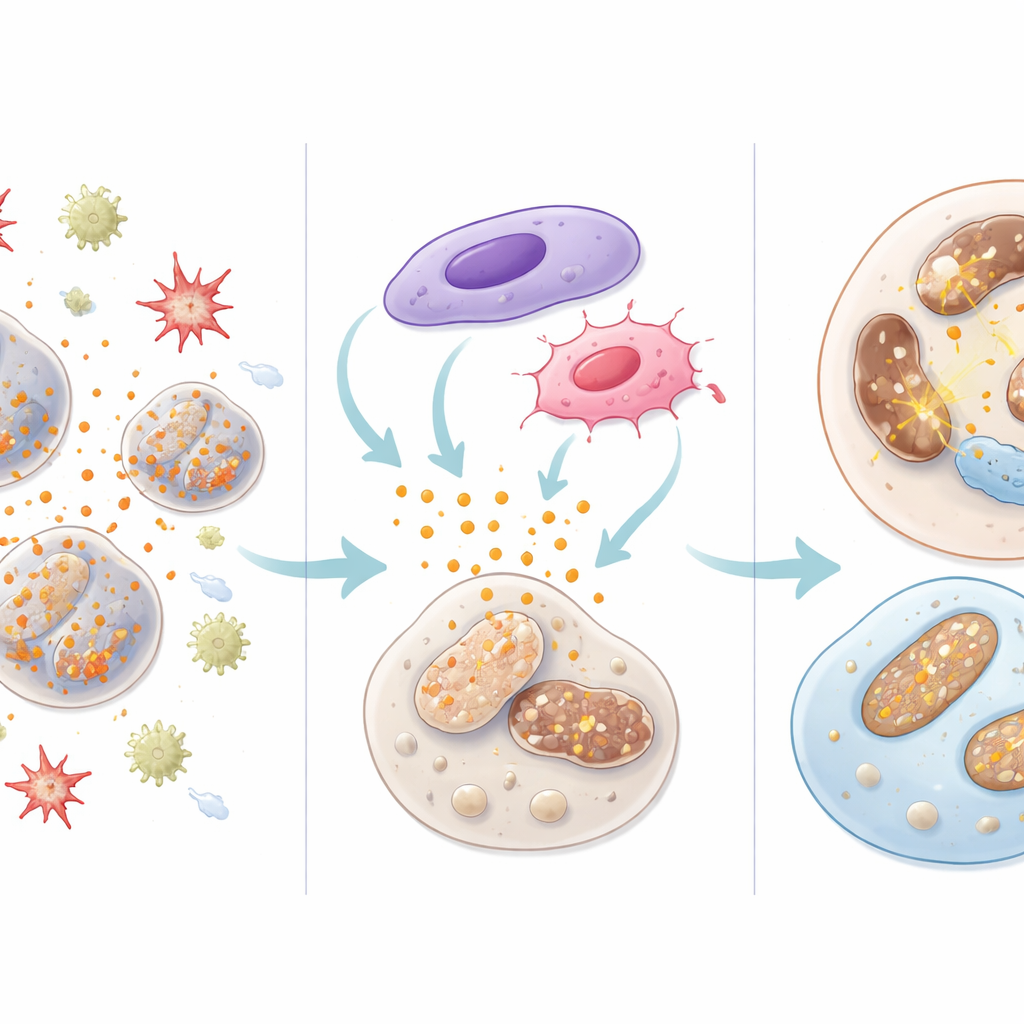
在活体关节中从保护走向再生
当团队将微球注入外科诱导骨关节炎的大鼠关节时,与生理盐水或更简单的水凝胶相比,关节表现出更少的软骨侵蚀、更少的滑膜炎症迹象,并且随时间显示出更健康的骨结构模式。动物活动更自如,疼痛迹象减少。在另一种全层软骨缺损模型中,将软骨形成前体细胞与微球一同负载,能更好地填补缺损,形成光滑、类透明软骨而非瘢痕样组织。重要的是,该材料在主要器官和血液检测中未显示明显毒性。
这项工作对关节炎患者意味着什么
对非专业读者而言,作者创建了一种类似“智能海绵”的关节材料——微小的凝胶微球能感知早期骨关节炎的化学紊乱,并响应性地在局部以受控方式释放保护性营养物质。通过恢复关节自身的抗氧化防御与能量平衡,这种方法同时保护软骨、抑制炎症并稳固关节表面下的骨质。尽管在用于人类之前仍需大量工作,这项研究勾勒出一种有前景的全流程骨关节炎护理策略:一次注射即可以疾病自身的生化语言工作,同时治疗多个问题区域,而不是在严重损伤发生后才去追逐症状。
引用: Liu, Y., Zhang, Y., Yu, C. et al. Organic di-selenide hydrogel microspheres for multimodal treatment of osteoarthritis. Nat Commun 17, 2300 (2026). https://doi.org/10.1038/s41467-026-68817-2
关键词: 骨关节炎, 硒, 水凝胶微球, 软骨再生, 氧化应激