Clear Sky Science · zh
可变剪接在造血谱系决策中的功能全景
基因的微小编辑如何塑造我们的血液
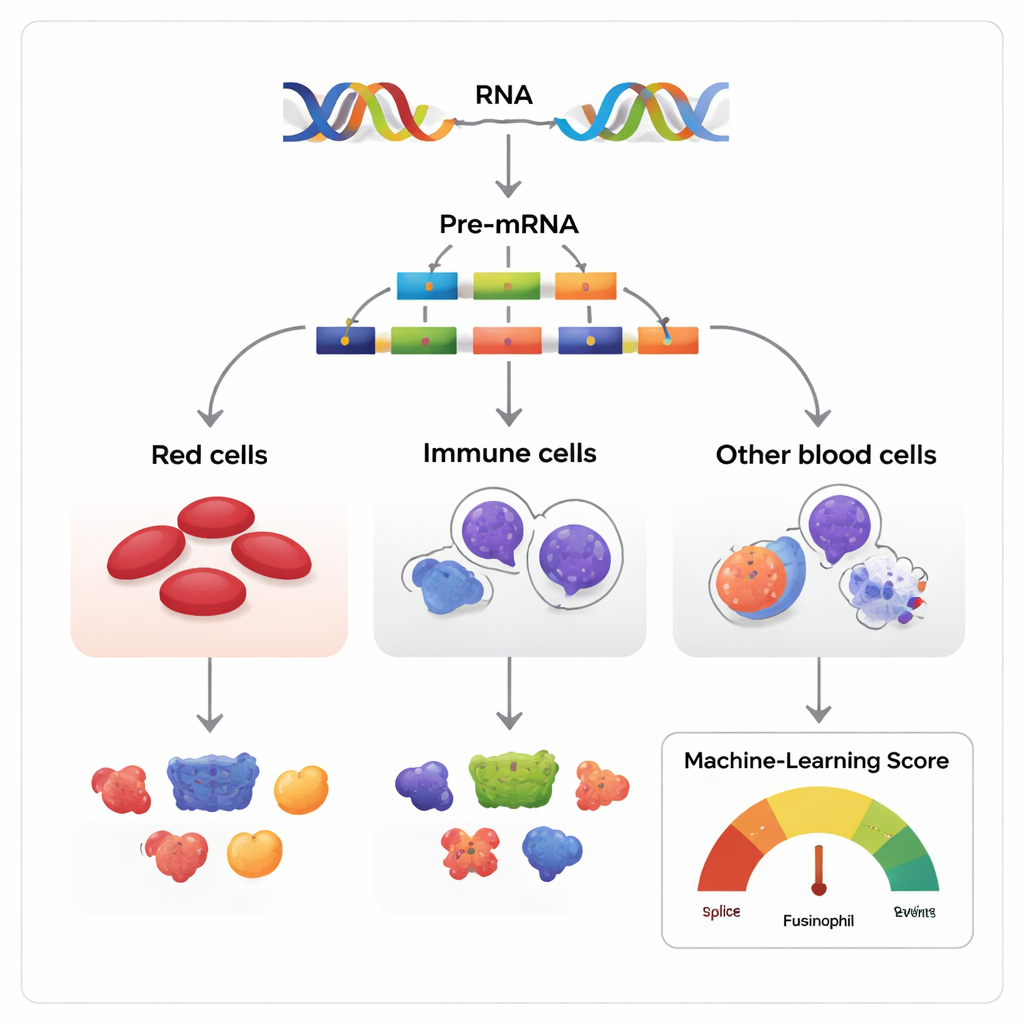
你的身体每秒钟都会制造数百万个新的血细胞。在这一静默奇迹背后,是一种分子编辑系统,它可以以不同方式剪接并粘贴遗传信息的片段,从而产生同一蛋白的略微不同版本。本研究探讨了这种称为可变剪接的编辑过程如何引导未成熟干细胞分化为红细胞、白细胞或其他血细胞类型——以及当某一被编辑的片段缺失时会发生什么。
同一遗传脚本产生的多种版本
人们常把基因比作蓝图,但实际上它们更像可以重排的剧本。基因被读取时,初始的RNA拷贝包含称为外显子(exon)的片段,这些片段在最终翻译成蛋白之前可以被保留或跳过。作者在人体、小鼠及若干其他脊椎动物的造血组织中考察了这一过程,尤其是外显子跳跃(exon skipping)。他们汇集了超过270个RNA数据集,跟踪造血干/前体细胞在成熟为三大类家族时的变化:产生红细胞的红系、抵御感染的髓系和产生抗体的淋系细胞。
评估哪些剪接改变真实重要
由于大多数多外显子基因可被多种方式剪接,核心挑战在于将无害变体与真正影响细胞命运的变体区分开来。研究者构建了一个机器学习模型,称为功能性可变剪接评分(Functional AS Score,FAScore),以应对这一问题。对于每个外显子跳跃事件,模型考虑了19项信息,例如该外显子在细胞发育过程中使用频率变化的强度、周围DNA在物种间的保守性、是否改变已知的蛋白结构域、以及是否包含蛋白的化学修饰位点等。该算法使用正样本-未标注样本策略训练,并采用随机森林分类器,输出介于0到1之间的分数,表明某一剪接事件具有功能影响的可能性。
发现保守且谱系特异的开关
将FAScore应用于数万例外显子跳跃事件后,团队将这些事件划分为可能有功能、无功能或不确定三类。被预测为有功能的事件更常出现在对相互作用重要的蛋白区域、在进化上保守的序列中,以及位于承载磷酸化或SUMO化等化学标记的片段中。许多此类事件还仅在特定血液谱系或胎儿期血液形成阶段活跃,表明它们在特定发育窗口中充当微调开关。研究还显示,一些最古老的剪接事件——在脊椎动物中保存了数亿年的那些——尤其可能具备功能性,这类似于年龄较大的基因往往承担核心生物学角色的情形。
实验证据:调控血细胞命运
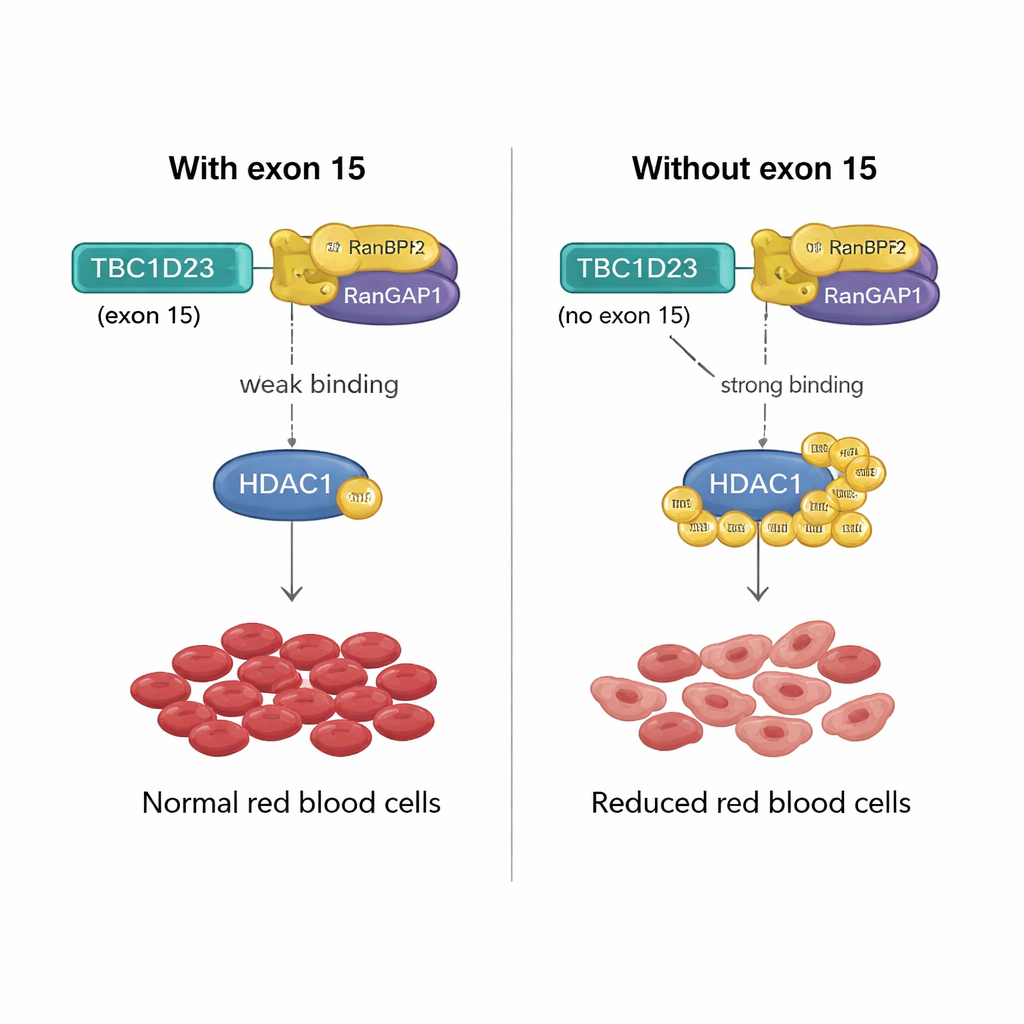
为了验证模型的预测,作者在不同血液谱系活跃的基因中选择了若干高分外显子,并在小鼠的造血干/前体细胞中用CRISPR删除这些外显子。结果与模型预期一致:删除KLF6和SSBP3基因中的某些外显子会损害髓系集落的形成而不影响红细胞产出;而删除EPB41L1和TBC1D23中的外显子则改变了红系集落的形成。尤其是删除TBC1D23的第15号外显子会降低小鼠和斑马鱼红细胞前体的产生,导致循环红细胞数量减少、血红蛋白水平下降,而对白细胞影响较小。
调节红细胞生成的分子杠杆
为何TBC1D23的第15号外显子编码的仅15个氨基酸片段会产生如此影响?团队发现,包含该外显子会削弱TBC1D23与一对称为RANBP2/RANGAP1的蛋白的结合,这对蛋白协同作用可将SUMO标签附加到其他蛋白上。缺失第15号外显子时,TBC1D23与该蛋白对的结合更强,进而增强了一种关键酶HDAC1的SUMO化。这种增强的修饰改变了许多转录因子的活性——这些转录因子是基因表达的主控器——扰乱了红细胞正常成熟所需的基因程式。当研究者构建了一个在两个关键位点无法被SUMO化的HDAC1版本时,该变体在缺失TBC1D23第15号外显子的细胞中恢复了红细胞形成,证实了该化学修饰是关键步骤。
这项工作对健康与未来疗法的意义
对非专业读者而言,这项工作的核心信息是:并非所有遗传变化都等价——有时,健康血液与贫血之间的差别就在于遗传信息的一个微小片段在最终信息中是被保留还是被跳过。通过将大规模RNA数据与复杂的评分系统结合,研究为识别哪些剪接变体最可能影响干细胞命运提供了路线图。这一方法不仅加深了我们对健康与疾病状态下血细胞形成机制的理解,还提供了一种通用策略,用于在其他器官中定位重要的剪接事件,可能为未来的基因疗法和精准治疗提供指导。
引用: Hu, X., Wang, J., Chen, L. et al. The functional landscape of alternative splicing in hematopoietic lineage commitment. Nat Commun 17, 2047 (2026). https://doi.org/10.1038/s41467-026-68811-8
关键词: 可变剪接, 造血, 机器学习, 红细胞, 基因调控