Clear Sky Science · zh
比较多组学分析揭示鳍与肢体再生的保守与派生机制
为什么长回丢失的身体部位很重要
许多动物能够再生丢失的身体部位,从蜥蜴的尾巴到蝾螈的肢体。弄清楚它们如何做到这点,不只是出于好奇:让鱼重建鳍或让蝾螈替换肢体的规律,未来可能为人类严重伤害的治疗提供新思路。本研究比较了几种在再生方面表现异常出色的动物,深入细胞层面以发现哪些修复机制是古老且共有的,哪些是较新的演化创新。
不同的动物、不同的肢体、相同的重大问题
研究人员聚焦三种物种:能完全再生肢体的墨西哥钝口螈(axolotl)、以鳍修复著称的斑马鱼(zebrafish),以及一种原始的硬骨鱼Polypterus,它不仅能再生薄薄的外鳍条,还能重建包括内骨骼和肌肉在内的整个鳍。通过比较这些动物,团队探问是否存在一个可追溯到早期脊椎动物演化的通用“工具箱”用于重建复杂器官。他们采用现代基因组学方法,读取数千个单细胞中哪些基因被激活,并绘制这些细胞在组织中的位置。
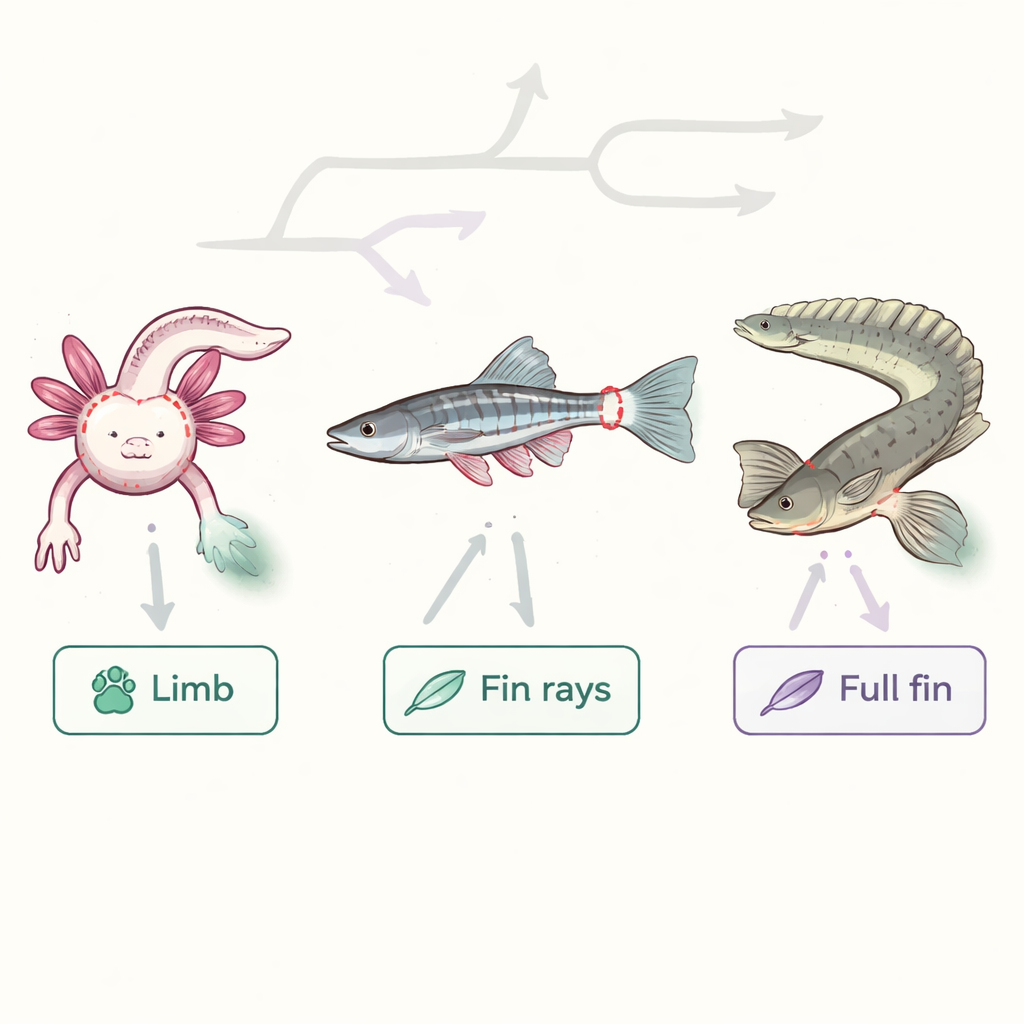
绘制再生鳍的细胞图谱
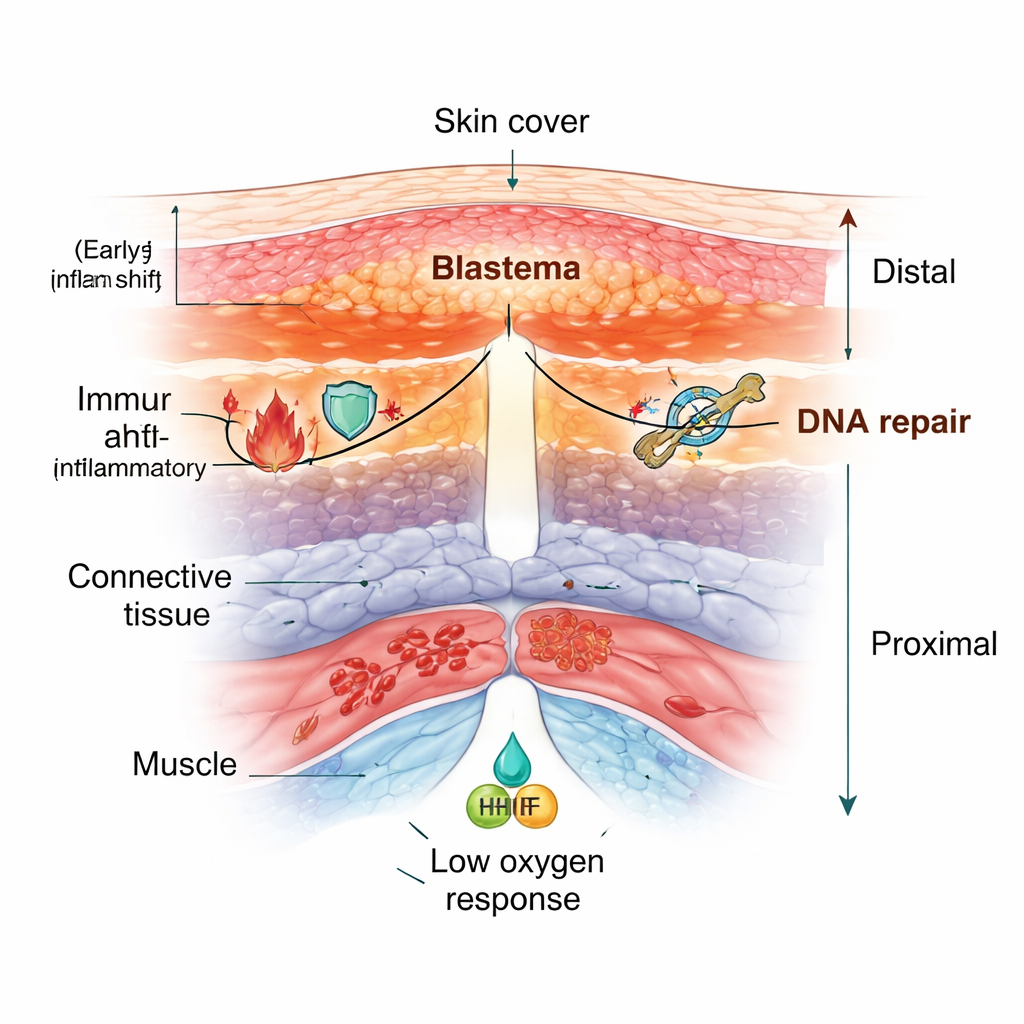
在Polypterus中,科学家在受伤前以及截肢后数个时间点采样鳍。他们发现了三十多种不同的细胞群体,包括不同层次的皮肤、免疫细胞、血管、肌肉、结缔组织以及分裂活跃的“芽体”细胞——推动新生长的细胞团。随着鳍的愈合,沉寂的成体组织被活跃的修复区所取代:免疫细胞大量涌入,皮肤增厚形成专门的创面覆盖层,结缔组织细胞向切口处迁移以构建芽体。在检查墨西哥钝口螈的肢体和斑马鱼的鳍时也观察到类似模式,表明这种细胞类型重组是附肢再生的共有特征。
古老的构建蓝图与新的变化
更仔细的观察显示,生长尖端并非均质。在Polypterus的鳍和墨西哥钝口螈的肢体中,创面下方的结缔组织沿肢体长度分裂为两类区域:远端靠近尖端,富含快速分裂并产生基质的成纤维细胞;近端更靠近躯体,细胞更像稳定的收缩支持型细胞。覆盖创口的皮肤也重新激活了胚胎期用于构建“顶端外胚层脊”(apical ectodermal ridge)的基因程序——这是一条对肢体外生至关重要的信号带。该程序出现在创面皮肤和邻近的结缔组织中,表明成体再生重复利用了古老的发育指令,但将其分布于多个组织之中。
应激信号、氧气调控与免疫开关
跨物种观察到,受伤的鳍和肢体强烈激活DNA损伤与修复相关基因,仿佛细胞在进入强烈生长期之前检查并修复它们的基因组。免疫反应也遵循相似的顺序:早期的一波促炎信号有助于清除受损组织,随后抗炎信号上升,促进组织重建而非瘢痕形成。另一个共同主题是“低氧”反应。细胞稳定了对缺氧敏感的因子并增强支持糖酵解的基因,糖酵解是一种即使在氧气匮乏时也能运行的代谢途径。在Polypterus和墨西哥钝口螈中,受伤部位附近红细胞显著扩增,并携带一种特殊的氧感受基因变体,这提示血细胞可能帮助调节愈合环境。在Polypterus和斑马鱼中,甚至创面皮肤也开启了一种通常见于肌肉的肌红蛋白基因,可能在再生过程中帮助缓冲氧气和有害的活性分子。
基因组中的控制开关
为找到控制再生基因开闭的DNA开关,团队测量了Polypterus在鳍受伤后基因组哪些区域变得更“开放”。数百个区域可及性增加,其中许多位于已知在创面皮肤和芽体中活跃基因的附近。这些区域富集有AP-1转录因子结合位点,AP-1是一类作为基因网络主开关的蛋白质。类似因子也已被指认为斑马鱼和墨西哥钝口螈再生过程中的参与者,表明在不同动物和附肢间存在保守的调控逻辑。
对未来愈合的意义
对一般读者来说,核心信息是:鳍与肢体再生并非神奇而孤立的现象;它们依赖一套古老的细胞参与者和基因回路,这些要素在很久以前就已演化出来。高度再生的动物将这套古老工具箱与物种特有的调整相结合——例如额外的肌红蛋白基因或不同寻常的血细胞行为——以细化修复过程。通过描绘这些共有与独特的策略,本研究使我们更接近理解为何某些脊椎动物能重建复杂结构而另一些(包括人类)不能,并指出了未来可能用于增强我们自身愈合能力的分子通路。
引用: F. Sousa, J., Lima, G., Perez, L. et al. Comparative multi-omic analysis reveals conserved and derived mechanisms of fin and limb regeneration. Nat Commun 17, 1922 (2026). https://doi.org/10.1038/s41467-026-68801-w
关键词: 肢体再生, 鳍再生, 创伤愈合, 干细胞, 进化