Clear Sky Science · zh
将肽凝聚体递送到细胞内以构建稳定的相互作用中心
在细胞内构建新的“工作站”
我们的细胞内充满了执行重要任务的小型工作区——例如产生能量或应对应激反应。随着时间推移或在疾病状态下,这些天然的工作站可能会失效。本研究探索了一种通过简单的实验室合成短肽构建小液滴,将全新的“相互作用中心”引入活细胞的方法。这些合成中心能够捕获特定蛋白、将其浓缩,甚至促成其降解,提示了未来疗法和细胞工程的新策略。
为何细胞需要定制工作区
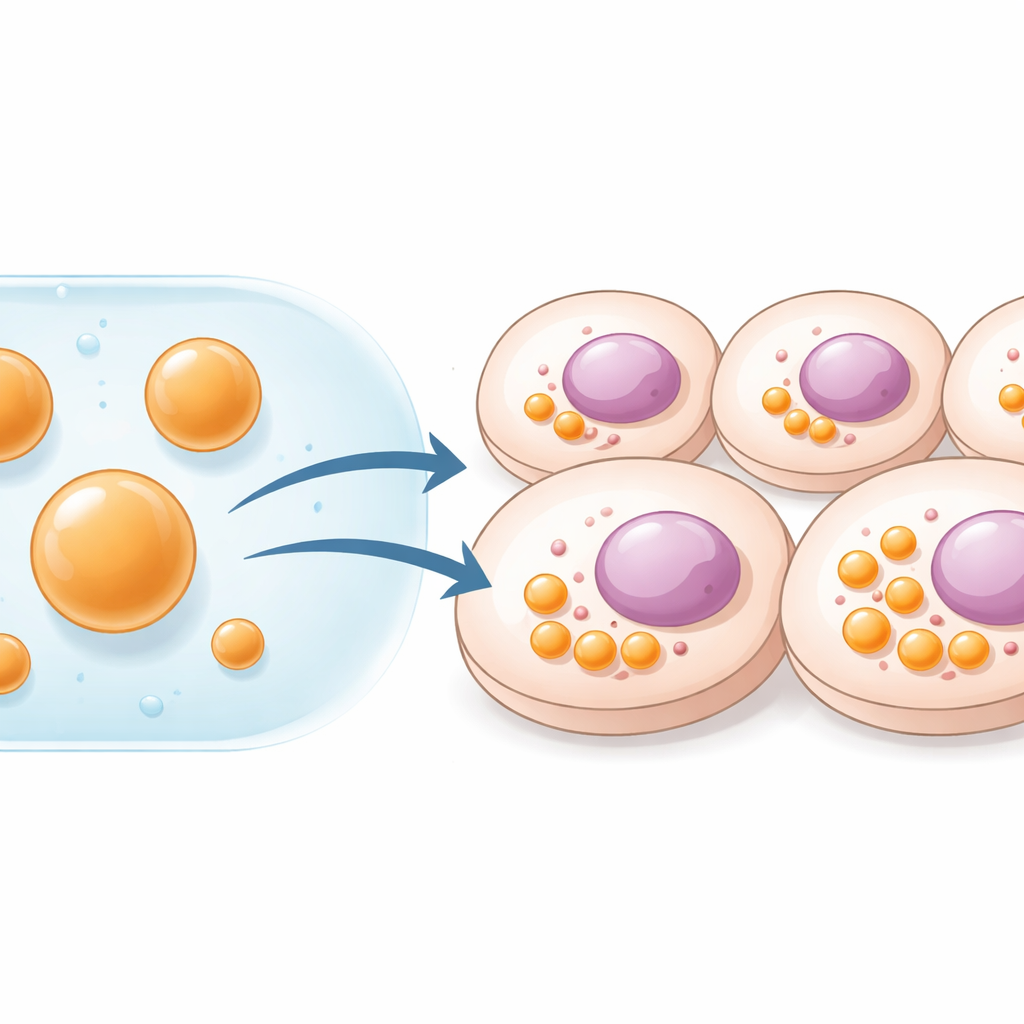
细胞通过将不同任务隔离到独立的区室来维持秩序。有些区室由膜包裹,例如线粒体;另一些则是较为柔软的、由某些蛋白和RNA聚集形成的液滴状结构。这些流体液滴或凝聚体充当反应中心,加速或关闭特定生化通路。此前科学家通过让细胞表达外源支架蛋白来人工构建此类区室。尽管方法强大,但需要基因递送,并受限于细胞能产生的物质量。本文作者试图完全绕过DNA,而是在细胞外构建即用型区室,然后将它们直接作为稳定的微米级液滴递送入细胞。
形成稳定中心的肽液滴
研究团队使用了短且无规则的肽,称为HBpep,以及一种对氧化还原敏感的变体HBpep‑SA。在微酸性条件下这些肽保持溶解,但当pH调整到接近生理水平或温度降低时,它们会相分离形成直径约1–5微米的软凝胶样液滴。通过调节肽浓度,研究者可以控制液滴的大小和数量。利用荧光技术,他们显示液滴内部肽分子的运动缓慢,表明处于凝胶状态,足够坚固以抵抗稀释和操纵。将液滴加入人类癌细胞、小鼠黑色素瘤细胞和原代人类免疫细胞的培养物后,液滴被高效内吞并在细胞质中富集。尤其是较大的液滴至少能在细胞内保持五天不破裂,有效地作为细胞内的长寿命合成细胞器存在。
为中心加载并瞄准目标
要使这些中心有用,必须能容纳并组织货物蛋白。研究者首先通过在示踪蛋白GFP上连接一段来源于HBpep的短标签来改进装载。该标签促使GFP强烈分配到液滴中,有趣的是,GFP在液滴表面富集,形成核—壳结构。接着,他们在液滴中嵌入纳米抗体——这种紧凑的类抗体蛋白可与所选靶点紧密结合。一种能结合GFP的纳米抗体使这些中心能在试管和细胞内选择性捕获GFP。由于肽凝胶较为致密,初期大部分被捕获的GFP积聚在液滴表面。但当内部结构部分松散化(通过改变氧化还原条件)或帮助液滴逃离包围它们的内体膜时,GFP也开始渗入内部。细胞实验中,促进内体逃逸的化学助剂显著提高了成功招募目标蛋白的液滴比例。
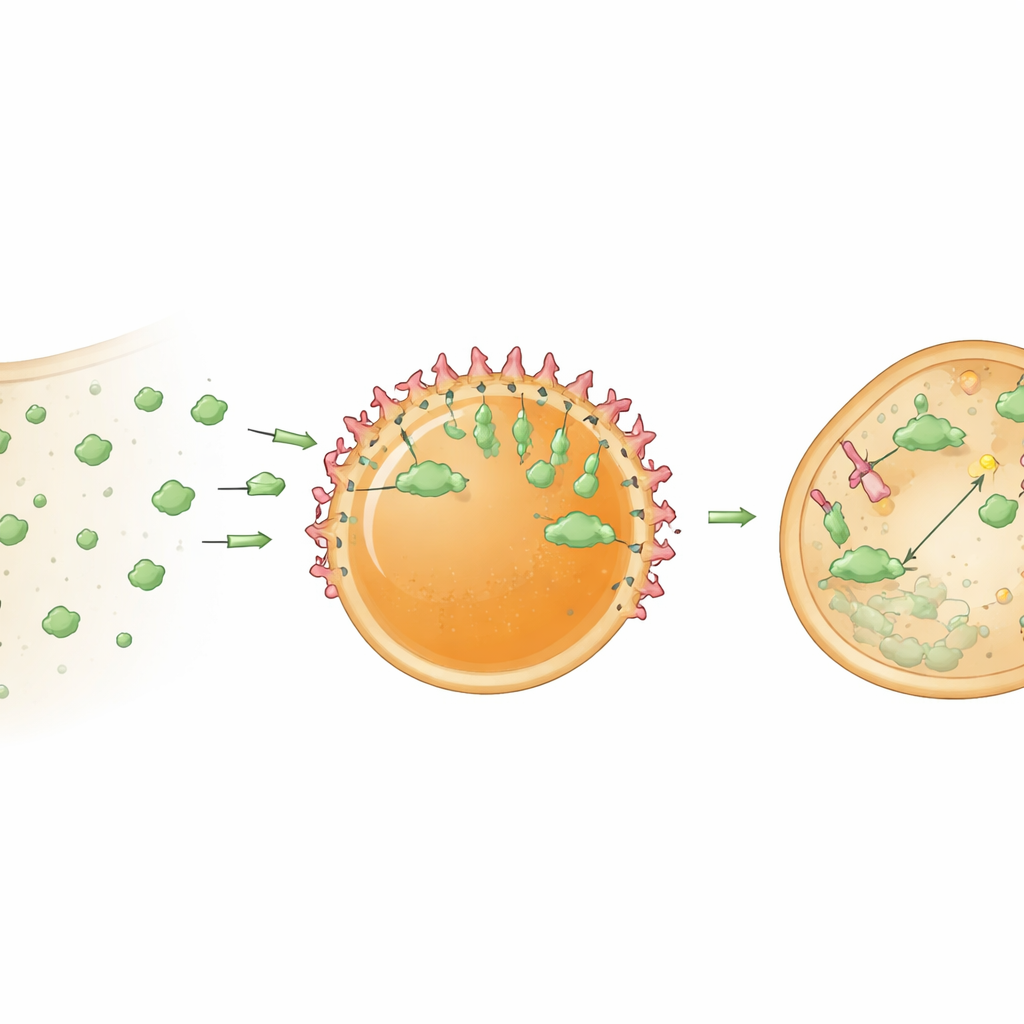
将中心变为蛋白“碎纸机”
随后作者将这些中心从被动陷阱升级为主动处理中心。他们向液滴装载了bioPROTAC——一种融合蛋白,将能结合靶标的纳米抗体与一段能招募细胞降解系统的酶适配子连接在一起。当这些“降解体”液滴被递送入稳定表达GFP的细胞时,细胞质中的GFP水平在一天内约下降了78%。仅含纳米抗体的对照中心虽能封存GFP,但并未显著降低其总体水平,证实了GFP强烈下降源于靶向降解而非单纯捕获。研究结果表明,将bioPROTACs聚集在高浓度微环境中比其在细胞质中自由分散时要高效得多。
这对未来疗法意味着什么
简言之,这项工作表明科学家可以在试管中制造基于肽的液滴,装载定制的蛋白工具,然后将它们递送入活细胞,在那里它们表现为新的、持久的细胞器。这些合成中心能选择性地吸引天然蛋白,并在配备降解装置时主动清除选定靶标。由于该平台避免改变细胞基因且所携带内容模块化,它为通过在细胞内安装新的可编程“工作站”来恢复或重写细胞行为(例如清除有害蛋白或重接线错误信号)开辟了途径。
引用: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
关键词: 合成细胞器, 肽凝聚体, 细胞内递送, 蛋白降解, 细胞工程