Clear Sky Science · zh
被侧翼R环、延长的间隔区和失活的HNH结构域阻碍的CRISPR-Cas9转切割活性
为什么微小的DNA切割重要
CRISPR-Cas9以其作为可在指定位点切割DNA的分子手术刀而闻名,但这种工具还有第二种不那么被注意到的行为:一旦被激活,它也可以啃噬附近的其他遗传物质。理解这种“附带”切割何时开启或关闭,对于开发更安全的基因编辑疗法和更灵敏的诊断测试至关重要。本研究解析了决定Cas9是安静地完成预期切割,还是同时开始切割零散单链DNA的Cas9–DNA–RNA复合物的物理特征。
CRISPR剪刀如何启动
为了发挥作用,Cas9结合一段短的引导RNA,引导其识别基因组中的匹配DNA序列。当Cas9找到目标时,引导RNA与一条DNA链配对,使两条链分开,形成称为R-环的DNA–RNA杂交区域。在其经典作用中,Cas9随后在该位点切断双链DNA。但最近的研究显示,一旦Cas9以这种方式被激活,其RuvC切割结构域也能切割溶液中不相关的单链DNA,例如一段多T序列。作者旨在探明:目标DNA和引导RNA的哪些精确几何和结构特征会使这种附带活性强、弱或消失?
短靶 vs 长靶:给Cas9留出活动空间
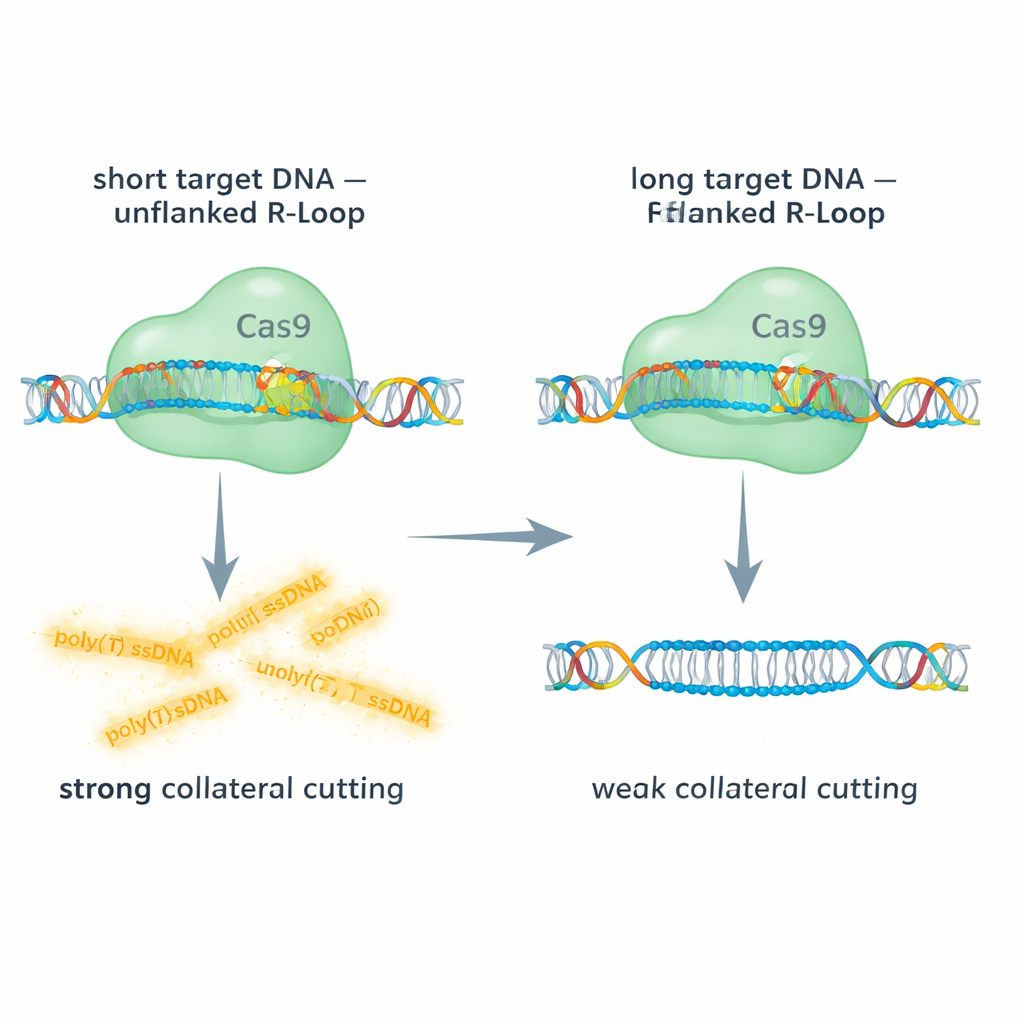
研究团队比较了Cas9在短双链DNA和长双链DNA靶上的行为,使用荧光读出同时跟踪靶向切割和对单链DNA探针的附带切割。对短DNA靶点而言,引导RNA的5′端处的R-环是“无侧翼”的——在杂交区域之外没有额外的双链DNA。在这种情况下,Cas9对单链DNA表现出强烈的附带活性。相比之下,当使用较长的DNA片段、在R-环两侧留有额外的双链DNA时,附带切割急剧下降,有时约降低90%,尽管主要的靶向切割仍发生。针对长单链DNA(彻底移除R-环)则在很大程度上恢复了附带活性。这些比较表明,位于R-环旁的双链“帽盖”使复合物变得更刚性,并在物理上阻碍了RuvC结构域接触或产生切割其它单链所需的灵活性。
通过引导长度与错配微调
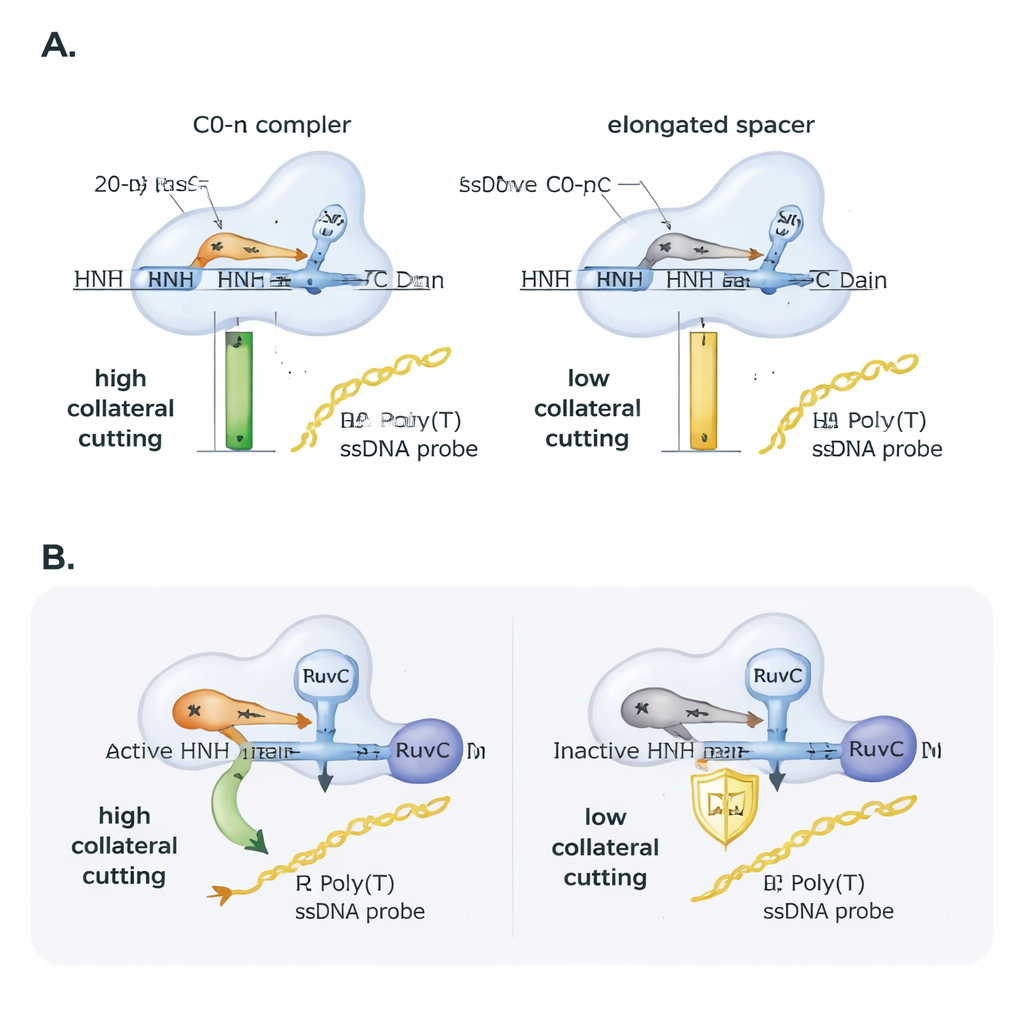
研究者接着探讨了引导RNA自身如何调节这种行为。他们在引导和目标DNA之间引入微小的错配,并跟踪Cas9的切割效率。主要的靶向切割对许多单碱基错配具有耐受性,但附带切割更脆弱,并且强烈依赖错配出现的位置,凸显了其敏感性。随后,他们系统性地将引导RNA的间隔区延长,超过常规的20个核苷酸。尽管Cas9仍能结合并切割目标DNA,附带活性随着间隔区长度增加几乎呈线性下降:仅增加两个碱基就使附带活性约减半,增加四个碱基则进一步降低。在使用SARS-CoV-2遗传物质的实用测试中,只有设计成与标淮长度引导配对并产生无侧翼R-环的DNA扩增产物才给出强烈的附带信号,这凸显了引物和引导设计如何决定基于CRISPR的检测方案的成败。
幕后的一位关键辅助结构域
Cas9有两个切割结构域:RuvC和HNH。既往工作将附带切割直接归因于RuvC,但本研究显示HNH仍然重要。当作者使用HNH结构域失活的Cas9变体时,附带活性骤降,尽管对目标的结合和切裂行为仍然存在。有趣的是,如果他们提供给Cas9一个已经在一条链上有切口的DNA靶点,失活HNH版本会恢复类似于正常酶的附带切割。这表明HNH的作用部分是机械性的:通过切割或松动被靶向的那一链,HNH帮助蛋白进入一种构象,使RuvC更容易接触附近的单链DNA。对现有三维结构模型的分析支持这一观点,显示无侧翼R-环和标准长度引导让RNA的5′端贴靠在Cas9上并将催化区定位得当,而有侧翼的R-环和延长的引导则使蛋白更紧密地堆积,可能屏蔽RuvC位点以阻止对零散单链的切割。
这对未来工具意味着什么
对非专业读者而言,最重要的信息是Cas9的行为不是非黑即白的:微小的几何细节——DNA延伸的距离、引导的长度以及辅助结构域能否完成其切割——共同决定了酶是专注于其主要任务还是同时破坏附近的单链。留下无侧翼R-环的短靶、标准的20碱基引导和活性的HNH结构域共同促进强烈的附带切割;长侧翼DNA、拉长的引导或失活的HNH结构域则抑制它们。这些见解为研究人员提供了更精确的调节手段,帮助他们设计能避免不良附带损伤的更安全基因编辑系统,或有意利用该附带活性以检测微量病毒或遗传物质的更强大诊断方法。
引用: Montagud-Martínez, R., Ruiz, R., Baldanta, S. et al. CRISPR-Cas9 trans-cleavage is hindered by a flanked R-loop, an elongated spacer, and an inactive HNH domain. Nat Commun 17, 1998 (2026). https://doi.org/10.1038/s41467-026-68789-3
关键词: CRISPR-Cas9, 附带切割, R-环, 引导RNA间隔区, 核酸诊断