Clear Sky Science · zh
NatA在核糖体肽链通道出口处参与多因子复合体
细胞如何在新生蛋白产生时进行微调
每一秒,你的细胞都在被称为核糖体的小型机器上合成数千种新蛋白。当每条蛋白链从核糖体伸出时,它必须被修剪、标记并正确折叠,否则可能发生功能异常并导致疾病。该研究关注一种关键的标记系统——称为N端乙酰化的修饰,并展示了核心酶复合体NatA如何与若干伙伴在新生蛋白离开核糖体的地方协同工作。理解这种协同有助于解释细胞如何保持其蛋白质工厂的正常运行。
重要的微小化学标签
大多数蛋白质的起始残基是相同的第一个氨基酸——甲硫氨酸。通常,这个起始的甲硫氨酸会被切除,并被一种称为乙酰基的小化学标签取代。这个加在蛋白质最前端(N端)的标签可以影响蛋白的寿命、在细胞内的位置以及功能。在核糖体的出口通道处,有两类主要酶负责这一最初的改造:去除起始甲硫氨酸的甲硫氨酸氨肽酶(MAPs),以及添加N端乙酰基的N端乙酰转移酶(NATs)。在这些NAT中,NatA是人类细胞中的主力,可能修饰近40%的所有蛋白。由于许多蛋白同时被合成,细胞必须组织这些酶以便修剪和标记既快速又按正确顺序发生。
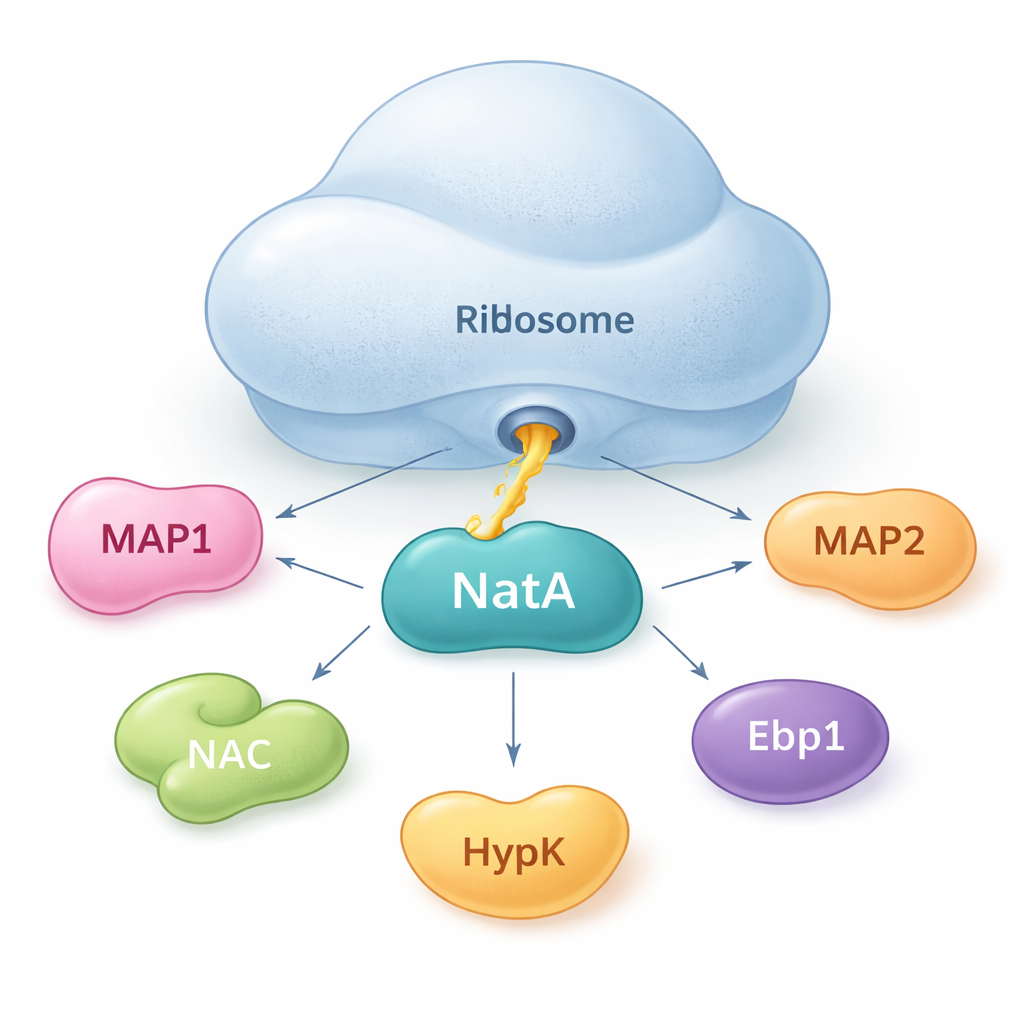
NatA作为蛋白辅助因子的汇聚点
作者表明NatA并非单独起作用。相反,它表现为一个枢纽,将多种辅助蛋白在核糖体上或游离于核糖体外聚集在一起。通过在溶液中进行敏感的结合测量,他们发现即便在没有核糖体的情况下,NatA也能与MAP1、新生肽链相关复合体(NAC)、调节蛋白HypK以及另一种酶Naa50形成高亲和力的复合体。NAC可以将NatA与MAP1连接起来,使切除和乙酰化步骤在同一组装体内相互衔接。然而,通常抑制NatA活性的HypK能阻止NAC结合。这表明细胞可能根据需要在更活跃的、与NAC相连的状态和受限的、与HypK结合的状态之间切换NatA。
在通道出口处的第二个对接位点
通过使用冷冻电子显微镜(一种能够以近原子分辨率成像大分子的技术),研究人员发现NatA可以以两种不同的位置与核糖体结合。一个位点是先前已知的,位于通道出口稍远处。新发现的“近端”位点将NatA的催化核心置于非常靠近新生肽链出现的位置,缩短了肽链被修饰所需经过的距离。有趣的是,这两个位置可以同时被占据,这意味着同一核糖体上可以存在两个NatA复合体。更远的那个拷贝充当支架和锚定点,而近端的拷贝则处于最佳位置来标记新生蛋白。两个NatA分子之间也存在接触,表明NatA能够将自身的复制体协调为多酶团队。
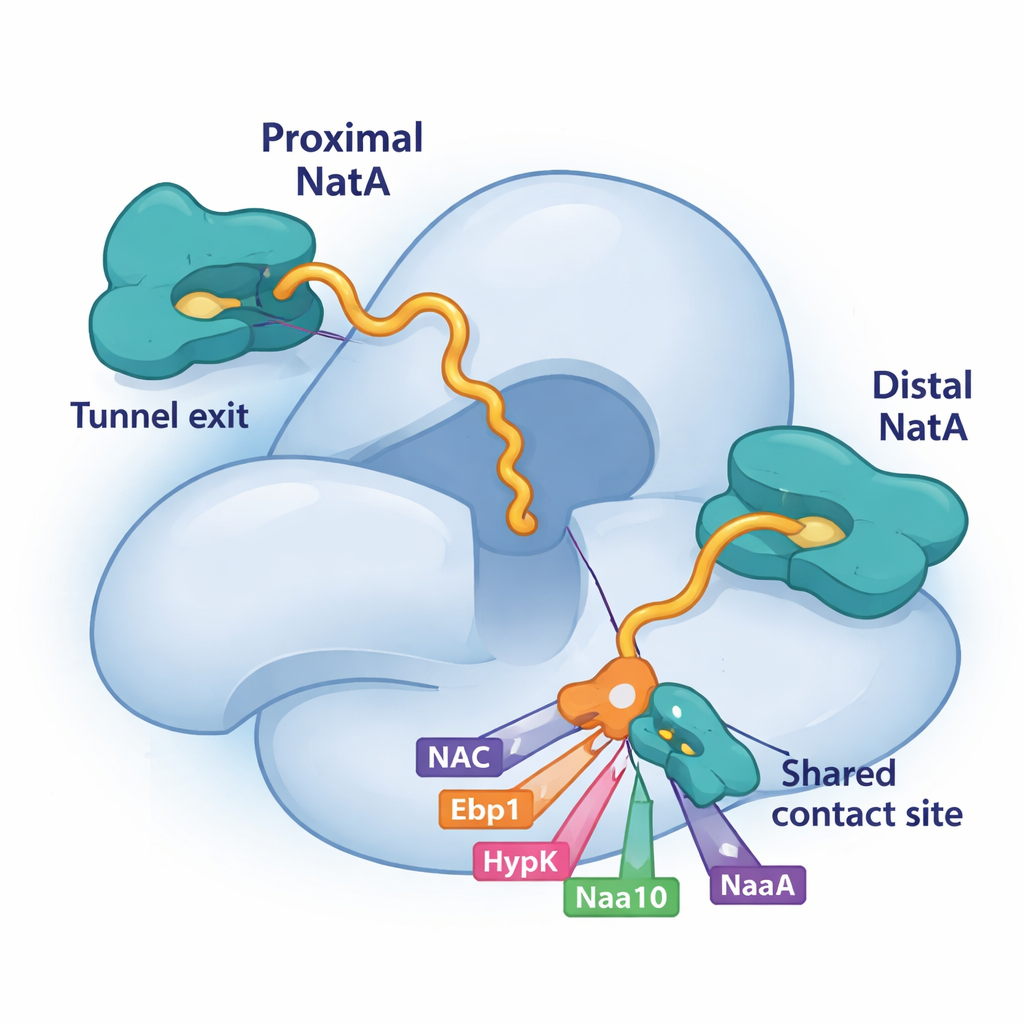
对NatA上共享停靠位的竞争
这幅拼图的关键是一段位于大NatA亚基Naa15上的小沟槽。研究显示,四种不同的与核糖体相关的因子——NAC、HypK、Ebp1,甚至NatA自身催化亚基Naa10的一个尾部片段——都使用短螺旋钩住Naa15上完全相同的补丁。因为它们都依赖这个共享的停靠位,所以必须互相竞争。当HypK占据该位点时,它不仅抑制NatA的活性,还阻止NatA与NAC配对或形成NatA–NatA二聚体。当NAC、类酶Ebp1或近端的Naa10占据该位点时,它们可以重塑NatA在核糖体上的位置或连接方式。这种竞争性结合为细胞提供了一种灵活机制,以决定在任何时刻哪些伙伴会围绕NatA组装。
作为交通调控者的类酶
蛋白Ebp1尤其引人注意。它类似于去除甲硫氨酸的酶之一,但缺乏催化活性;因此被称为“类酶”。先前的工作表明Ebp1可以位于靠近通道出口的核糖体上并夹住一段长的RNA。在本研究中,作者发现当NatA加入核糖体时,Ebp1会改变位置,放开RNA,转而使用其自身的螺旋占据Naa15上与NAC和HypK相同的结合位点。这种重排表明Ebp1可以充当占位者或组织者:它能塑造局部RNA环境,然后将控制权交给像MAPs和NatA这样的活性酶,而自身并不直接执行化学反应。
为何这种分子级的“人群管理”重要
对非专业读者来说,关于螺旋和结合位点的细节可能听起来抽象,但结论很简单:细胞在蛋白质诞生处运行着高度编排的、多步骤的质量控制系统。NatA位于该系统的中心,能够根据哪些因子赢得关键对接补丁的访问权限以及NatA占据哪个核糖体位点来招募或释放不同的伙伴。这个灵活的网络有助于确保成千上万种不同蛋白的剪切和乙酰化以正确的时序和顺序发生。由于N端加工错误与发育障碍、神经退行性疾病和癌症相关,绘制出NatA及其伙伴如何组装的图谱,为研究人员提供了更清晰的蓝图,说明早期蛋白加工如何被调控——以及当其出错时如何作为靶点进行干预。
引用: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
关键词: 蛋白质质量控制, N端乙酰化, 核糖体通道出口, NatA复合体, 共翻译修饰