Clear Sky Science · zh
植物岩藻糖基转移酶FUT11通过短暂的氧杂碳阳离子中间体机制扭曲糖受体以催化反应
植物如何微调蛋白上的糖链
无论是我们细胞内的蛋白,还是植物中的蛋白,常被复杂的糖链修饰,这些糖链如同条形码,决定蛋白如何折叠、寿命以及能与哪些配体结合。本研究聚焦一种植物酶FUT11,它将一种小糖——岩藻糖,添加到这些糖链上。通过在原子水平揭示FUT11的工作方式,作者发现了一个令人惊讶的伎俩:酶短暂地将其糖受体弯曲变形,从而推动一个困难的化学步骤。理解这一过程不仅对基础生物学重要,也有助于设计更安全的植物产药物,避免在人体中触发不期望的免疫反应。
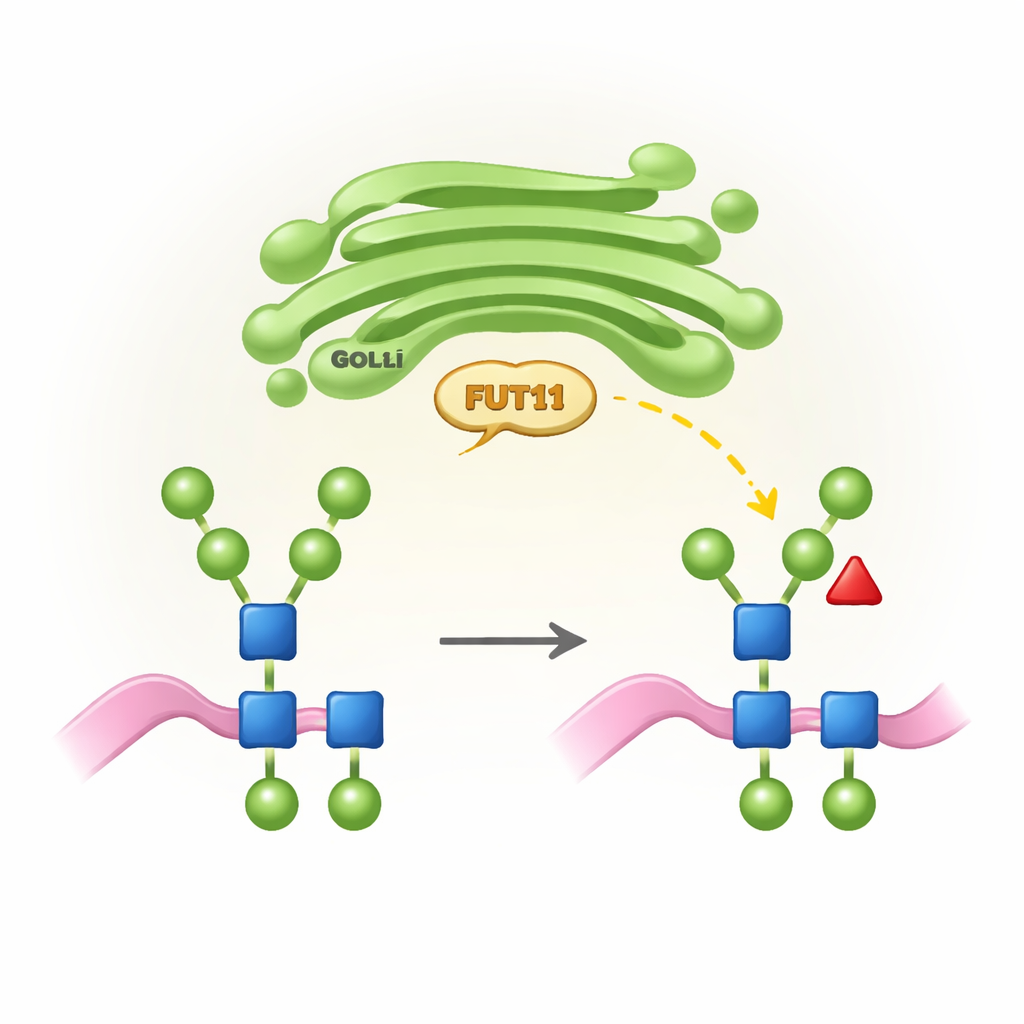
植物特有的糖标签及其重要性
所有高等生物都使用一种称为N-糖基化的过程,将糖链(N-寡糖)连接到蛋白的特定位置。在动物细胞中,这些糖链在高尔基体中被修饰为复杂结构,常以唾液酸为终端并在核心的特定位点带有一个岩藻糖。而植物遵循不同的“设计规则”:其N-寡糖通常缺少唾液酸,但在另一个位置(称为 β1,3)携带核心岩藻糖,并额外带有一个木糖。这些植物特有的特征对正常生长和生殖至关重要,但在人类免疫系统看来可能被识别为外来物。FUT11是将该核心岩藻糖接上的关键植物酶之一,其活性既影响植物发育,也决定植物生产的治疗性蛋白在人体中的免疫学表现。
绘制FUT11能作用于复杂糖枝的位点
为了弄清FUT11识别的底物,研究人员在包含144种不同N-寡糖结构的微阵列上测试了该酶。他们发现FUT11对糖树的一条分支——所谓的 β1,3 臂——具有较高选择性:该臂必须携带特定的构件(末端的乙酰氨基葡糖,GlcNAc)才能发生反应。同时,FUT11对其他修饰较为宽容:当中央甘露糖携带植物特有的木糖,甚至当核心上的哺乳动物位置已有岩藻糖时,酶仍然能工作。相反的那条分支(β1,6)大多暴露于溶剂,仅与酶形成弱相互作用,这解释了FUT11能够容纳该处各种修饰的原因。这些结合偏好有助于解释植物为何生成特征性的N-寡糖集合,并表明在为生物技术改造植物细胞时可如何利用或避免FUT11的作用。
抓取并定位糖分子的独特结构设计
研究团队通过X射线晶体学解析了FUT11与其糖供体(GDP-岩藻糖)和N-寡糖受体复合体的三维结构。该酶呈双叶片的“GT-B”构架:一侧叶片包裹GDP-岩藻糖,而另一个异常复杂的受体叶片——包括一个植物特有的N端亚结构域——环绕并包裹N-寡糖。这个额外的亚结构域由二硫键连接到酶的其余部分,锚定寡糖的中间区域,并帮助将反应性的GlcNAc呈向供体。关键氨基酸的突变验证了它们的作用:改变单个谷氨酸(Glu158)会使活性消失,而改变两个相邻残基则在工程化的人类细胞中大幅削弱了岩藻糖化活性。这些结果将结构定格与细胞功能联系起来,明确指出酶中哪些部分对结合与催化是不可或缺的。
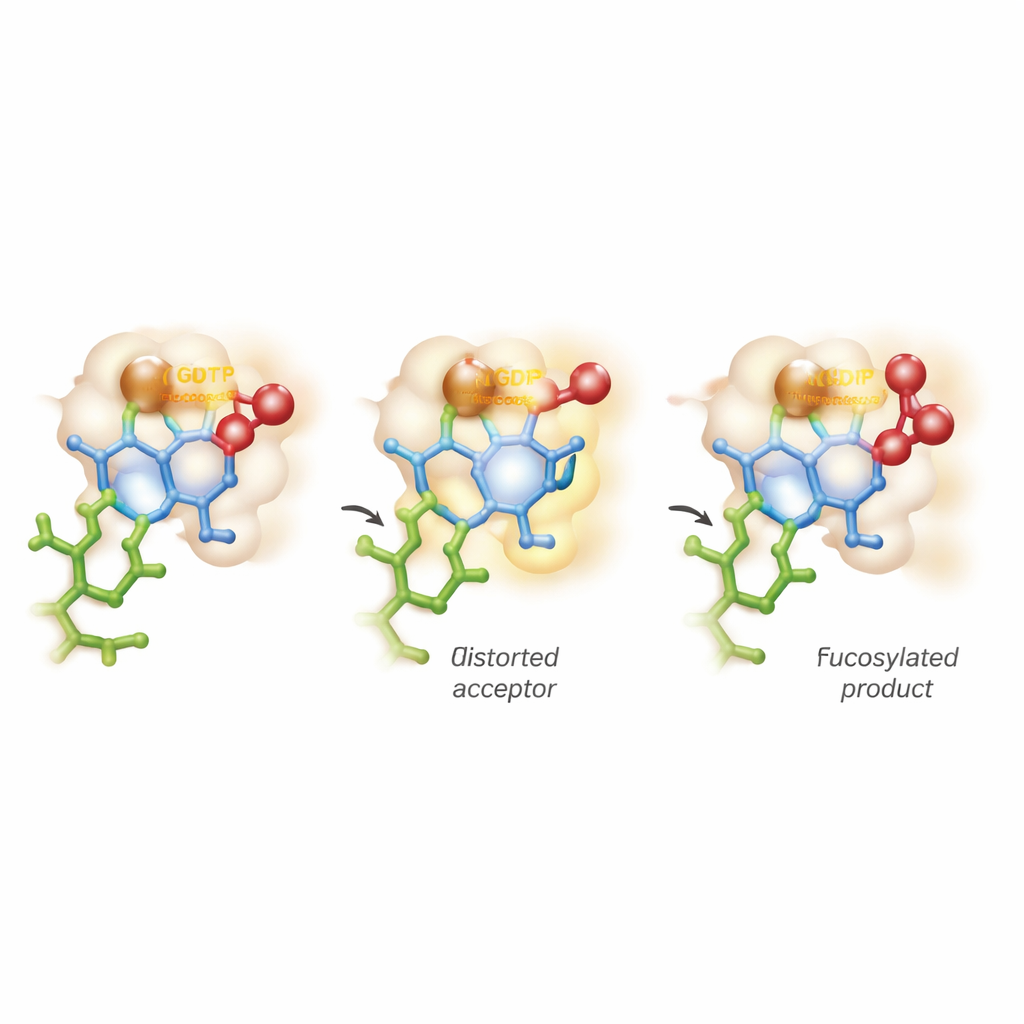
弯曲糖环并在两条反应路径间权衡
最引人注目的发现来自结合量子力学与分子动力学的高阶计算模拟。传统观点假定受体糖保持稳定的椅式构象,而酶仅激活供体。而在FUT11中,情况更为积极:由Glu158驱动的相互作用短暂扭曲了最内层GlcNAc环,使其进入一种不太舒适的扭曲构象。在这种受张力的姿态下,关键的羟基完美对准以进攻岩藻糖供体。计算揭示,随着与GDP的化学键断裂,一个短寿命的、带正电的“类氧杂碳阳离子”状态会出现在糖环上,然后新的键才完全形成到受体。这意味着反应并不能简单归入教科书上的SN1或SN2类别,而是在一个连续体上进行,以一种异步、近乎分步的方式完成。
隐含的柔性与进化回声
通过将FUT11与相关的人类酶FUT9比较,作者发现植物酶也能(尽管很弱)修饰另一类糖基序列(LacNAc),生成被称为Lewis X的结构。这种副反应在植物中很可能并不具有生物学重要性,因为植物中通常不见Lewis X,但它凸显了相似的蛋白骨架可在进化中被改造以适应不同的糖环境。研究表明FUT11及其同源物共享一种用于识别N-寡糖的模块化框架,通过细微调整来在植物核心与动物侧链之间改变特异性。
这种弯曲伎俩为何对科学与医学重要
综上所述,研究表明FUT11不仅仅把两个糖配对放到一起:它主动将受体糖弯曲到一个反应性构象,并通过一个短暂的带电中间体引导化学过程。对非专业读者而言,这意味着蛋白上的糖并非刚性的停靠位点,而是酶可以塑形的柔性参与者。这种关于“构象催化”的新观点有助于解释酶如何同时获得高速与选择性,并为重新设计糖基化通路提供蓝图。从实用角度看,确切了解FUT11如何识别并修饰植物N-寡糖,可指导作物与植物生产系统的工程改造,以最小化人类治疗用蛋白中的免疫原性糖型,或创造具有定制生物学特性的设计型糖蛋白。
引用: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
关键词: 植物糖基化, 岩藻糖基转移酶 FUT11, N-寡糖, 酶学机制, 糖工程