Clear Sky Science · zh
二聚体 OS9-SEL1L-HRD1 ERAD 核心复合体的结构基础及病理学含义
细胞清道夫在显微镜下
在我们每个细胞内部,一个繁忙的工厂将遗传信息转化为有功能的蛋白质。像任何工厂一样,错误也会发生。当蛋白质折叠错误时,它们会堵塞系统并促进疾病产生。本研究聚焦于细胞主要的质量控制机器之一——SEL1L‑HRD1 复合体,揭示其详尽的三维结构,并展示微小的基因变化如何破坏这一机械装置,从而可能导致人类疾病。
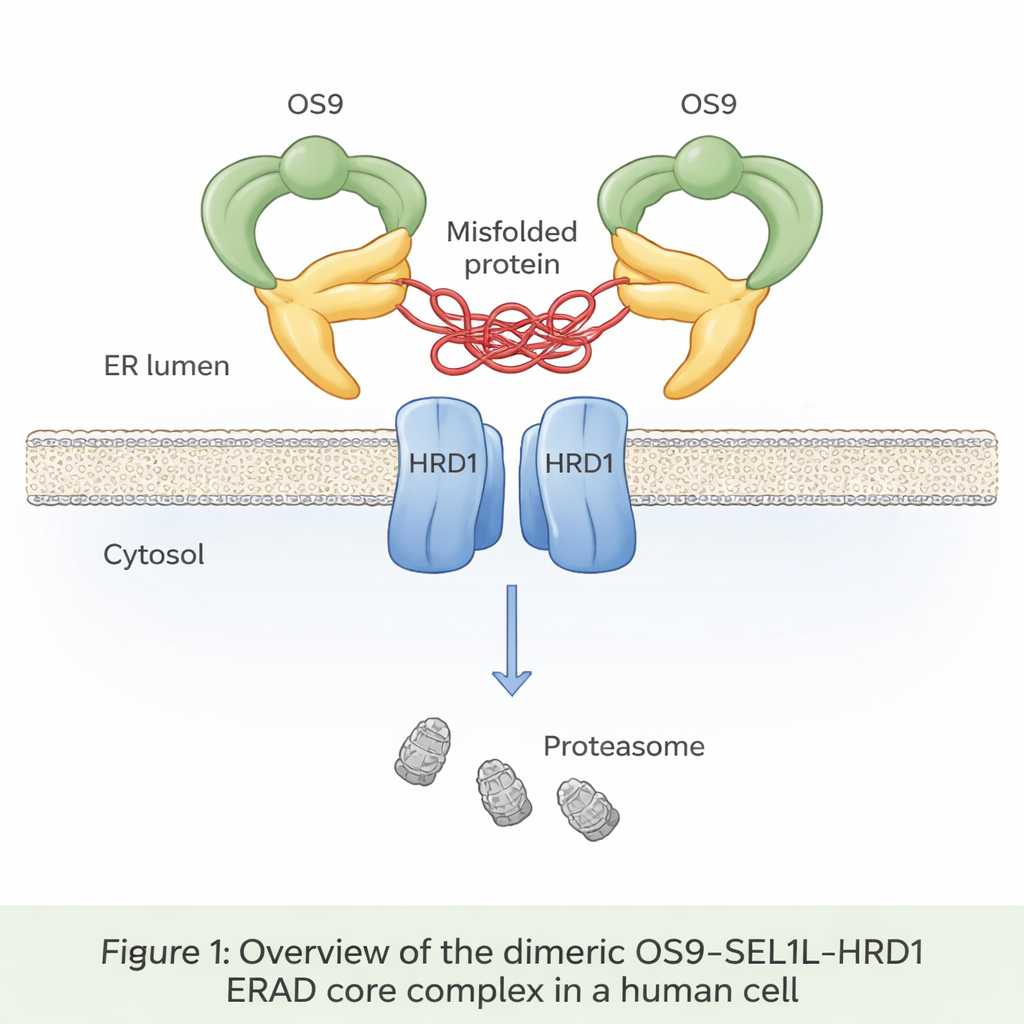
细胞内的隐形传送带
多达三分之一新合成的蛋白进入名为内质网(ER)的隔室,在那里接受折叠和检查。错误折叠的蛋白通常会被识别、从 ER 中拉回并在称为 ER‑相关降解(ERAD)的过程中被清除。在一种主要的 ERAD 通路核心有三种蛋白:OS9、SEL1L 和 HRD1。OS9 作为识别带糖基错误蛋白的感应器;SEL1L 提供支架作用;HRD1 则用小的泛素标记将注定被降解的蛋白标记出来,指引它们被细胞的废物处理单元——蛋白酶体所降解。然而直到现在,还没有人在原子级别上看到这三部分在人体细胞中如何组合在一起。
揭示核心机器的形态
作者使用冷冻电镜(cryo‑EM),这是一种可以在近原子分辨率下对快速冷冻的分子成像的技术,来观察从人类细胞纯化得到的 OS9‑SEL1L‑HRD1 复合体。他们发现该复合体形成二聚体——本质上是两个相同单元结合在一起——而不是保持单体形式。在 ER 腔侧(ER 的内部),两个 OS9 和两个 SEL1L 分子组装成类似蟹钳的环状结构,中央有一个开口,似乎用于抓取错误折叠的蛋白。在膜内,两条 HRD1 分子配对形成共享的通道。这种排列将“钳口”直接置于 HRD1 的通道之上,形成一条连续通路,使错误折叠的蛋白能够从 ER 腔穿过膜,并朝向胞质中的降解路径移动。
微小变化如何破坏大系统
鉴于在患有严重神经发育等疾病的患者中发现了 SEL1L 和 HRD1 的突变,研究团队将若干与疾病相关的变体映射到他们的结构上,并在细胞中测试这些变体的行为。两个 SEL1L 突变,G585D 和 S658P,分别位于与 OS9 和 HRD1 接触的位点。在细胞实验中,G585D 几乎消除了 SEL1L 与 OS9 的结合能力,而 S658P 则大大削弱了其与 HRD1 的结合;二者同时存在时,基本上破坏了核心复合体,但并未影响其他结合伙伴。因此,细胞在给一个错误折叠的激素前体打标并清除它方面遇到困难,使得有缺陷的蛋白得以滞留。
膜通道中的致病突变
结构还显示 HRD1 的跨膜段 3 是两条 HRD1 分子相互会合形成通道的关键界面。研究者在特定位点设计了半胱氨酸“把手”并使用化学交联,证实这些区域在活细胞中确实紧密接触,证明 HRD1 在体内确实形成二聚体。当他们扰动该界面上的一个高度保守的残基(T93)时,二聚体解体且 ERAD 活性崩溃,尽管该复合体仍能与 OS9 和 SEL1L 组装在一起。随后他们检查了一种新发现的患者变体 HRD1 A91D,该变体在一名有心肺问题的儿童中被发现。该变化也位于二聚体界面,约将 HRD1 二聚化能力削减一半,并严重损害错误折叠蛋白的清除,同样不会破坏整体伙伴结合。
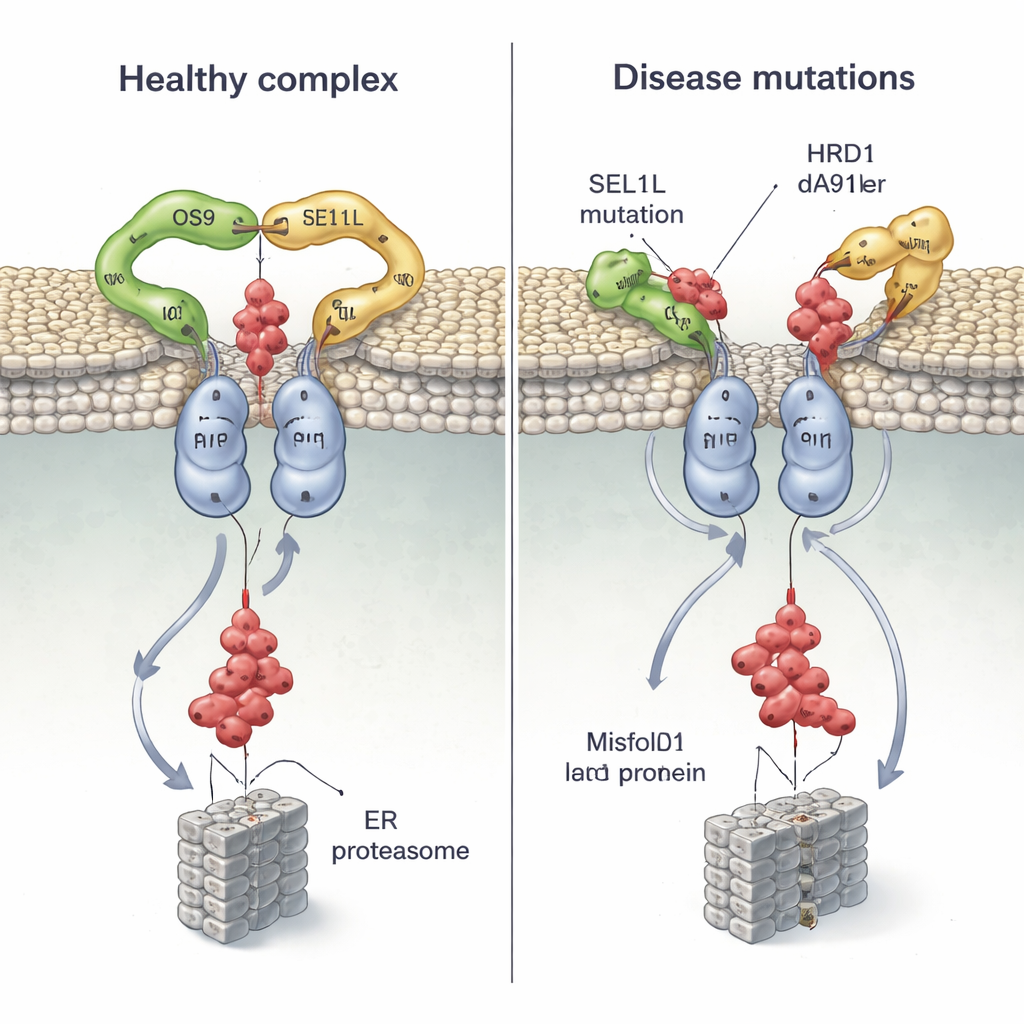
对蛋白质质量控制与疾病的新视角
通过将结构生物学与细胞水平的测试结合,本研究表明 OS9‑SEL1L‑HRD1 复合体作为一台成对的二聚体机器运作:一个类似钳子的捕捉装置与一个共享通道相连,将有缺陷的蛋白从 ER 运输出去。那些放松钳口或破坏 HRD1 成对稳定性的突变,并非只是微调效率——它们可以彻底卡住系统,使受损蛋白积累并促成人体疾病。对非专业读者而言,关键的信息是:即便是我们 DNA 中的单个字母变化,也能微妙地扭曲重要细胞机器的形状,进而对大脑发育、免疫和器官功能产生深远影响。
引用: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
关键词: 蛋白质质量控制, 内质网, ERAD, SEL1L-HRD1 复合体, 蛋白质错误折叠