Clear Sky Science · zh
光酶催化促进的立体选择性氰基迁移反应
移动微小部件以产生重大影响
化学家常常希望像工程师重新定位机器中的齿轮那样调整分子——在不重建整体结构的情况下移动一个小部分。本文展示了科学家如何利用光和专门的酶,将氰基这一微小却功能强大的化学手柄,从分子的一处温和地滑移到另一处。其结果是构建药物和高端材料所需分子的一种更精确、更可持续的方法。
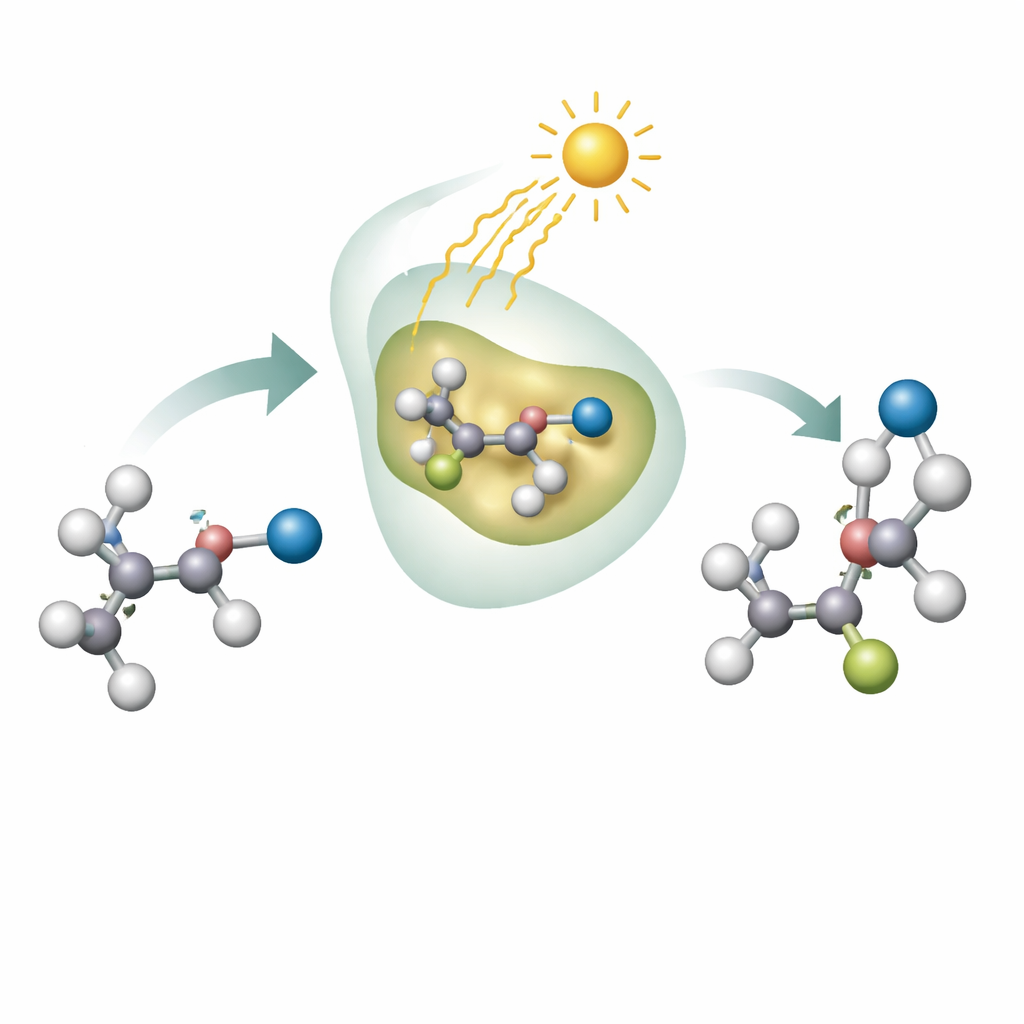
为什么移动一个小基团很重要
有机分子的行为在很大程度上由其功能基团决定——这些原子小簇像控制开关一样工作。即便将这样的基团沿碳链移动一小段距离,也会显著改变分子在体内或材料中的表现。化学家们知道如何实现这些迁移,尤其是利用自由基反应,但通常难以控制产物的“手性”。像左右手一样,许多分子存在镜像异构体,而通常只有其中一个对用途或安全性合适。到目前为止,在这些基团迁移反应中获得期望手性一直非常困难。
协同利用酶与光
作者将酶与光的优势结合起来解决了这一问题。他们的研究集中在将氰基(CN 单元)沿碳链在称为烷基腈的分子中移动,烷基腈是可转化为多种有用功能的重要构件。团队使用了黄素依赖型酶,这是一类在生物细胞中天然处理氧化还原化学的常见蛋白。当酶内的黄素辅酶吸收蓝光时,会进入激发态,足以切断起始分子上的碘原子,产生高度活泼的自由基。在酶的狭窄结合口袋内,这个自由基能接近氰基,引发重排使其重新定向,随后通过黄素向自由基转移氢原子将其“关闭”,实现受控的终止步骤。
按需生成单一手性异构体
这项工作的一个关键成就是,酶不仅实现了氰基的迁移,还对手性具有优异的控制力。通过筛选天然酶并对其进行改良,研究者鉴定出能够以极高纯度生成一种镜像异构体的体系,以及偏好另一种镜像异构体的体系。他们证明,不同芳香环和侧链的多种起始分子都可以在光驱动的氰基迁移中保持对单一手性的强烈偏好。对起始材料进行电子效应微调——添加给电子或拉电子基团——进一步影响优选手性的形成程度,揭示了反应性底层平衡的细微性。
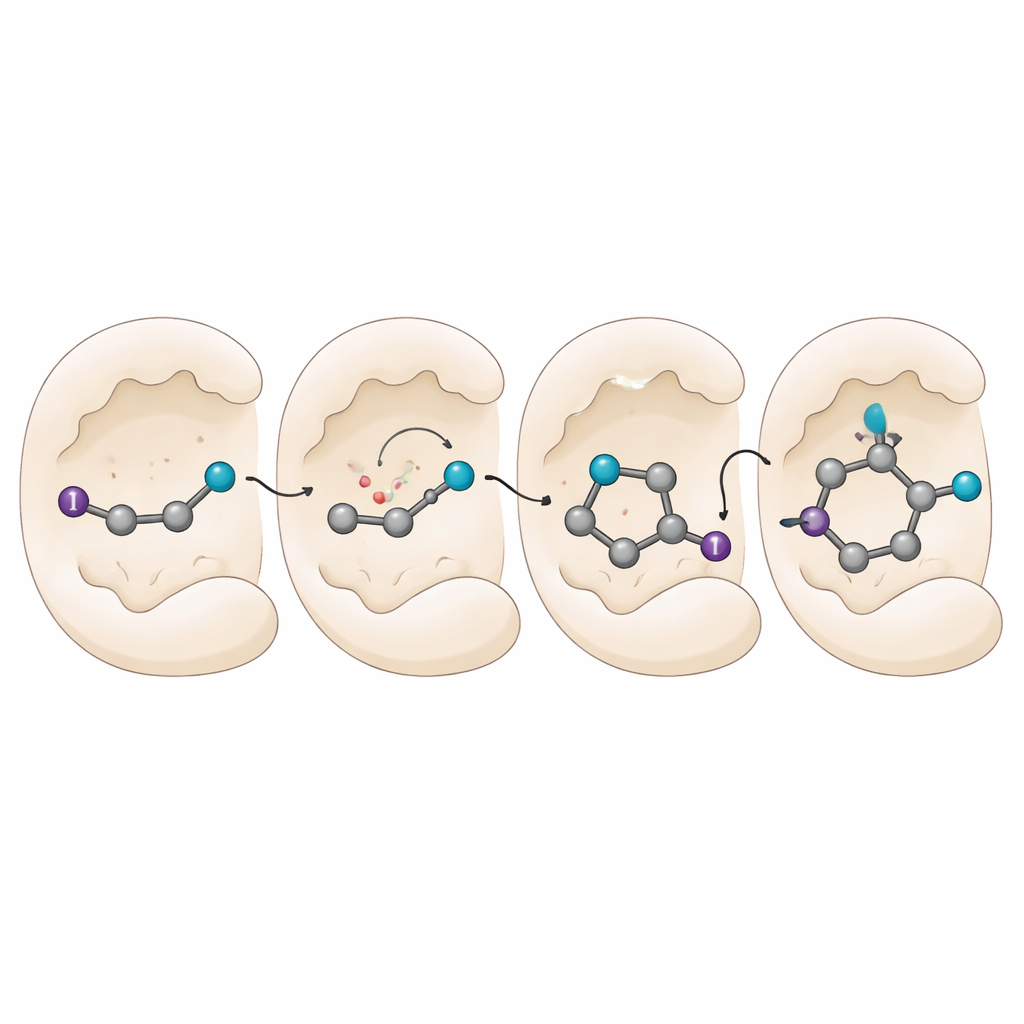
窥视分子机器的内部
为理解酶如何施加如此精确的控制,团队进行了机理实验和计算机模拟。捕捉自由基的实验证实该过程确实经过自由基中间体,但大部分化学反应被酶内部所屏蔽,外部的捕捉剂难以干扰。光学测量显示,酶与底物形成了一种特殊的光吸收复合体,有助于反应的起始。对酶—自由基复合体的模拟显示,氰基被特定氨基酸锚定,而分子的其余部分则可以旋转到有利的构象。底物的芳香环与某些氨基酸之间的微弱堆积相互作用,在最终氢原子给与时使自由基的某一面更有利,从而锁定了产物的镜像形式。
构建更好分子的全新工具
最终,这项研究引入了一种以精巧手法重排分子的全新方式。通过使用光激活酶来引导基于自由基的氰基迁移,作者展示了在移动功能基团的同时精确决定产物的镜像构型是可行的。对于药物发现和材料科学而言,这提供了一条灵活且更环保的途径来获得微调的分子结构,扩展了化学家设计更安全药物与更智能材料时可用的工具箱。
引用: Duan, X., Xu, J., Bai, R. et al. Stereoselective cyano translocation reaction enabled by photoenzymatic catalysis. Nat Commun 17, 2133 (2026). https://doi.org/10.1038/s41467-026-68776-8
关键词: 光酶催化, 功能基团迁移, 氰基迁移, 酶的立体控制, 烷基腈