Clear Sky Science · zh
模拟颗粒酶B的纳米酶用于纳米囊靶向抗癌应用
重塑体内的癌细胞杀手
我们的免疫系统拥有可以追踪并杀死癌细胞的专门细胞,但在许多实体肿瘤中,它们难以渗透、容易疲惫,或会错误攻击健康组织。这项研究描述了一种完全人工的纳米级系统,模仿免疫系统中最强有力武器之一,并将其直接送入肿瘤细胞。该工作重要之处在于它指向了那种行为类似活体免疫细胞、但由稳定且可控材料制成而非脆弱人源细胞的癌症治疗方法。
把天然刺客变成设计蓝图
细胞毒性T细胞(一类白细胞)使用一种名为颗粒酶B的酶来杀死危险细胞。一旦识别到目标,它们就在目标膜上打出小孔并注入颗粒酶B,后者启动细胞内的自杀程序。这一策略也是现代疗法(如CAR‑T细胞疗法)背后的原理,后者能治愈某些血液肿瘤。然而在实体瘤中,CAR‑T细胞常常失败,因为它们无法到达所有肿瘤区域、变得耗竭,或误伤健康组织。作者们提出能否构建一种非生物的纳米装置,复制颗粒酶B的关键功能——触发细胞的自毁机制——而无需依赖活体T细胞。
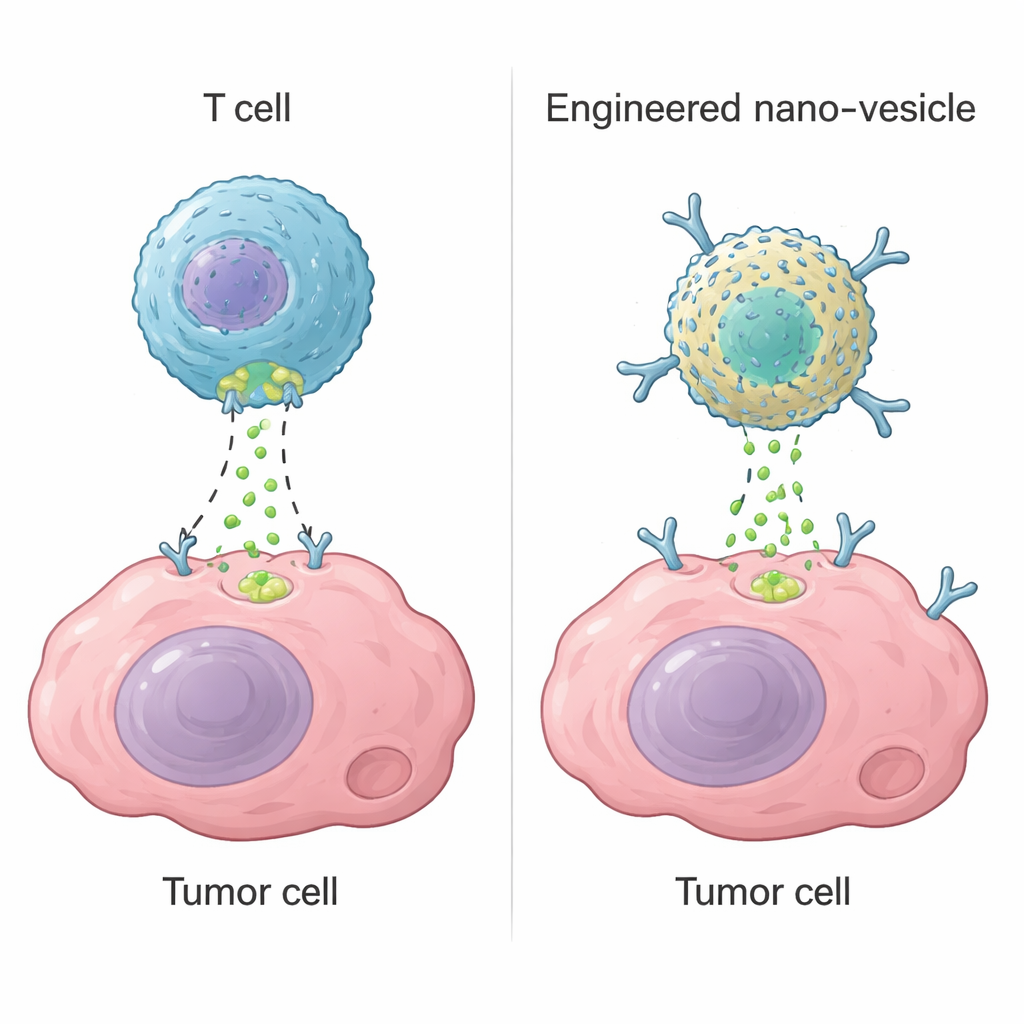
设计微小的人工酶
研究团队以铁蛋白为起点,这是一种天然蛋白,能形成空心纳米笼且易于大量制备。通过将钯离子结合到人源铁蛋白上,他们创造出具有酶样行为的“纳米酶”。精细的结构学研究显示,两枚钯原子嵌入蛋白表面的特定口袋,由含硫和含氮的氨基酸以及水分子固定在位。这个双核金属中心充当人工切割位点,能识别颗粒酶B在关键靶标(即半胱天冬酶‑3)上使用的相同短肽序列。在体外试验中,该纳米酶有效地在正确位置切割半胱天冬酶‑3并使其被激活,同时对高度相关的蛋白保持选择性。该人工酶的效率略低于天然颗粒酶B,但在较宽的温度和酸碱度范围内表现出明显更高的稳定性。
将纳米酶偷运入肿瘤细胞
像颗粒酶B这样的酶只有进入肿瘤细胞内部才有效。为此,研究者将其钯‑铁蛋白纳米酶封装在脂质纳米囊中——由类脂分子构成的小而柔软的囊泡。然后他们用识别HER2(一种在乳腺癌和膀胱癌细胞上常常过度表达的蛋白)的抗体片段对这些囊泡进行修饰。当这些伪装的囊泡遇到富含HER2的细胞时,会紧密结合并与细胞膜融合,使纳米酶货物直接滑入细胞质,而不是被困在细胞的回收降解隔室中。显微镜显示囊泡在细胞表面滞留的同时,纳米酶向细胞内部扩散,为从内而外的可控自毁奠定了基础。
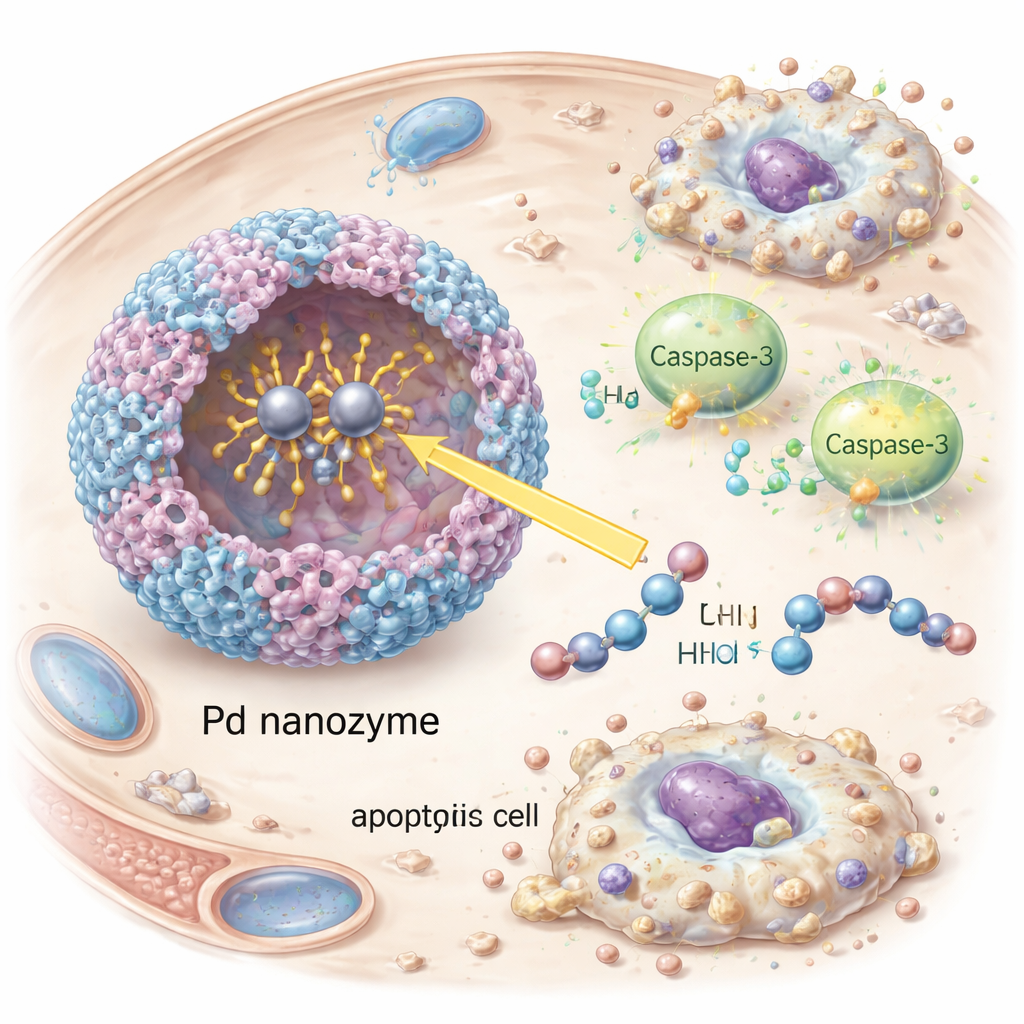
精确触发癌细胞自杀
进入癌细胞后,纳米酶激活了作为程序性细胞死亡核心执行者的半胱天冬酶‑3。研究者观察到活化的半胱天冬酶‑3及其下游靶标PARP的出现,以及培养的HER2阳性肿瘤细胞中明显的凋亡特征——细胞缩小与碎裂。用RNA干扰沉默半胱天冬酶‑3会显著降低细胞死亡,证实该效应依赖于这一通路而非非特异性损伤。在携带HER2阳性肿瘤的小鼠模型中,带有抗体装饰的囊泡在血液中循环时间更长、更强地在肿瘤处富集,并比缺少靶向抗体或缺少纳米酶货物的囊泡更有效地减缓肿瘤生长。重要的是,接受治疗的动物未见明显体重下降、血液学异常或主要器官组织损伤,表明在这些早期试验中具有良好的安全性迹象。
这对未来癌症护理意味着什么
对非专业读者而言,核心信息是研究者构建了一个微小的非生物装置,其行为类似于我们免疫系统中关键的杀癌机制之一。他们没有改造活体T细胞,而是设计出一种稳定的纳米酶,能在肿瘤细胞内激活相同的自毁开关,并将其包裹在可识别特定癌症的智能递送外壳中。尽管在人类使用之前仍需大量工作,这一方法提供了一个灵活的平台:理论上,抗体涂层可以更换以瞄准其他肿瘤标志物,人工酶也可以进一步优化。该研究展示了通向无细胞免疫疗法的一条有前景途径——精心设计的纳米材料而非活体免疫细胞,用来追踪并摧毁实体肿瘤。
引用: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
关键词: 癌症纳米医学, 免疫治疗, 颗粒酶B, 纳米酶, HER2阳性肿瘤