Clear Sky Science · zh
同源细胞膜驱动的电化学微流控外泌体分析用于精准癌症诊断
把癌细胞自身的“护甲”变成诊断工具
包裹癌细胞的细胞膜上布满独特的分子“旗帜”。这项研究展示了科学家如何剥离这些护甲,将其铺展到微小的金属芯片上,然后用它从血液中捕获具有指示性的微粒。结果是一种高度灵敏的血液检测,可以揭示不仅是否存在乳腺癌,还能识别其亚型——这对选择合适治疗至关重要。
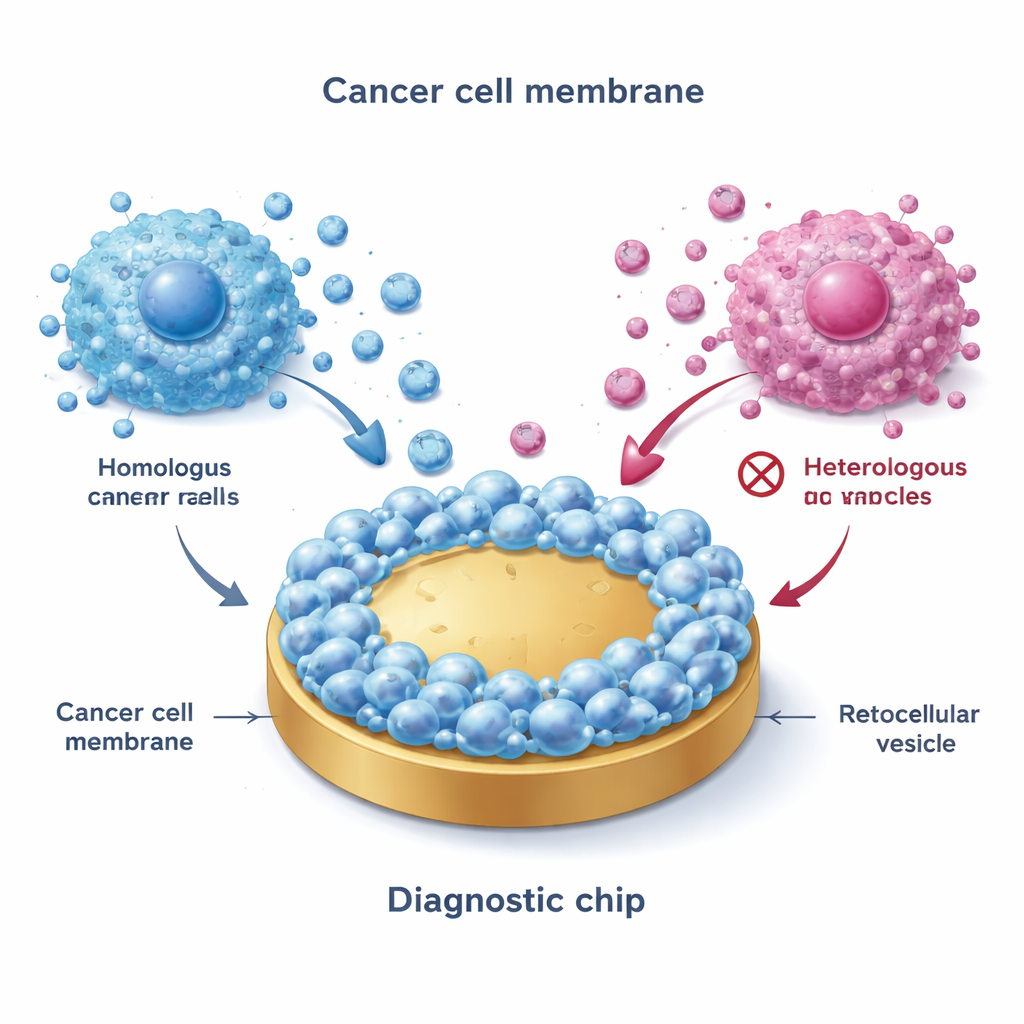
为何乳腺癌亚型很重要
乳腺癌并非单一疾病。肿瘤被分为多种亚型,例如雌激素受体阳性(ER+)、HER2 阳性和三阴性等,每种亚型对激素疗法、靶向药物或化疗的反应不同。如今,医生通常通过直接取肿瘤组织的活检来确定亚型。这一过程具有侵入性,不能频繁进行,并且可能错过疾病演进过程中出现的变化。能够随着时间跟踪这些亚型特征的血液检测,将使医生更早、更精确地调整治疗方案。
漂浮在血液中的微小信使
癌细胞不断向血液释放纳米尺度的囊泡,称为细胞外囊泡(EVs)。EVs 携带的蛋白质、脂质和遗传物质与其来源细胞非常相似,使它们成为“液体活检”的有力候选对象。但这也存在挑战:如果只关注一两种蛋白,来自不同乳腺癌亚型的 EVs 可能看起来非常相似。现有检测要么针对共有标志物——难以区分亚型,要么依赖复杂的基因学检测——速度慢且可能产生误导性结果。作者的目标是以一种简单、稳健的方式读取 EV 表面的更完整分子指纹。
构建仿生“渔网”
研究团队首先从代表主要亚型的培养乳腺癌细胞中提取细胞膜:ER+(如 MCF-7)、HER2 阳性和三阴性细胞。通过冻融过程,他们裂解细胞,分离出外膜,并将这些膜融合到平坦的金表面上。由此形成了一个“仿生界面”,近似模拟原始癌细胞的外表面。值得注意的是,当 EVs 在这些涂膜表面上流动时,只有来自配对或密切相关亚型的囊泡会强烈粘附——这一现象称为同源结合(homotypic binding)。先进的成像和电学测量证实,膜涂层表面更粗糙、亲水性更强、且比裸金更不容易发生非特异性吸附,使其适合在血液等复杂液体中进行高质量测量。
将囊泡捕获转化为电信号
为了把结合事件转换成可读信号,研究者瞄准了 EV 表面一种丰度较高的蛋白 CD47。他们通过一段短 DNA 桥将针对 CD47 的抗体连接到银纳米颗粒上,构建出微小的电活性标签。在膜涂层表面捕获到目标 EVs 后,这些标签会结合到被捕获囊泡上的 CD47。当暴露于酸性溶液并随后进行电化学测量时,银会产生清晰、易于量化的电流。该信号在宽范围的 EV 浓度内呈线性上升,灵敏度可达每毫升仅数百个囊泡——远超常见方法如 ELISA 或纳米颗粒追踪。每种癌细胞膜仅对其匹配的 EVs 产生强信号,即便在其它亚型囊泡、血小板或无关细胞存在的情况下也能保持选择性。
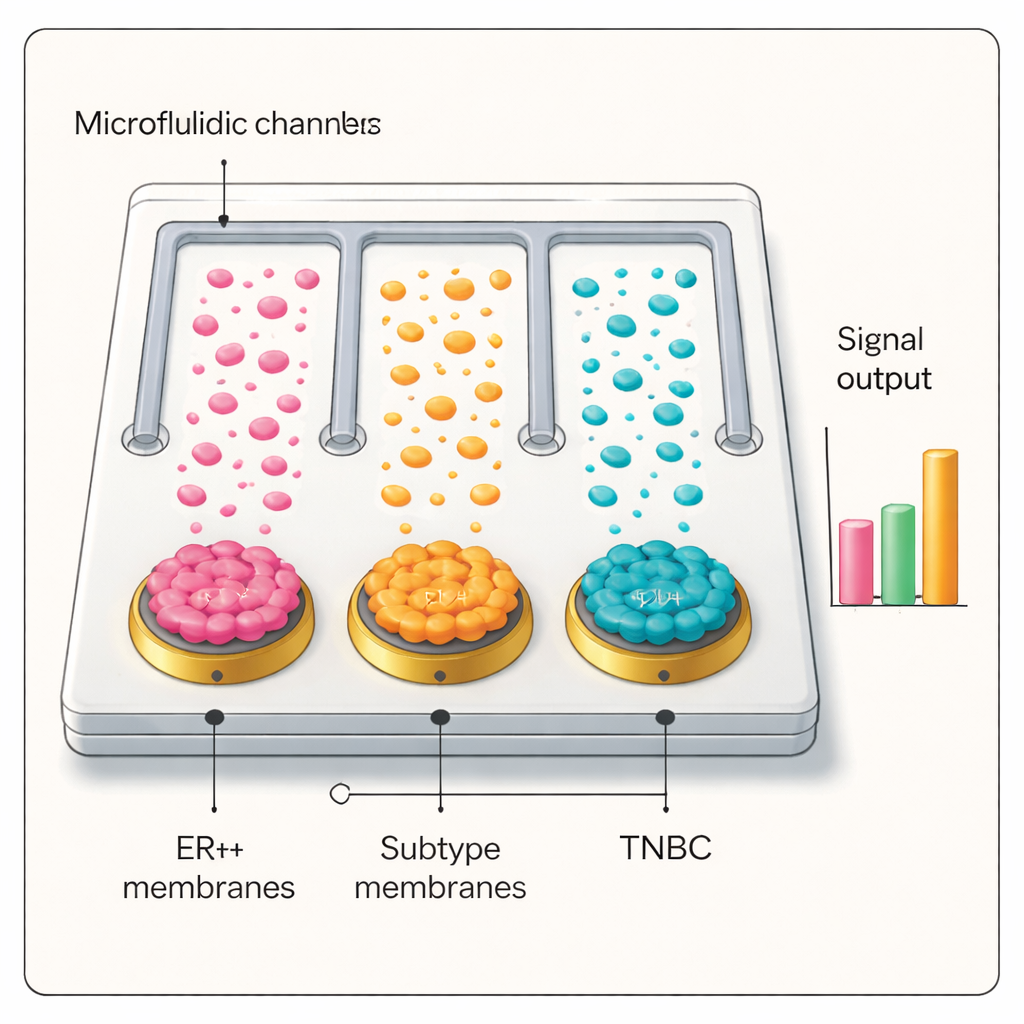
从实验台到患者血样
借助这一选择性且灵敏的界面,团队构建了一块微流控芯片,包含多条平行通道,每条通道涂有不同乳腺癌细胞的细胞膜,并设置了未涂层的对照通道。当患者血浆通过芯片并用银-抗体标签探测时,只有与患者肿瘤亚型匹配的通道产生高电信号。在对数十名受试者的盲测中——包括 ER+ 与三阴性乳腺癌患者、良性乳腺疾病患者、肺癌患者以及健康志愿者——该平台准确地区分了癌症与非癌症样本,并正确识别乳腺癌亚型。其诊断性能在许多情况下与标准病理相当或更优,并在病期分级与病情监测方面显示出潜力。
对未来癌症护理的意义
简而言之,研究者已将癌细胞的外壳变成了一种高度选择性的诱饵,用以捕获肿瘤释放到血液中的微小颗粒。通过读取哪条通道“发光”的电学特征,医生未来或能仅凭一滴血就判断不仅是否存在癌症,还能确定其类型。虽然该系统仍需进一步改进——例如增加更多标志物和膜类型、并整合智能数据分析——它指向了一个前景:常规的、创伤小的血检可以辅助个体化癌症治疗决策并监测肿瘤随时间的变化。
引用: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
关键词: 乳腺癌亚型, 液体活检, 细胞外囊泡, 微流控诊断, 细胞膜传感器