Clear Sky Science · zh
内皮细胞PDLIM5通过调节依赖ACTN1/ACTN4的肌动蛋白束形成促进箭头细胞丝状伪足形成与肿瘤血管生成
癌症如何劫持血管
没有促使邻近血管输送氧气和营养,癌症无法从一个小的细胞团扩大。这项研究揭示了血管内皮细胞中一个鲜为人知的蛋白如何帮助肿瘤长出新的、异常的分支。理解这一过程或许能开辟更聪明的治疗途径,既能饿死肿瘤,也能提高免疫疗法的疗效。
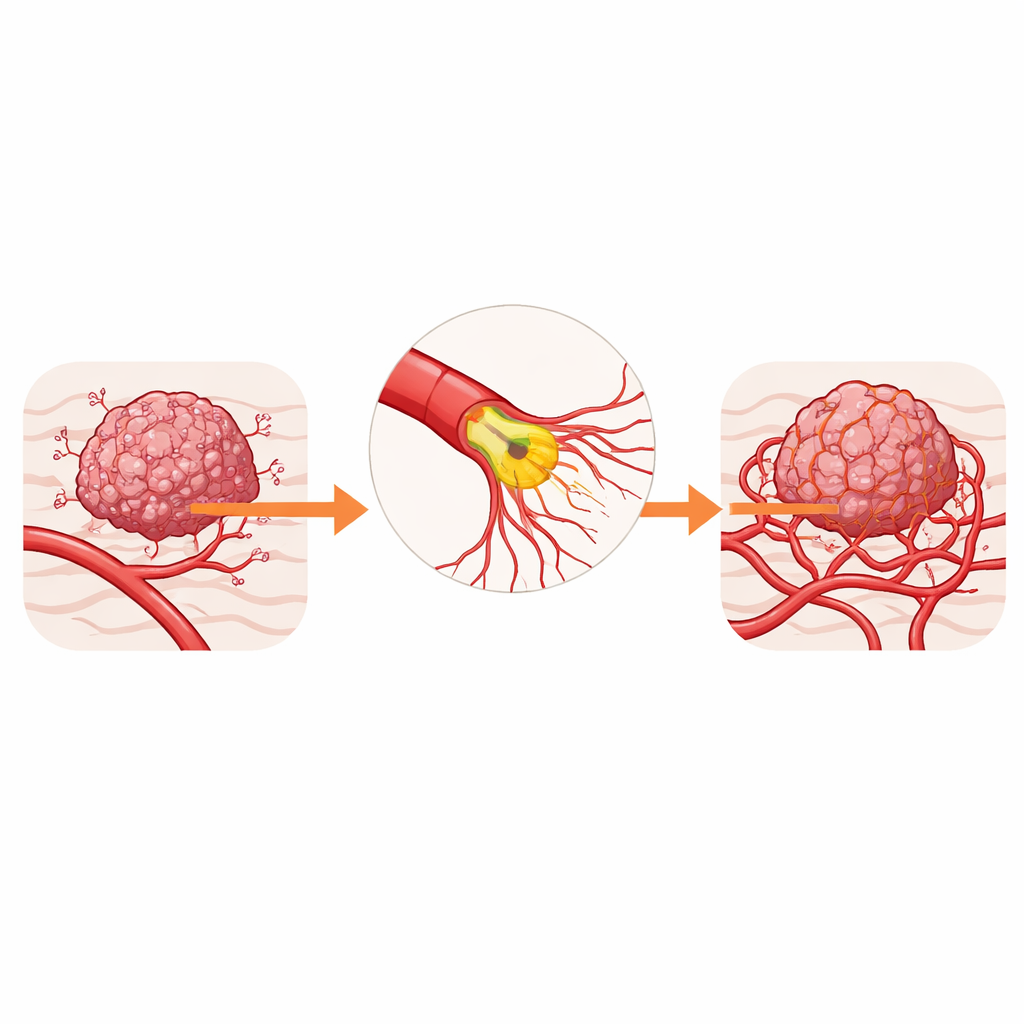
肿瘤血供的隐形建筑师
为肿瘤提供血液的血管由一种名为内皮细胞的专门细胞构成,它们衬里血管的内壁。在每个新血管分支的生长前端有一个“箭头细胞”,它会伸出称为丝状伪足的细长指状突起。这些突起感知来自肿瘤的化学信号,引导新芽朝向缺氧的区域。在许多癌症中,这种萌发过度活跃,形成渗漏且扭曲的血管,加剧缺氧,并使药物和免疫细胞更难到达肿瘤。
一种能强化萌发的蛋白
通过分析来自人类肺肿瘤的单个细胞,研究者发现与肿瘤相关的内皮细胞显著激活了一组控制细胞内支架的基因,尤其是一种名为PDLIM5的蛋白。肿瘤血管中的PDLIM5比正常血管更丰富,且肿瘤血管中PDLIM5表达较高的患者通常生存期更短。在多种癌症的小鼠模型中,增强血管内皮中的PDLIM5使肿瘤生长更快并形成更为密集的血管网络,表明该蛋白是驱动肿瘤血管生成的重要因子。
PDLIM5如何构建细胞“触角”
为了观察PDLIM5如何影响血管行为,团队使用了可以详细观察新芽生长的实验体系,如小鼠视网膜的血管生长和三维内皮细胞培养。当PDLIM5在内皮细胞中特异性被删除时,血管新芽推进更慢,箭头细胞减少,丝状伪足显著减少。在显微层面,PDLIM5被发现将两种关键的肌动蛋白束缚蛋白ACTN1和ACTN4连接到形成细胞内框架的长肌动蛋白丝上。这种桥接作用有助于将肌动蛋白丝打包成支撑丝状伪足的刚性束。将PDLIM5上的两个关键位点(命名为S593和F596)发生突变会破坏这种连接、削弱肌动蛋白束缚,并使PDLIM5无法恢复正常的萌发,证明这一分子“握手”对于构建箭头细胞的“触角”至关重要。
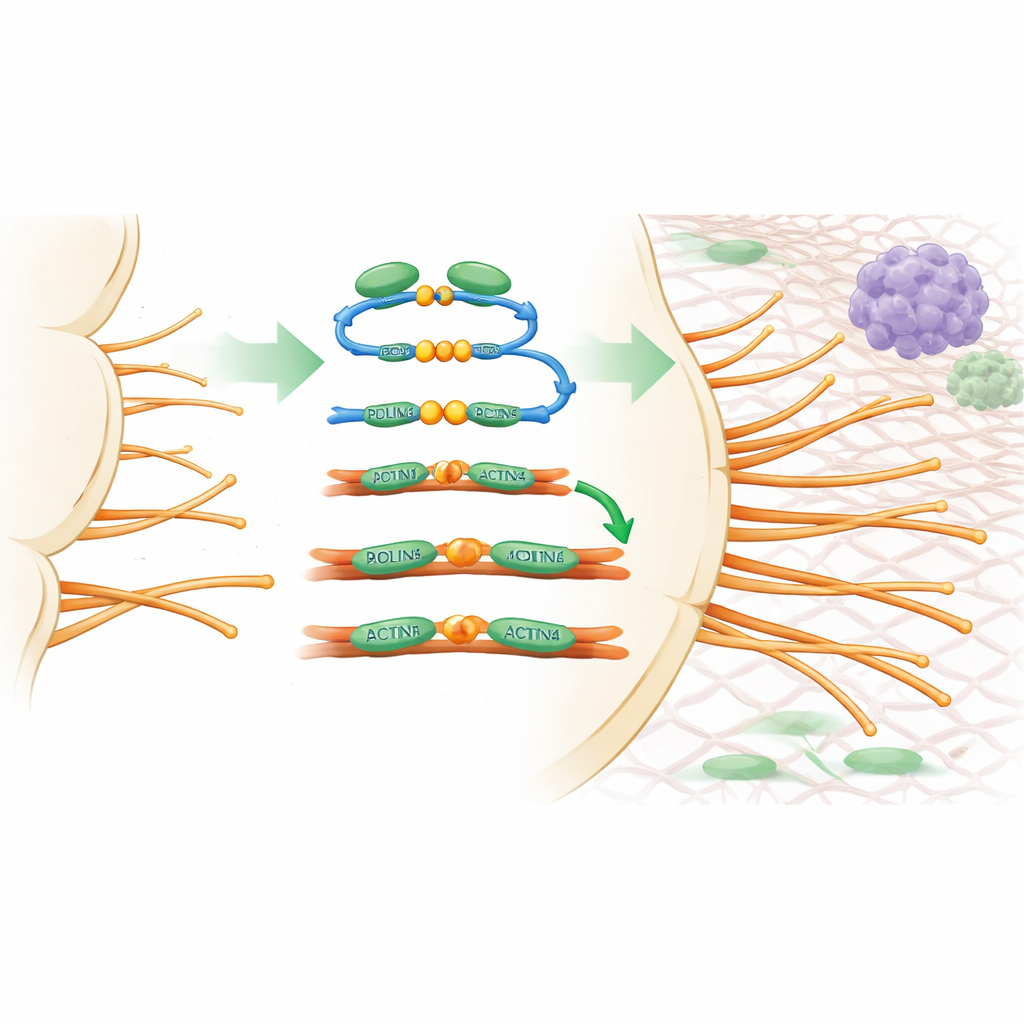
重塑肿瘤血管以帮助免疫系统
出人意料的是,抑制血管内皮中的PDLIM5不仅仅减缓了肿瘤生长。肿瘤血管变得形态更规则、渗漏性降低,并且被稳定支持细胞更好地覆盖。因此,氧气输送改善,严重缺氧的区域减少。这些更“正常化”的血管允许更多免疫T细胞进入肿瘤。PDLIM5的缺失还改变了内皮细胞上黏附分子的组织方式,使T细胞更容易黏附于血管壁并挤出进入肿瘤组织。在通常对免疫检查点药物有抵抗的小鼠肿瘤中,删除PDLIM5使抗PD-L1抗体的治疗效果大大增强,缩小了肿瘤并增加了肿瘤内的辅助和杀伤性T细胞。
这对未来癌症治疗的重要性
综合来看,这些发现表明PDLIM5作为箭头细胞肌动蛋白骨架的核心组织者,促成强大的丝状伪足形成和指向肿瘤的快速血管萌发。在内皮细胞中去除或使PDLIM5失活可减缓肿瘤血供的扩张,使残留血管变得笔直且稳定,缓解氧气匮乏,并吸引免疫细胞进入肿瘤。对患者而言,这意味着设计用于破坏PDLIM5–ACTN1/ACTN4相互作用的药物,既可阻断肿瘤新血管的形成,又可将混乱的肿瘤血管系统转变为更有利于化疗和免疫疗法的网络。
引用: Xu, Z., Shi, Y., Yang, Y. et al. Endothelial PDLIM5 promotes tip cell filopodia formation and tumor angiogenesis by regulating ACTN1/ACTN4-dependent actin bundling. Nat Commun 17, 2103 (2026). https://doi.org/10.1038/s41467-026-68765-x
关键词: 肿瘤血管生成, 内皮箭头细胞, PDLIM5, 肌动蛋白细胞骨架, 癌症免疫疗法