Clear Sky Science · zh
沉默脂质分解决定禁食响应中的寿命
为何关闭脂肪燃烧反而可能有益
许多人认为禁食之所以健康,是因为它迫使机体燃烧脂肪以获取能量。这项在微小线虫秀丽隐杆线虫(Caenorhabditis elegans)中完成的研究颠覆了这一观念。研究者发现,禁食后延长寿命的关键并不是细胞在禁食期间将脂肪燃烧打开得多强烈,而是当食物恢复时它们将脂肪燃烧精确地关闭得有多好。在这种简单动物中理解这种开—关控制,最终可能影响我们为人类设计的禁食和饮食策略。
一种具有代谢柔韧性的简单动物
研究者使用的秀丽隐杆线虫是一种显微级别的线虫,其代谢和衰老通路与人类有许多相似之处。他们让处于青春期的成虫禁食24小时,然后恢复喂食。禁食期间,线虫迅速消耗主要脂质储备——以肠道脂滴形式存在的三酸甘油酯,同时保留必要的胆固醇。恢复喂食后,脂滴和游离脂肪酸谱恢复到禁食前的水平,线虫在肌肉中的能量(ATP)水平保持正常。尽管能量保持稳定,单次的禁食-再喂食循环仍将中位寿命延长约40%,并使动物在晚年保持更高的活力。
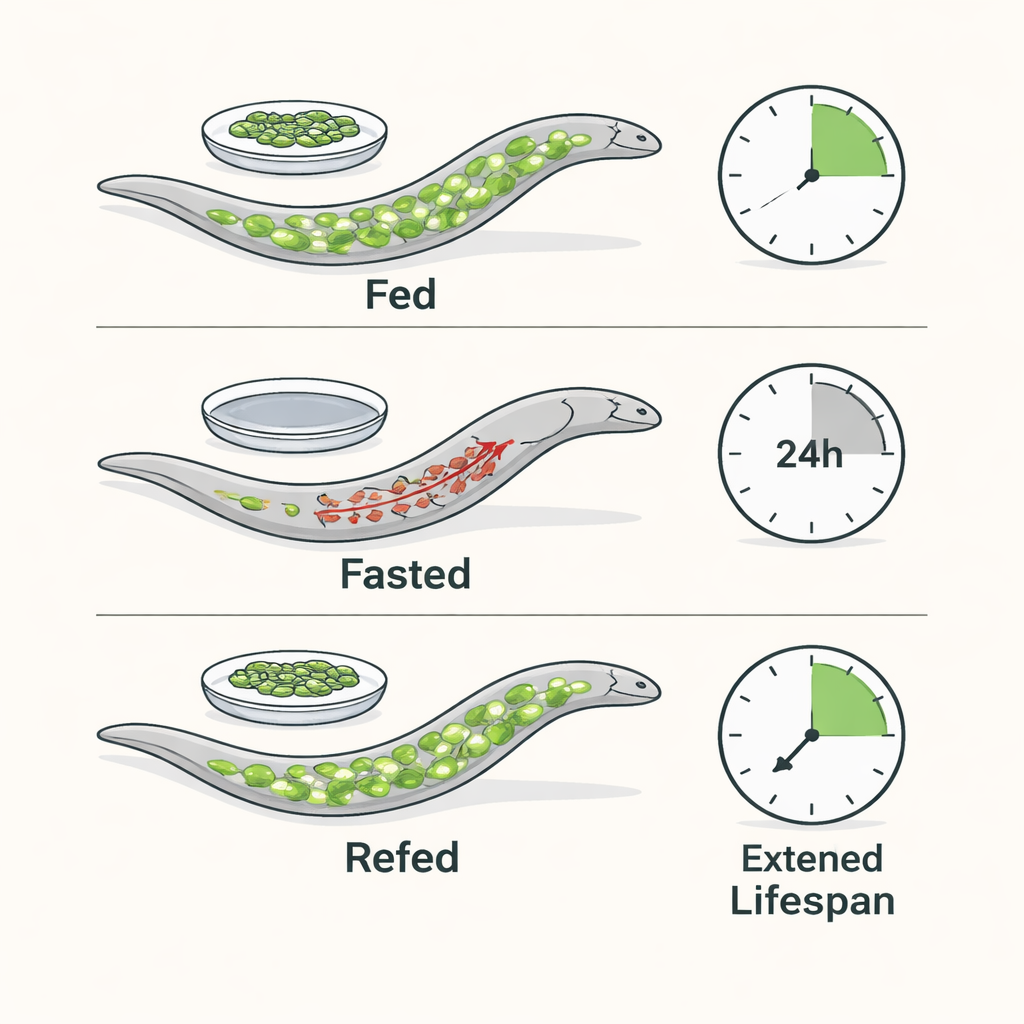
脂肪燃烧并非禁食延年益寿所必需
因为禁食通常促使细胞分解脂肪,团队提出这个脂肪燃烧是否真的是延长寿命所必需的。研究集中在NHR-49上——一种可激活线粒体β-氧化相关基因的核受体,β-氧化是主要的脂肪燃烧途径。缺失NHR-49的线虫在禁食期间无法适当上调这些基因,并表现出更大的ATP下降。然而,令人惊讶的是,它们仍然从禁食中获得了与正常线虫类似的明显寿命延长。研究者用遗传工具阻断脂肪分解的上游步骤时也得到了相同结果。这些实验表明,在禁食期间脂质分解被强烈激活本身对寿命益处在很大程度上并非必需。
一个在时间上关掉脂肪燃烧的开关
如果开启脂肪燃烧不是关键,那么关闭它可能才是。研究显示NHR-49受一种配体非依赖机制控制——与被经典类激素小分子直接翻转不同,其活性由附加到蛋白质本身的化学修饰来调节。在从禁食恢复期间,NHR-49在一个柔性“铰链”区域的相邻丝氨酸残基上获得特定模式的磷酸化。这些带负电的修饰削弱了NHR-49与DNA的结合并促进其从脂肪燃烧基因上被移除,从而在食物恢复时有效地使这些基因沉默。没有这种时序性的关闭,细胞可能持续处于高脂肪燃烧模式,耗尽储备并扰乱长期稳态。
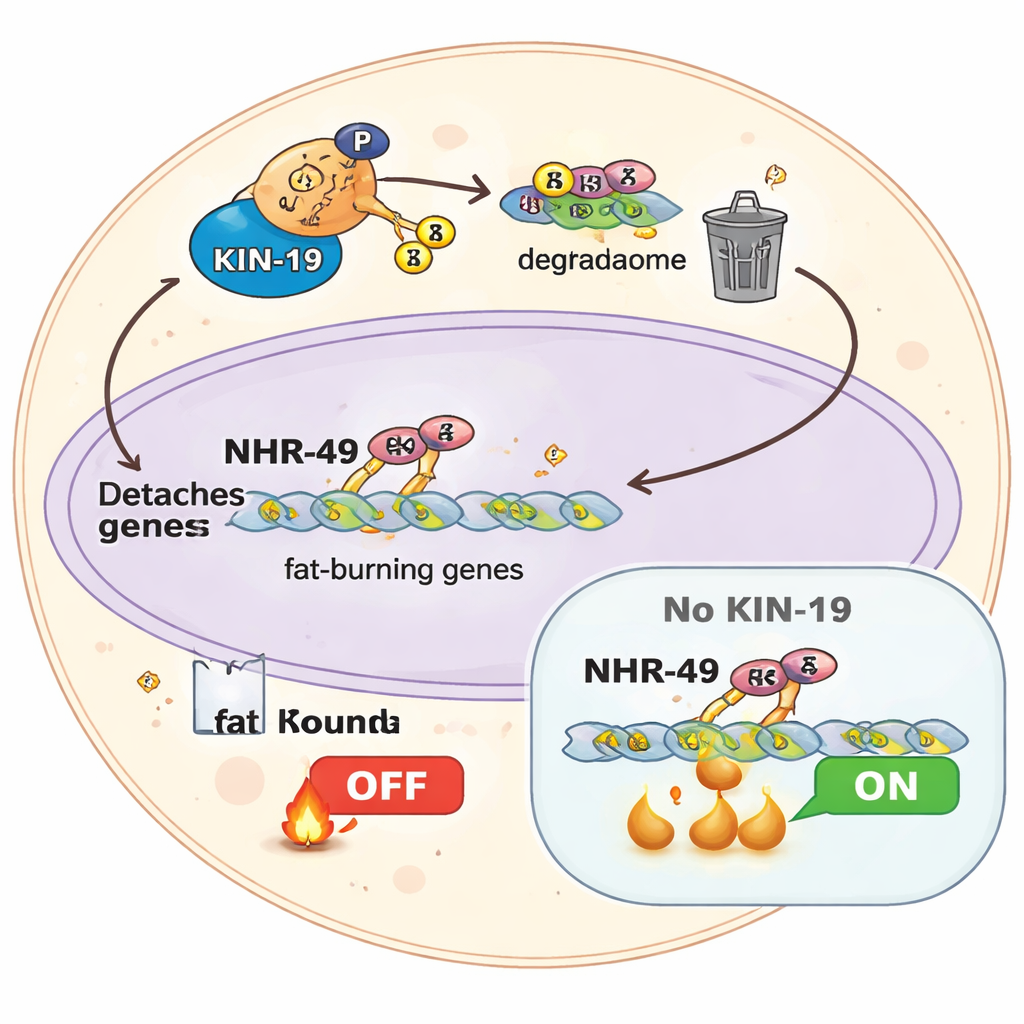
KIN-19:结束禁食的酶
作者鉴定出一种酪氨酸激酶家族的激酶——KIN-19,作为该关闭系统的核心参与者。生化测定显示,一旦NHR-49被初始磷酸化“引发”,KIN-19就能高效地在附近添加更多磷酸。下调KIN-19的线虫表现得像处于永久禁食状态:体型更小、脂质储备低、线粒体形态改变、耗氧量降低,即使食物充足也是如此。它们的基因表达谱类似慢性禁食状态,且在再喂食后能量水平无法正常恢复。关键是,当KIN-19受损时,24小时禁食不再能延长寿命;寿命获益缩减到极小效果。这表明通过KIN-19关闭由NHR-49驱动的脂肪燃烧对于禁食促进健康衰老是必不可少的。
对禁食与健康衰老的启示
对普通读者而言,核心信息是:机体改变档位的能力可能比单一档位的输出强弱更重要。在线虫中,禁食之所以有益,并非因为它们尽可能多地燃烧脂肪,而是因为它们能够在食物恢复时平稳过渡到储存与修复的状态。酶KIN-19通过标记并清除NHR-49来终止脂肪燃烧阶段,防止有害的、永无止境的“紧急”状态。尽管人类的复杂性远超线虫,这项工作暗示,成功的禁食策略可能依赖于代谢中有节律的启动与休整阶段,而不是持续、激进的单一脂肪耗减策略。
引用: Tatge, L., Kim, J., Solano Fonseca, R. et al. Silencing lipid catabolism determines longevity in response to fasting. Nat Commun 17, 1919 (2026). https://doi.org/10.1038/s41467-026-68764-y
关键词: 禁食与寿命, 脂质代谢, 核受体, 代谢柔韧性, 秀丽隐杆线虫衰老