Clear Sky Science · zh
一种稳定的串联抗原嵌合体,可引发强效的疟疾传播减少活性
为何阻断蚊子传播至关重要
现有的疟疾疫苗能够大幅减少幼儿的重症和死亡,但它们留下了一个重大漏洞:不感到不适的人仍可能携带可感染蚊子的寄生虫,从而维持传播。本研究提出了一种下一代疫苗设计,其目的不是仅保护某一个人,而是切断人类与蚊子间的感染链。通过精确设计关键寄生虫蛋白如何呈递给免疫系统,研究者旨在诱导出使蚊子成为不良宿主的抗体,从而帮助社区更接近消除目标。
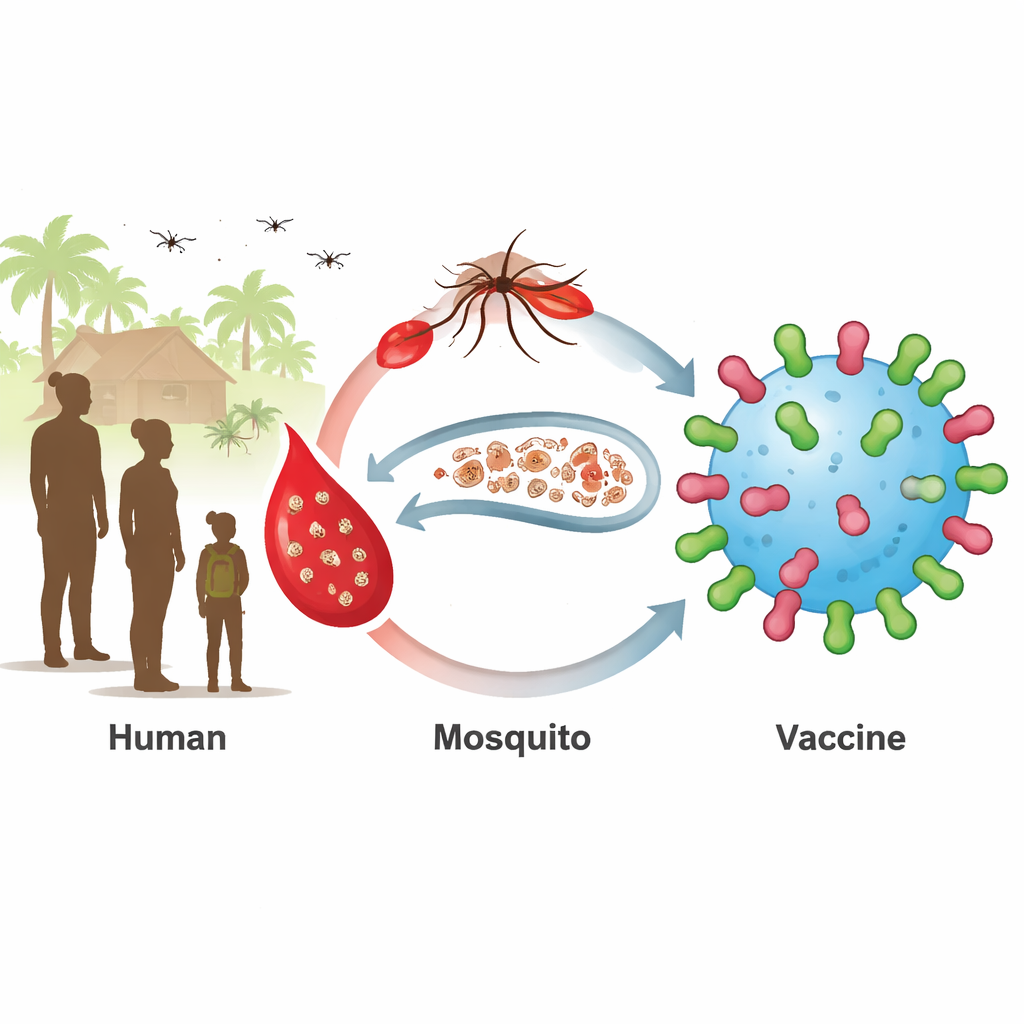
维持疟疾传播的隐匿储库
当前的疟疾疫苗侧重于肝脏和血液中的早期感染阶段。它们在幼儿中效果最好,但年长儿童和成人常常无症状地携带成熟的性态寄生虫,称为配子体。当蚊子叮咬这些人时,会带走寄生虫并进一步传播。两种位于这些性态表面的寄生虫蛋白,称为Pfs230和Pfs48/45,是所谓阻断传播疫苗的有吸引力的靶点。针对这些蛋白片段的疫苗已进入临床试验,但在所有受试者中激发强烈且持久的抗体反应方面一直存在困难。
为免疫系统构建更聪明的诱饵
为改进早期设计,作者采用了结构生物学方法,从原子层面研究人源强效抗体如何结合Pfs230和Pfs48/45。他们鉴定出一些小区域(或抗原表位),这些区域在阻断寄生虫在蚊子体内发育方面尤为有效。同样重要的是,他们绘制出“非功能性”表位,这些表位会吸引能结合但不能阻断传播的抗体——实质上是在浪费免疫资源。利用计算建模和蛋白工程工具,他们将Pfs230中最有力的区域(其第一区域)与Pfs48/45的关键区域(其第三区域)融合为单一、精心排列的蛋白,称为稳定化串联抗原嵌合体(STAC)。
隐藏无用靶点,保留有用表位
挑战在于以模拟它们在寄生虫上排列的方式将这两个结构域一起呈现,同时物理性地遮蔽在完整蛋白中本应被埋藏的非功能性表面。研究团队反复改进短连接肽和两个结构域之间的界面,测试每个版本的稳定性、正确折叠性以及是否仍能结合一组表征良好的抗体。先进的设计软件建议了能够收紧界面并改善细胞培养表达的突变。通过X射线晶体学、小角X射线散射和冷冻电子显微镜的结构研究证实,在最终的STAC构建体中,期望的表位得到高保真地展示,而已知的无益部位被空间上阻挡。
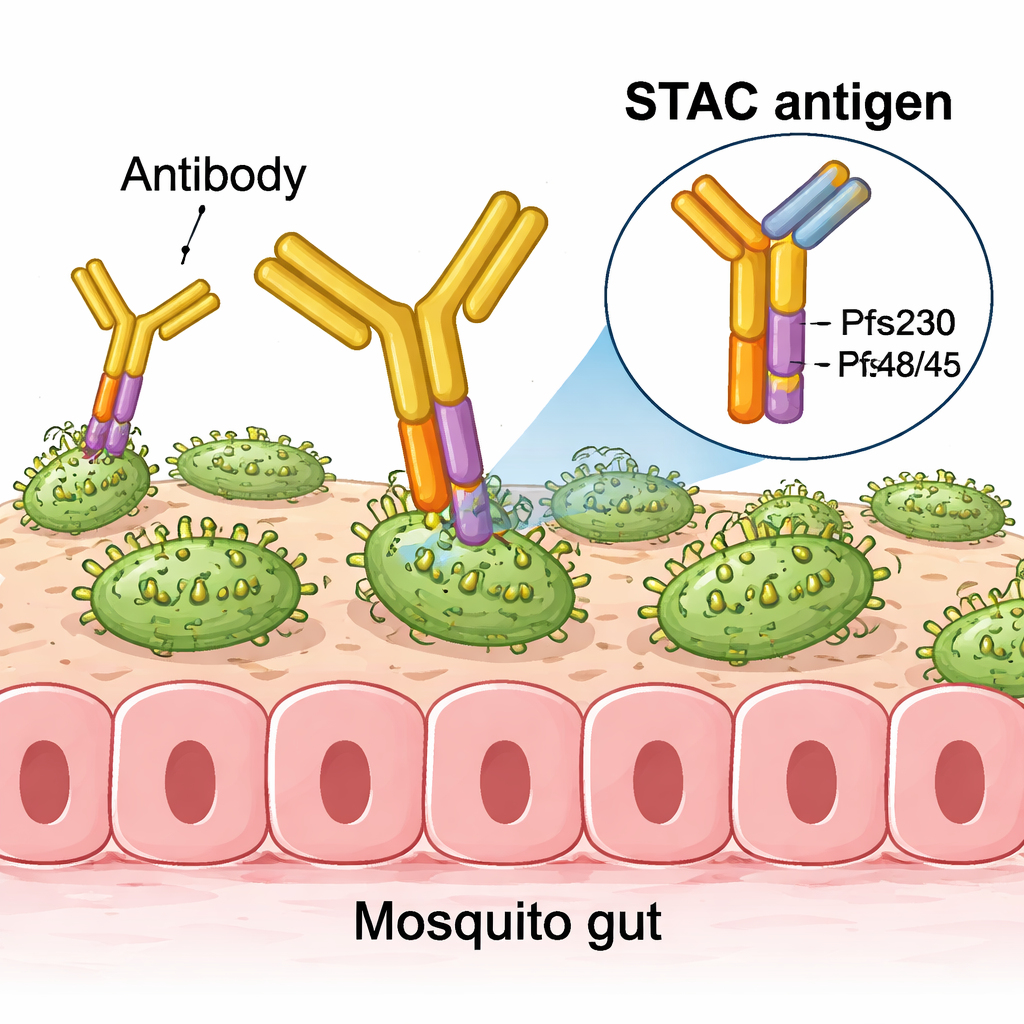
从单分子到强效纳米颗粒
在小鼠中的测试表明,当将STAC连接到专用脂质体或自组装蛋白纳米颗粒上时,它能诱发强烈的抗体反应,显著降低在标准蚊子喂食测定中寄生虫的发育。在相等或更低剂量下,STAC通常能匹敌或优于分别使用Pfs230和Pfs48/45片段的疫苗——无论是单独给药、混合给药,还是在同一颗粒上共同展示。在高灵敏度的稀释小鼠血清测试中,STAC装饰的纳米颗粒诱导的抗体在多倍稀释后仍保持较好的阻断传播活性,表明其诱导的反应尤其强且针对性明确。
这对疟疾控制意味着什么
对非专业读者来说,核心思想是STAC是一种定制的诱饵,向免疫系统准确展示疟疾寄生虫中最关键的、能阻断传播的部分,同时隐藏那些分散注意力但无助于防护的区域。在动物模型中,这一设计产生的抗体使寄生虫难以在蚊子体内完成生命史,即便抗体水平相对较低。如果在人类中能取得类似效果,STAC可成为现有疟疾疫苗的强力伙伴:在保护接种者免受疾病的同时,也缩减社区内的感染性储备。更广泛地说,这项工作展示了如何利用细致的结构洞察与蛋白工程来设计多组分疫苗,使其更强效、稳定且潜在地更廉价生产。
引用: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
关键词: 疟疾疫苗, 阻断传播, Pfs230, Pfs48/45, 纳米颗粒免疫原