Clear Sky Science · zh
NONO–HOXA1–Wnt 轴在心肌细胞分化中的关键作用
为什么微小的心脏细胞与我们息息相关
每一次心跳都依赖于在胚胎期形成的数十亿种专门化肌肉细胞。当这一过程出现问题时,婴儿可能会出生时就带有严重的心脏缺陷。本研究利用人类干细胞揭示了一个关键的调控系统——由名为 NONO 和 HOXA1 的分子及著名信号通路 Wnt 构成——它帮助早期细胞决意走上健康心肌的命运。理解这套隐蔽的电路,或可最终为先天性心脏病的更好诊断与治疗提供线索。
从空白细胞到早期心脏构建者
研究者从人诱导多能干细胞出发——这类细胞具有分化为几乎任何细胞类型的潜能。采用标准方案,他们将这些细胞诱导为心肌细胞,即心脏的搏动细胞。删除 NONO 基因后,成功获得心脏细胞的数量大幅减少。那些通常在细胞离开原始状态并走向心脏谱系时出现的早期标志显著下降。单细胞 RNA 测序显示,许多缺失 NONO 的细胞在分化途中停滞,滞留于一种未成熟的类胚中胚层(mesendoderm)状态,而未能继续向成熟心肌细胞发展。
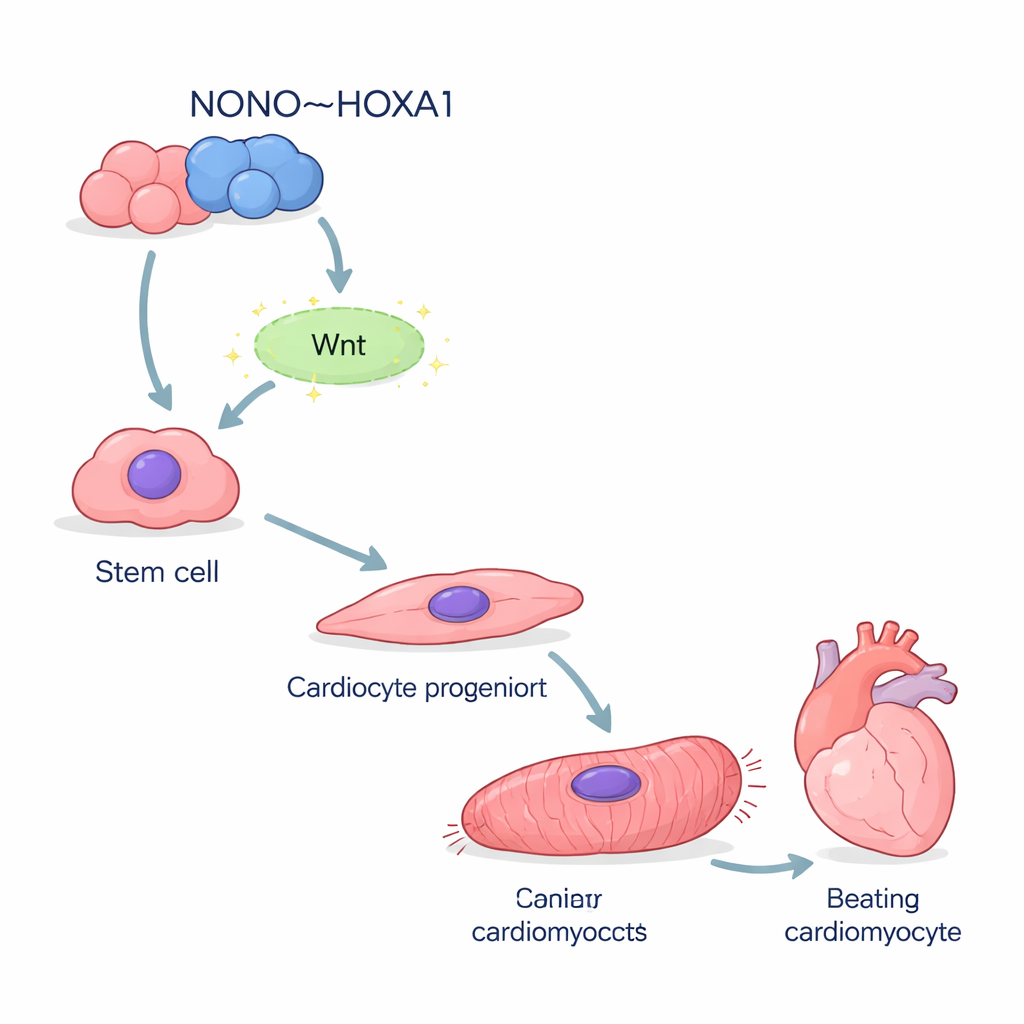
当支架缺失时,心肌细胞表现不佳
即便在没有 NONO 的情况下有少数细胞分化为心肌细胞,它们也远非健康。它们的结构蛋白——构成肌节(sarcomere)的组分——表达显著降低。在显微镜下,大多数突变细胞显示出紊乱、断裂的收缩纤维,而非正常细胞所见的整齐条纹。电子显微镜确认,通常的 Z 盘“横档”缺失或畸形。功能上,这些细胞跳动更慢且不规则。钙浪涌(触发每次心跳的电活动)测量显示波形紊乱、峰值延迟且恢复缓慢,反映出钙转运通道在基因表达层面的缺陷。
挽救分化并揭示 NONO–HOXA1 的协作
为检验这些问题是否确由 NONO 丧失引起,团队在分化的最初两天通过可药物诱导的方式重新引入 NONO。短暂的 NONO 激活在很大程度上恢复了早期心脏基因的上调,增加了搏动性心肌细胞的比例,并重建了有序的肌节与 Z 盘。基因表达谱分析证实,许多肌肉收缩与心脏发育相关基因恢复到了接近正常的水平。相比之下,来自患者的突变版 NONO 无法挽救这些表型,支持这些变异通过扰乱早期程序致病的观点。蛋白相互作用实验证明,NONO 能物理结合转录因子 HOXA1,这种结合稳定了 HOXA1 并有助于其形成结合 DNA 所需的二聚体。
开启 Wnt 信号以决定心脏命运
对这些蛋白在基因组上的结合位点进行绘图显示,NONO 和 HOXA1 经常占据相同的调控区域,包括那些控制重要早期心脏和 Wnt 通路基因的区域。缺失 NONO 时,HOXA1 在许多这些位点上的结合减弱,尤其是那些驱动前心脏中胚层(前期形成心脏组织)的基因。下游的 Wnt/β-连环蛋白通路——通常有助于启动中胚层与心脏发育——也受到抑制:核内 β-连环蛋白累积减少,Wnt 响应性报告系统的活性降低。在分化最早期通过提高 Wnt 激动剂的剂量加强 Wnt 信号,能够部分克服 NONO 缺失的影响,恢复更多的心脏细胞并提升心脏基因表达。
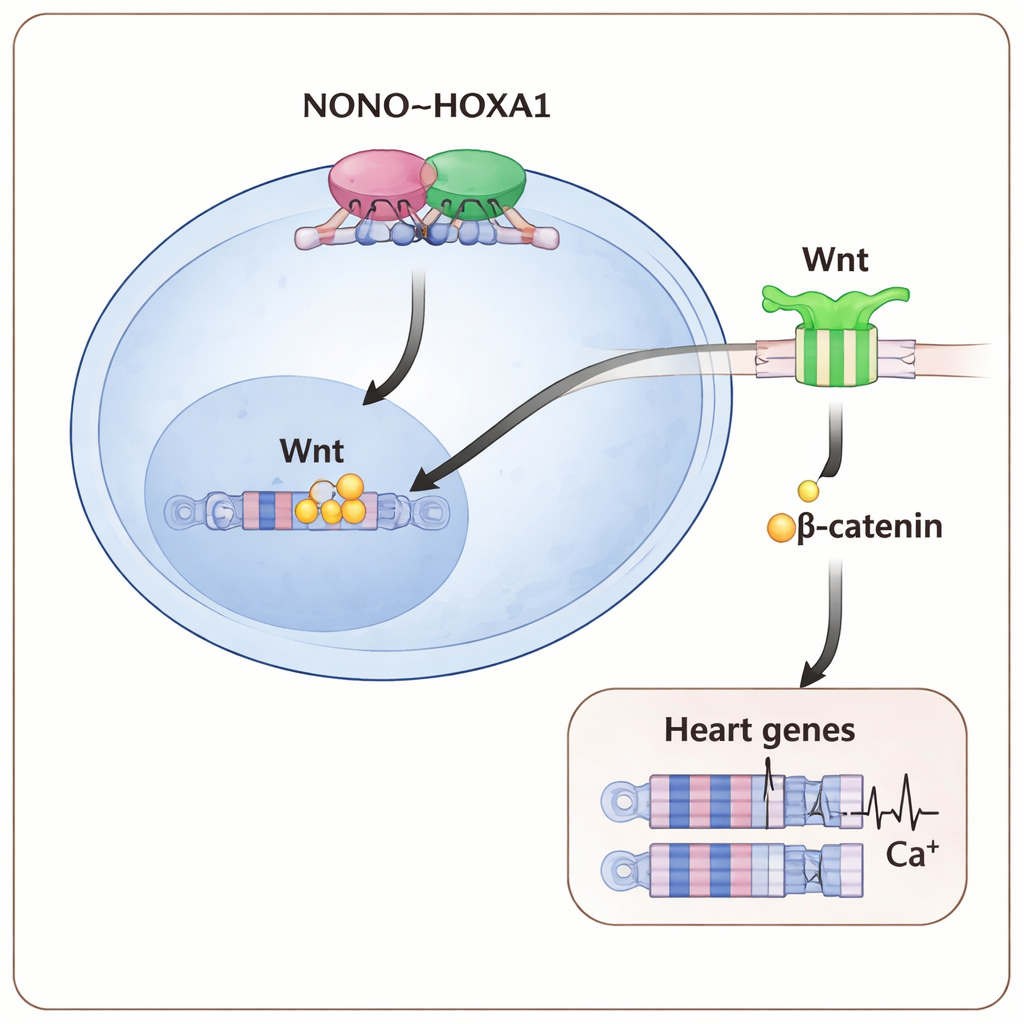
对理解先天性缺陷的意义
对非专业读者而言,核心信息是:一支由 NONO 与 HOXA1 协同调整 Wnt 信号的小分子团队,充当了早期的“交通指挥官”,指示幼稚细胞成为心肌并使其具备正常搏动的能力。当 NONO–HOXA1–Wnt 轴的任何部分受扰动时,细胞会犹豫、关键心脏基因无法开启,最终形成的心肌细胞在结构和电生理上都更脆弱。这些见解为为何 NONO 的突变与先天性心脏病相关提供了更清晰的分子解释,并指明了在干细胞模型中操控该通路,或未来用于预防或修复心脏畸形的潜在策略。
引用: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
关键词: 先天性心脏病, 心肌细胞分化, Wnt 信号通路, 干细胞心脏模型, 基因调控