Clear Sky Science · zh
对1032例脑转移瘤的蛋白组学-基因组学图谱揭示分子亚型、免疫景观及治疗脆弱点
为何癌症会转移到大脑至关重要
随着癌症诊疗的进步,越来越多患者活得足够久以致肿瘤有机会转移到新的部位,包括大脑。脑转移现在已成为一种常见且往往毁灭性的并发症,但临床上仍多按原发肿瘤的起源—肺、乳腺、皮肤、结肠—来治疗,而不是按癌细胞如何适应在脑内生存来划分。本研究构建了一个包含一千多例脑转移瘤的详尽“图谱”,旨在揭示其隐含的生物学特征、与脑内细胞和免疫系统的相互作用,以及潜在的新治疗机会。
绘制大型脑肿瘤图谱
研究者收集了1032例来源于多种原发癌的脑转移样本,另有数十例配对的原发肿瘤以及若干侵袭性原发性脑肿瘤作为比较。他们结合了多种前沿方法:DNA与RNA测序、大规模蛋白质与代谢物检测、单细胞与空间水平的肿瘤与免疫细胞定位图谱,以及在体外培养的患者来源类器官。通过整合这些层面的数据,目标不只是列出基因清单,而是观察整个生物系统在脑转移中的表现。
脑转移瘤的四种常见“性格”
尽管来自不同器官,脑转移瘤反复落入四个主要分子亚型。一类称为 BrMS1,呈现“类神经”特征:肿瘤细胞及周围组织表达许多脑和神经细胞相关程序,并显示相对活跃的免疫监视。BrMS2 为“免疫浸润型”,充斥着免疫细胞,尤其是T细胞,并表现出上皮–间质转化(EMT)程序,这会松动细胞间黏附并重塑局部环境。BrMS3 为“代谢型”,以高度活跃、重编程能量利用的癌细胞为主——例如脂肪酸代谢和氧化磷酸化通路。BrMS4 为“增殖型”,以快速细胞分裂、干样特征和高度基因组不稳定性为标志,但显著缺乏免疫细胞。
肿瘤微环境揭示的线索
通过单细胞及空间分辨率的放大观察,团队显示每个亚型在大脑中占据不同的“社区”。BrMS1 病灶富含星形胶质细胞和神经元等脑支持细胞,提示肿瘤在很大程度上模仿并劫持正常脑组织。相比之下,BrMS2 肿瘤点缀着密集的T细胞簇,包括大量表达PD‑1等检查点分子的“耗竭”T细胞,并伴有活化的血管与炎性信号。BrMS3 病灶位于代谢活动旺盛的区域,而 BrMS4 则形成快速分裂细胞的孤岛,周围多为免疫贫乏的地带。总体来看,研究发现——在脑转移而非原发肿瘤中——强烈的上皮–间质转化常与更高的T细胞浸润并存,提示该程序可能有助于免疫细胞进入肿瘤。
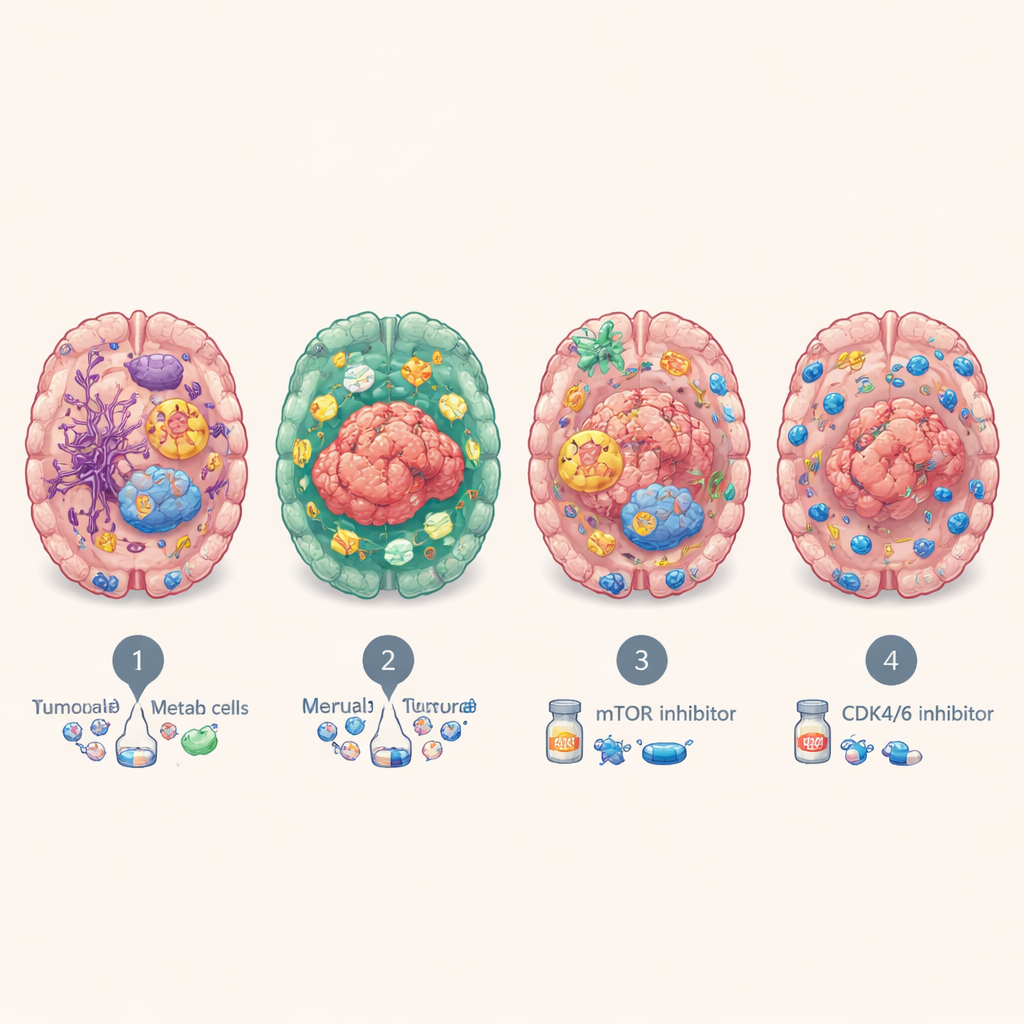
对治疗与患者结局的启示
这些分子“性格”并非纯学术性的区分。具有免疫浸润型 BrMS2 的患者总体生存倾向优于增殖型 BrMS4,后者一贯预后最差。通过在患者来源类器官上测试药物,研究团队发现代谢型 BrMS3 对阻断 mTOR 信号通路(该通路调控细胞生长与代谢)特别敏感,而快速分裂的 BrMS4 对 CDK4/6 抑制剂(可减缓细胞周期的药物)更为脆弱。另有独立分析提示 BrMS1 可能对放疗反应更好,而 BrMS2 那种炎性、检查点富集的环境可能更有机会从使耗竭T细胞恢复活性的免疫疗法中获益——不过这一点还需在脑转移患者中直接验证。
这对脑转移患者意味着什么
该图谱表明,一旦癌细胞进入大脑,它们往往会汇聚到少数几种共享的生物学状态,这些状态与原发部位无关。了解某位患者的脑转移瘤是类神经、免疫丰富、代谢型还是高度增殖型,未来可能有助于指导更个体化的治疗选择——例如在放疗、免疫疗法或针对代谢或细胞分裂的药物之间进行选择。尽管目前这项工作尚未改变标准治疗,但它为未来研究和临床试验提供了详尽的路线图,旨在将这些分子脆弱点转化为更好、更精准的治疗方案,造福面临脑转移的患者。
引用: Yang, Z., Wei, S., Duan, H. et al. A proteogenomic atlas of 1032 brain metastases identifies molecular subtypes, immune landscapes, and therapeutic vulnerabilities. Nat Commun 17, 2038 (2026). https://doi.org/10.1038/s41467-026-68748-y
关键词: 脑转移, 肿瘤亚型, 肿瘤微环境, 癌症免疫治疗, 癌症代谢