Clear Sky Science · zh
磷脂成分强烈影响β桶蛋白在纯化细菌外膜中的组装
为什么细菌外衣很重要
耐药的“超级细菌”构成日益严重的威胁,因为许多抗生素根本无法穿透它们坚固的外层防御。该研究着眼于革兰氏阴性细菌(如大肠杆菌)防御的一项关键组成:一种由桶状蛋白和特化脂质填充的保护性外衣。通过解析这些脂质混合物如何控制外衣的构建,作者揭示了在设计未来抗生素时可被利用的薄弱点。
双层护盾
革兰氏阴性细菌的特殊之处在于它们具有两层膜。内膜负责日常细胞功能,而外膜则像一件坚固的雨衣,阻挡许多毒素和抗生素。这一外层由两类脂质构成:靠内侧的是常见的磷脂,而外侧则是刚性较强的糖脂——脂多糖(LPS)。穿过这层外壳的是大量“β桶”蛋白——形成营养物质孔道和门控的中空圆柱体。一台被称为BAM(桶装配机器,barrel assembly machine)的分子机器负责将这些蛋白折叠成形并插入外膜。
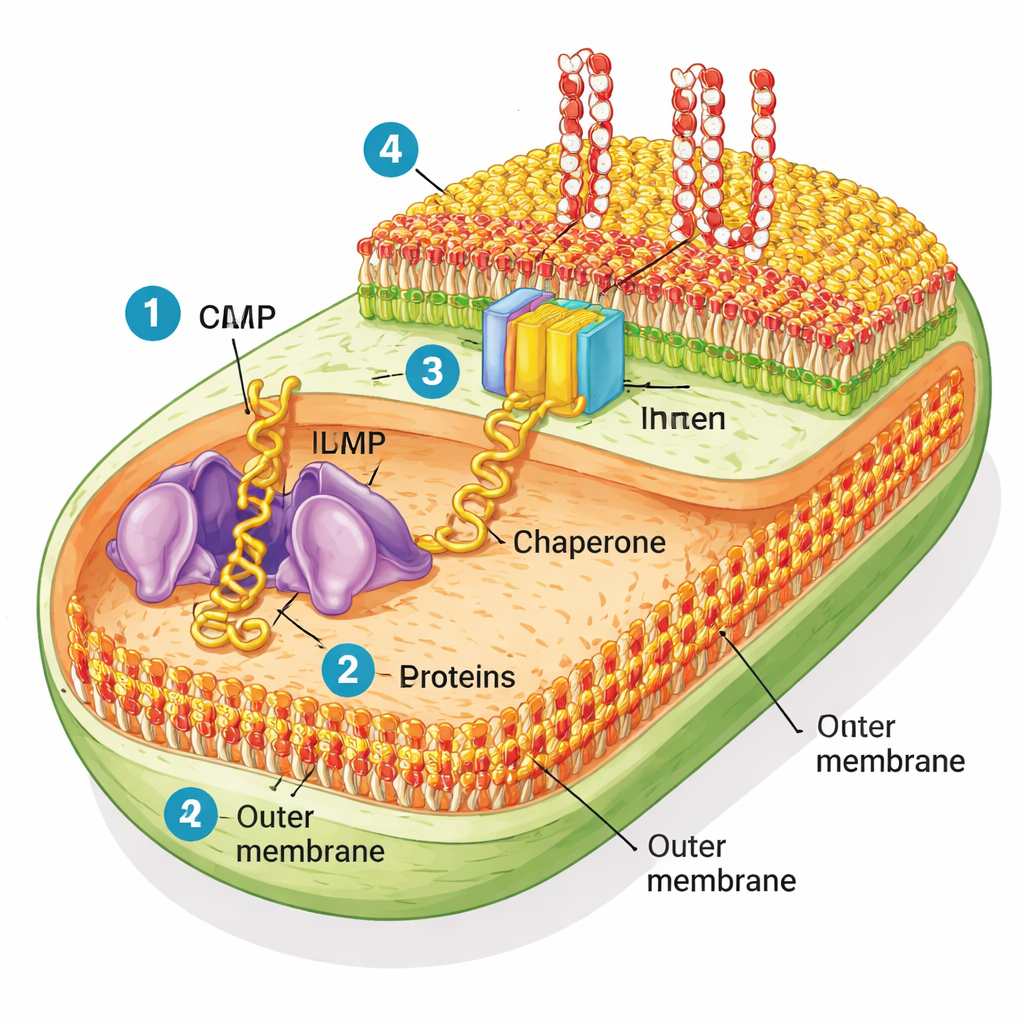
在试管中重建细菌外衣
为了在更真实的环境中观察BAM的功能,研究者从大肠杆菌中纯化出外膜片段,制成他们所谓的“原生外膜”微泡。与许多实验中使用的简单人工膜不同,这些原生膜保持了完整的蛋白和脂质组成。团队随后使用无细胞蛋白质合成系统从头构建新的外膜蛋白,并观察原生微泡中的BAM能否折叠并插入这些蛋白。他们以一种模型β桶蛋白EspP及其他几种为研究对象。在助胞蛋白SurA存在时,原生膜中的BAM能够高效折叠EspP;而一种已知针对BAM的抗生素darobactin能阻断这一过程——这清楚表明天然的机器仍然具有活性。
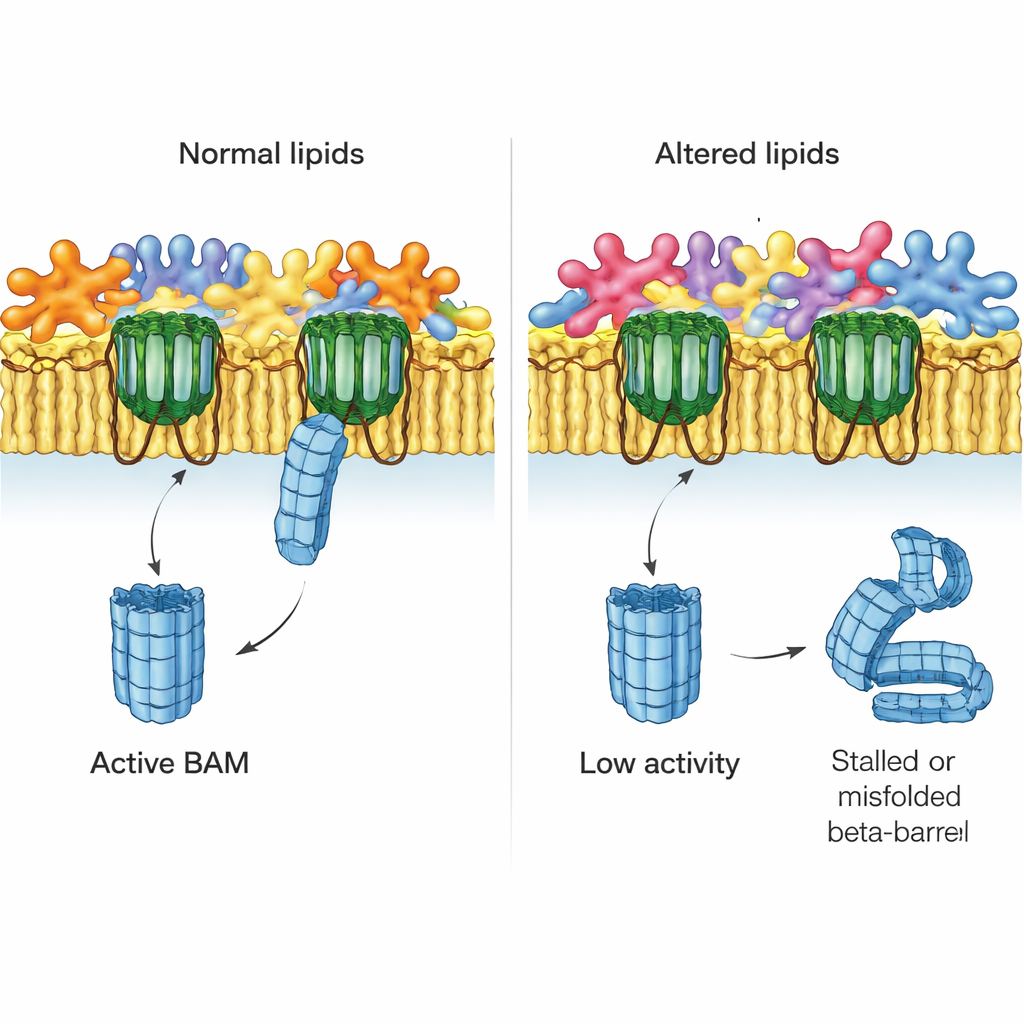
当脂质混合失衡时
作者接着探讨当外膜的脂质平衡被破坏时会发生什么。他们研究了缺失通常用于纠正外叶片中错位磷脂关键系统的大肠杆菌突变株。一个系统MlaA负责将游离的磷脂运回内膜;另一个酶PldA负责将其分解。使用来自这些突变株的原生膜,团队发现缺失MlaA的菌株中BAM驱动的EspP组装明显下降,而缺失PldA时则严重受损。这些影响并非由于BAM本身或其他主要蛋白的丢失——这些蛋白仍保持正常水平——因此罪魁祸首指向改变后的脂质环境。
详细绘制脂质版图
为将功能与化学成分联系起来,研究者开发了一种高灵敏度的质谱方法,用于在全细胞和纯化外膜中列出数百种单独的磷脂。在正常大肠杆菌中,他们证实一种脂质(磷脂酰乙醇胺,PE)在外膜中富集,而其他脂质(磷脂酰甘油和心磷脂)则相对匮乏。他们还发现“溶血磷脂”(仅有一条脂肪链、易使膜弯曲)在外膜中出人意料地浓集。在突变株中,尤其是缺失PldA的那些,这些分布模式被打乱:内外膜之间的常见差异缩小甚至逆转,脂肪链的长度和种类也发生变化。脂质谱最紊乱的菌株正是BAM活性最差的那些。
对抗生素策略的启示
综合来看,这项工作表明外膜并非蛋白质的被动支架。其精确的磷脂构成强烈影响BAM构建保持细菌存活所需β桶孔道的能力。当脂质平衡被扰乱时,能够正常工作的BAM复合体数量减少,且部分复合体的工作速度变慢。尽管活细菌可以以试管体系无法做到的方式进行补偿,这项研究仍强调了通过调节或干扰特定脂质来削弱细菌外衣的可能性。这一见解为开发新型药物打开了途径——这些药物可以直接靶向BAM,或微妙地破坏外膜的脂质平衡,使即便是最难对付的革兰氏阴性细菌也更易受攻击。
引用: Nilaweera, T.D., Brandes, N.T., LaCroix, I.S. et al. Phospholipid composition strongly affects the assembly of β barrel proteins into purified bacterial outer membranes. Nat Commun 17, 1915 (2026). https://doi.org/10.1038/s41467-026-68743-3
关键词: 革兰氏阴性细菌, 外膜蛋白, β桶组装, 细菌脂质, 抗生素耐药性