Clear Sky Science · zh
犬尿喹啉酸通过调节肠道微生物介导化疗引起的肠毒性
这对正在接受化疗的人为何重要
化疗能挽救生命,但常伴随令人难受的肠道副作用——疼痛、腹泻、体重下降——这些问题可能迫使医生减量或提前停止治疗。该研究揭示了一条介于血液化学物质、免疫细胞与肠道微生物之间的隐性连锁反应,帮助解释为何一种常见的抗癌药物氧化铂会对肠道造成严重损伤,并指向在不削弱抗癌疗效的前提下保护患者的新方法。
治疗与肠道损伤之间的化学纽带
研究者从接受含氧化铂化疗的结直肠癌患者入手。他们将出现严重肠道副作用的患者与耐受性较好的患者的血样进行了比较。通过靶向代谢物分析,发现色氨酸的多种降解产物在高毒性组中升高,其中一种分子——L‑犬尿喹啉酸——尤为显著。血中L‑犬尿喹啉酸含量较高的患者同时表现出更多的炎症迹象和更低的白细胞计数,提示该分子可能与治疗相关损伤直接相关。
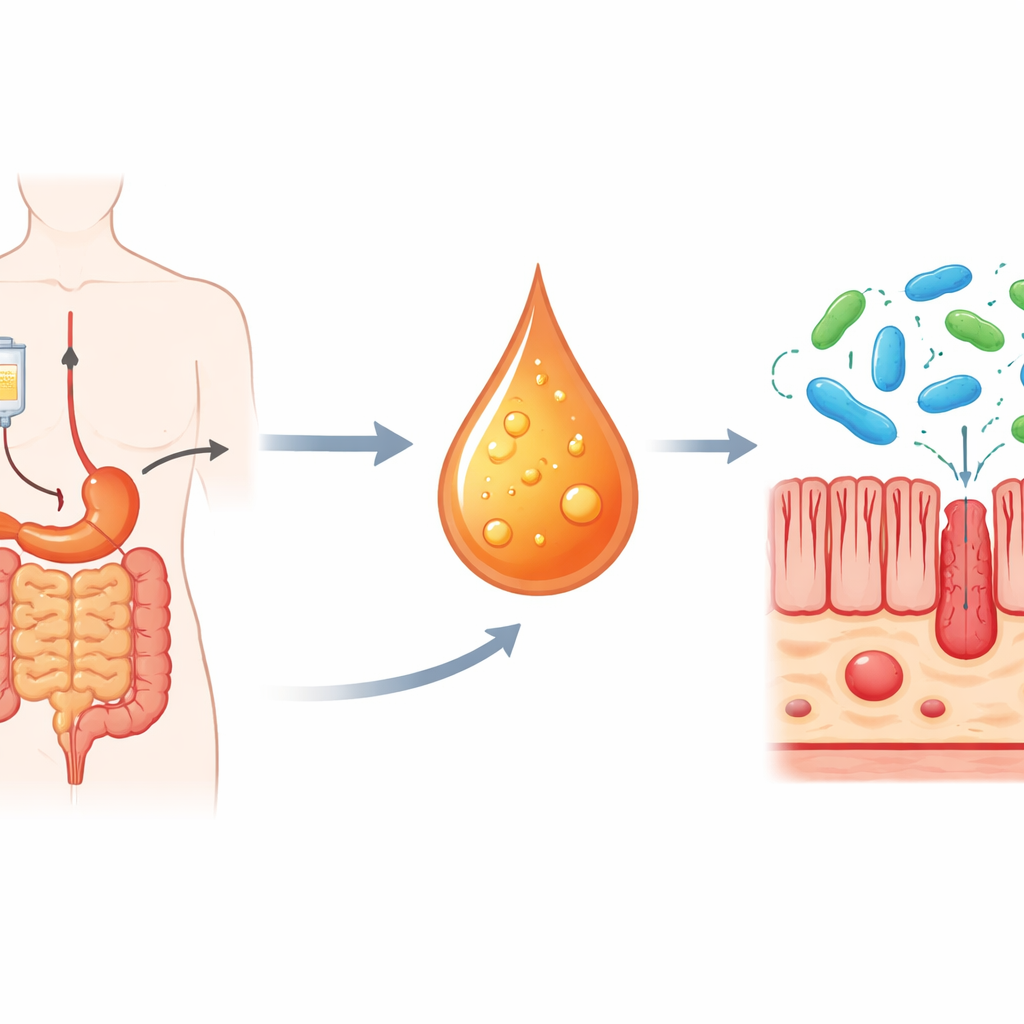
在小鼠中证明因果关系
为超越相关性,团队转向小鼠模型。健康小鼠接受高剂量氧化铂后出现典型的肠道损伤表现:体重下降、结肠变短、肠壁肿胀、分裂细胞减少以及肠上皮细胞死亡增加。这些小鼠血中L‑犬尿喹啉酸水平也显著上升,与人类数据相呼应。向接受氧化铂的小鼠额外补充L‑犬尿喹啉酸会使肠道损伤加重——但药物对肿瘤的杀伤作用并未受影响。相反,去除或阻断将色氨酸转化为L‑犬尿喹啉酸的酶IDO1的小鼠,对肠毒性表现出更强的抵抗力,同时仍从化疗中获益。
免疫细胞与肠道微生物成为交叉地带
进一步研究中,科学家们探寻了治疗期间哪些细胞负责产生过量的L‑犬尿喹啉酸。他们发现氧化铂刺激某些免疫细胞(CD8 T细胞)释放信号蛋白干扰素‑γ,后者在邻近的髓系细胞中开启IDO1。仅在髓系细胞中缺失IDO1的转基因小鼠产生的L‑犬尿喹啉酸明显更少,并受到肠道损伤的保护,而仅在肠上皮细胞中删除IDO1效果甚微。与此同时,肠道微生物组成发生了变化。在正常小鼠中,氧化铂和高水平L‑犬尿喹啉酸与一种有益细菌Lactobacillus johnsonii的减少相关。相比之下,L‑犬尿喹啉酸较低的小鼠保持了较高的L. johnsonii水平。当用抗生素消灭肠道细菌时,低L‑犬尿喹啉酸带来的保护作用消失;而将低犬尿喹啉酸小鼠的菌群移植给正常小鼠后,受体小鼠对氧化铂的肠道损伤变得更有抵抗力。
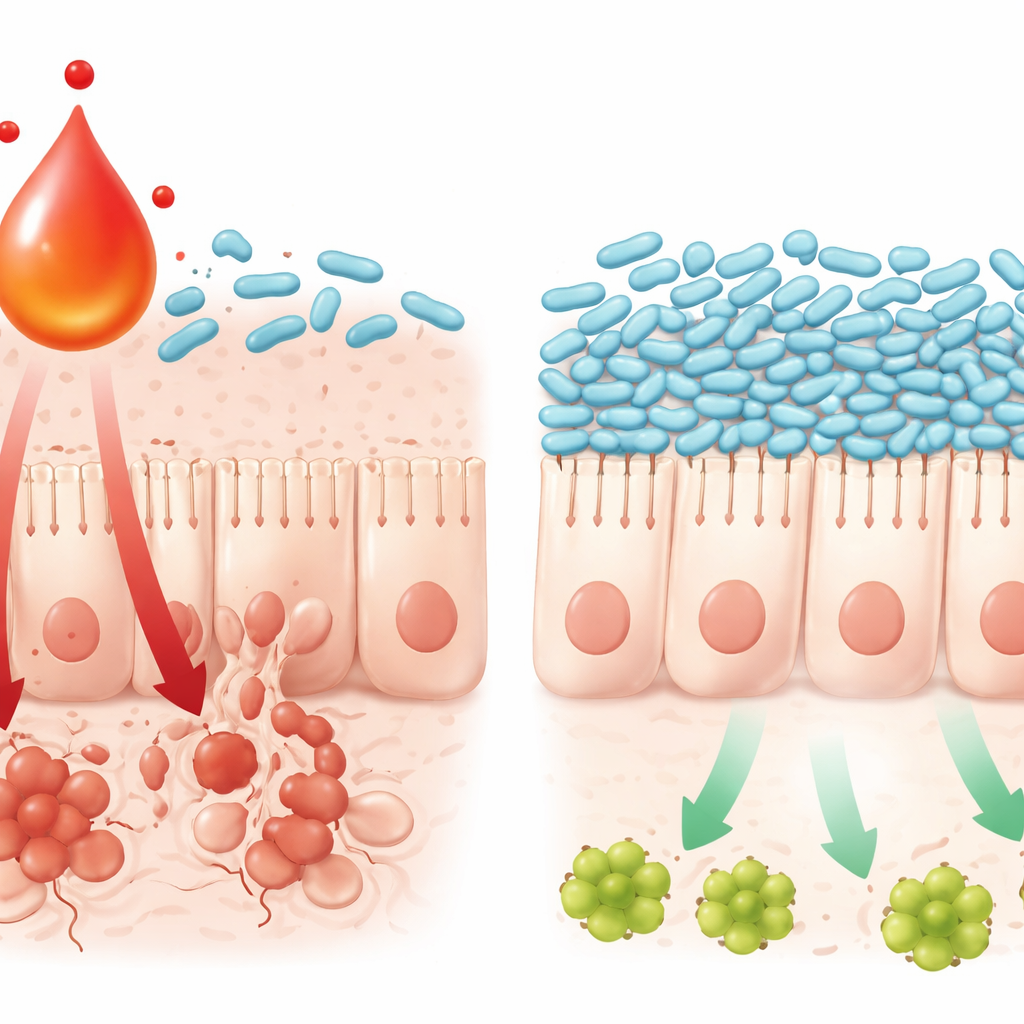
一种代谢物如何驱动肠上皮细胞死亡
研究还追踪了这种化学—微生物相互作用如何损伤肠上皮。高水平L‑犬尿喹啉酸与肠组织中一条知名的炎症通路TNFα/JNK活性增加有关,该通路促使细胞走向程序性死亡。在细胞培养中,氧化铂与L‑犬尿喹啉酸共同作用使肠细胞更容易激活该通路并死亡,而加入L. johnsonii能削弱该信号并维持细胞存活。L‑犬尿喹啉酸本身可在培养皿中抑制L. johnsonii的生长并削弱其生存机制,这有助解释当该代谢物积累时该细菌为何消失。综上所述,这些发现勾勒出一个自我强化的循环:化疗触发免疫信号,免疫细胞提高L‑犬尿喹啉酸产生,这破坏了像L. johnsonii这样的有益菌群,而改变后的微生物群又反过来放大导致肠上皮细胞死亡的炎症信号。
治疗期间保护患者的新路径
令人鼓舞的是,工作还指向了可行的干预策略。用一种名为Epacadostat的IDO1抑制剂处理小鼠可以降低L‑犬尿喹啉酸水平,并明显减少氧化铂引起的肠道损伤,同时不削弱对肿瘤的控制。作为互补方法,研究团队还改造了一株无害的大肠杆菌,使其在肠内过度表达一种能分解L‑犬尿喹啉酸的酶。给予这些工程菌的小鼠同样免受肠毒性侵害,且不影响化疗的抗癌作用。补充L. johnsonii本身也缓解了症状并保护了肠道结构。
这对癌症患者意味着什么
综合来看,这项研究表明单一的治疗驱动代谢物——L‑犬尿喹啉酸——在化疗、免疫系统、肠道微生物和肠道损伤之间扮演关键中介的角色。研究显示,通过阻断其生成、增强其分解或恢复保护性细菌,都可以减轻化疗对肠道的冲击,为在抗癌治疗过程中为患者提供附加保护、保持更好体力与舒适度开辟了道路。
引用: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
关键词: 化疗副作用, 肠道微生物组, 色氨酸代谢, L-犬尿喹啉酸, 结直肠癌